Dạng bài tập phản ứng Este hóa
VnDoc xin giới thiệu tới bạn đọc Dạng bài tập phản ứng Este hóa. Hy vọng tài liệu sẽ giúp các bạn giải bài tập Hóa học lớp 12 hiệu quả hơn.
Hóa học 12: Dạng bài tập phản ứng Este hóa
Phương pháp giải bài tập phản ứng Este hóa
Phản ứng este hóa với ancol là phản ứng quan trọng của axit cacboxylic.
- Phương trình phản ứng tổng quát:
R(COOH)x + R’(OH)y ![]() Ry(COO)xyR’x + xyH2O
Ry(COO)xyR’x + xyH2O
- Nếu axit cacboxylic và ancol tham gia phản ứng đều thuộc loại đơn chức (hay gặp) thì phản ứng có phương trình dạng:
RCOOH + R'OH ![]() RCOOH + H2O
RCOOH + H2O
Lưu ý: H2SO4 đặc trong phản ứng này ngoài vai trò là xúc tác của phản ứng còn làm nhiệm vụ hút nước.
- Vì phản ứng este hóa là phản ứng thuận nghịch nên các bài toán liên quan đến phản ứng này thường gắn với yếu tố hiệu suất phản ứng.
Ví dụ minh họa bài tập phản ứng Este hóa
Ví dụ 1: Thực hiện phản ứng este hóa 9,2g glixerol với 60g axit axetic. Giả sử chỉ thu được glixerol triaxetat có khối lượng 17,44g. Tính hiệu suất của phản ứng este hóa:
Giải
nglixerol = 0,1 mol
naxit axetic = 1 mol
![]()
Từ PT: meste = 0,1. 218 = 21,8g
Thực tế: meste = 17,44g
Hiệu suất: H% = 17,4421,8.100% =80%
Ví dụ 2: Hỗn hợp X gồm axit HCOOH và axit CH3COOH (tỉ lệ mol 1:1). Lấy 5,3 gam hỗn hợp X tác dụng với 5,75 gam C2H5OH (có xúc tác H2SO4 đặc) thu được m gam hỗn hợp este (hiệu suất của các phản ứng este hoá đều bằng 80%). Giá trị của m là:
A. 10,12
B. 6,48
C. 8,10
D. 16,20
Giải
Đáp án B
nHCOOH = ![]() = 0,05 mol
= 0,05 mol
![]() = 0,125mol ⇒ Ancol dư
= 0,125mol ⇒ Ancol dư
Vậy hỗn hợp este gồm:
![]() =
= ![]() = 0,05.80% = 0,04 mol
= 0,05.80% = 0,04 mol
⇒ m = 6,48 gam
Ví dụ 3: Đun nóng 6,0 gam CH3COOH với 6,0 gam C2H5OH (có H2SO4 làm xúc tác, hiệu suất phản ứng este hoá bằng 50%). Khối lượng este tạo thành là:
A.6,0 gam
B.4,4 gam
C.8,8 gam
D.5,2 gam
Giải
![]() = 0,1 mol
= 0,1 mol
![]() = 0,13 mol
= 0,13 mol
⇒![]() = 0,1.50% = 0,05 mol
= 0,1.50% = 0,05 mol
⇒![]() = 0,05.88 = 4,4g
= 0,05.88 = 4,4g
Bài tập phản ứng Este hóa
Câu 1. Khi đun nóng 25,8 gam hỗn hợp ancol etylic và axit axetic có H2SO4 đặc làm xúc tác thu được 14,08 gam este. Nếu đốt cháy hoàn toàn lượng hỗn hợp đó thu được 23,4 g H2O. Tìm thành phần trăm mỗi chất trong hỗn hợp đầu và hiệu suất của phản ứng este hoá.
A. 53,5% C2H5OH; 46,5% CH3COOH và H = 80%
B. 55,3% C2H5OH; 44,7% CH3COOH và H = 80%
C. 60,0% C2H5OH; 40,0% CH3COOH và H = 75%
D. 45,0% C2H5OH; 55,0% CH3COOH và H = 60%
![]() = 1,3 mol
= 1,3 mol
Đặt a, b là số mol C2H5OH và CH3COOH
⇒ 46a + 60b = 25,8 (1)
và ![]() = 3a + 2b = 1,3 (2)
= 3a + 2b = 1,3 (2)
Từ (1) và (2) ⇒ a = 0,3mol và b = 0,2 mol
![]() = 0,16 mol
= 0,16 mol
⇒ H = ![]() = 80%
= 80%
Câu 2. Đun nóng axit axetic với ancol isoamylic (CH3)2CH-CH2-CH2OH có H2SO4 đặc làm xúc tác thu được isoamyl axetat (dầu chuối). Tính lượng dầu chuối thu được từ 132,35g axit axetic đun nóng với 200g ancol isoamylic. Biết hiệu suất phản ứng đạt 68%
A. 97,5g
B. 195g
C. 292,5g
D. 159g
(CH3)2CH-CH2-CH2OH + CH3COOH ⇄ CH3COOCH2CH2CH(CH3)2 + H2O
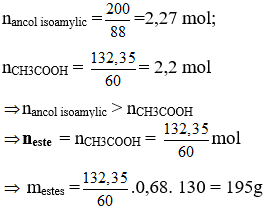
Câu 3. Cho 45 gam axit axetic phản ứng với 69 gam ancol etylic (xúc tác H2SO4 đặc), đun nóng, thu được 41,25 gam etyl axetat. Hiệu suất của phản ứng este hoá là:
A. 31,25%.
B. 40,00%.
C. 62,50%.
D. 50,00%.
![]() = 0,75 mol
= 0,75 mol
![]() = 1,5 mol
= 1,5 mol
![]() = 0,46875 mol
= 0,46875 mol
⇒ H = ![]() = 62,5%
= 62,5%
Câu 4. Chia a g axit axetic làm 2 phần bằng nhau.
Phần 1 được trung hòa vừa đủ bằng 0,5 lít dd NaOH 0,4M;
Phần 2 thực hiện phản ứng este hóa với ancol etylic thu được m g este. Giả sử hiệu suất phản ứng đạt 100%, giá trị của m là
A. 16,7.
B. 17,6.
C. 18,6.
D. 16,8.
Đáp án B
![]() = nNaOH = 0,5 . 0,4 = 0,02 mol
= nNaOH = 0,5 . 0,4 = 0,02 mol
CH3COOH + C2H5OH → CH3COOC2H5 + H2O
(H = 100%) ⇒ neste = ![]() = 0,02 mol ⇒ meste = 0,02 . 88 = 17,6g
= 0,02 mol ⇒ meste = 0,02 . 88 = 17,6g
Câu 5. Cho 0,1 mol Glixerol phản ứng với 0,15 mol axit axetic có H2SO4 đặc (H = 80%) thu được m gam este B. Giá trị m là:
A. 9,72.
B. 8,72.
C. 5,56.
D. 7,92.
Đáp án B
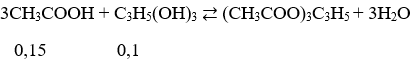
nax = 0,15 mol, nglixerol = 0,1 mol
⇒ neste = ![]() = 0,05 mol
= 0,05 mol
⇒ meste = 0,05 . 218. 80% = 8,72 g
- 30 bài tập Este trong đề thi Đại học
- 30 câu hỏi trắc nghiệm lý thuyết Este có đáp án
- Dạng bài tập cách gọi tên Este
- Dạng bài tập các phản ứng hóa học của Este
- Dạng bài tập cách nhận biết Este
- Dạng bài tập phản ứng đốt cháy Este
- Dạng bài tập phản ứng thủy phân Este
- Bài tập phản ứng thủy phân Este đa chức
Trên đây VnDoc đã giới thiệu tới các bạn Dạng bài tập phản ứng Este hóa. Để có kết quả cao hơn trong học tập, VnDoc xin giới thiệu tới các bạn học sinh tài liệu Giải bài tập Toán lớp 12, Giải bài tập Hóa học lớp 12, Giải bài tập Vật Lí 12, Tài liệu học tập lớp 12 mà VnDoc tổng hợp và đăng tải.



























