Đề thi thử THPT Quốc gia năm 2017 môn Hóa học trường THPT chuyên Hạ Long, Quảng Ninh (Lần 2) Có hướng dẫn giải chi tiết
Đề thi thử THPT Quốc gia năm 2017 môn Hóa học
Với mong muốn giúp các bạn học sinh làm quen, luyện tập cũng như hệ thống lại kiến thức, thử sức trực tiếp trên đề thi THPT thật sự, thư viện đề thi VnDoc đã sưu tầm và xin giới thiệu tới bạn: Đề thi thử THPT Quốc gia năm 2017 môn Hóa học trường THPT chuyên Hạ Long, Quảng Ninh (Lần 2) Có hướng dẫn giải chi tiết
Đề thi thử THPT Quốc gia năm 2017 môn Hóa học trường THPT chuyên Đại học Vinh (Lần 3)
| SỞ GD & ĐT QUẢNG NINH TRƯỜNG THPT CHUYÊN HẠ LONG | ĐỀ THI THỬ THPT QUỐC GIA LẦN 2 NĂM HỌC 2016 – 2017 Môn: HÓA HỌC Thời gian làm bài: 50 phút |
Câu 1: Cho thứ tự trong dãy điện hóa của một cặp oxi hóa-khử như sau Al3+/Al; Zn2+/Zn; Fe2+/Fe; Pb2+/Pb; Ag+/Ag. Phát biểu nào sau đây là đúng?
A. Nguyên tử Pb có thể khử Zn2+ trong dung dịch.
B. Nguyên tử Ag có thể khử Zn2+ trong dung dịch.
C. Nguyên tử Fe có thể khử Zn2+ trong dung dịch.
D. Nguyên tử Al có thể khử Zn2+ trong dung dịch.
Câu 2: 11,0 gam hỗn hợp A gồm Fe và Al phản ứng hết với dung dich HCl dư thu được 8,96 lít H2 (đktc). Cho 22 gam hỗn hợp A phản ứng hết với dung dịch HNO3 dư thu được V lít NO (đktc) là sản phẩm khử duy nhất. Giá trị V là:
A. 11,2 B. 6,72 C. 13,44 D. 8,96
Câu 3: Cho dãy các chất sau anđehit fomic, anđehit axetic, axit axetic, ancol etylic, glucozo, saccarozo, vinyl fomat. Số chất trong dãy khi đốt cháy hoàn toàn có số mol CO2 sinh ra bằng số mol O2 tham gia phản ứng là
A. 3 B. 4 C. 6 D. 5
Câu 4: Nung bột Fe2O3 với a gam bột Al trong khí trơ thu được 12,32 gam hỗn hợp rắn X. Cho toàn bộ X vào lượng dư dd NaOH, thu được 2,016 lít khí H2 (đktc). Biết các phản ứng đều xảy ra hoàn toàn. Giá trị của a là:
A. 2,56 B. 3,43 C. 4,32 D. 2,97
Câu 5: Khi đốt cháy hoàn toàn một chất hữu cơ X thu được hỗn hợp khí CO2 và hơi nước có tỉ lệ mol là 1 : 1. Trong mật ong có tới 40% chất X làm cho mật ong có vị ngọt sắc. X là chất nào trong các chất sau:
A. Saccarozo B. Glucozo C. Fructozo D. Axit oxalic
Câu 6: Xenlulozo trinitrat là chất dễ cháy và nổ mạnh được điều chế từ xenlulozo và axit nitric. Biết hiệu suất của phản ứng điều chế này là 88%. Thể tích axit nitric 99,67% (có khối lượng riêng 1,52 g/ml) cần dùng để sản xuất 59,4 kg xenlulozo trinitrat là
A. 28,35 lít B. 36,50 lít C. 27,72 lít D. 11,28 lít
Câu 7: Cho các chất sau FeCO3, Fe3O4, FeS, FeS2. Nếu hòa tan hoàn toàn cùng số mol mỗi chất trên vào dung dịch H2SO4 đặc, nóng (dư) thì số mol H2SO4 đã phản ứng lớn nhất ở phản ứng với
A. FeS2 B. Fe3O4 C. FeCO3 D. FeS
Câu 8: Trong số các chất dưới đây chất có nhiệt độ sôi thấp nhất là
A. CH3COOH B. C6H5NH2 C. HCOOCH3 D. C2H5OH
Câu 9: Trong các trường hợp dưới đây trường hợp không xảy ra phản ứng là
A. Ag + HCl đặc nóng B. Fe + CuCl2 C. Cu + AgNO3 D. Mg + AgNO3
Câu 10: Cấu hình electron của nguyên tử Cr (Z = 24) ở trạng thái cơ bản là
A. 1s22s22p63s23p63d54s1. B. 1s22s22p63s23p63d44s2.
C. 1s22s22p63s23p64s23d4. D. 1s22s22p63s23p63d6.
Câu 11: Công thức phân tử nào sau đây không thể của este.
A. C4H8O2 B. C4H10O2 C. C2H4O2 D. C4H6O2
Câu 12: Khi thủy phân hoàn toàn tripanmitin trong môi trường kiềm ta thu được sản phẩm là
A. C17H35COOH và glixerol B. C15H31COONa và glixerol
C. C15H31COOH và glixerol D. C17H35COONa và glixerol
Câu 13: Cho m gam hỗn hợp Ba và Al vào nước dư sau khi các phản ứng xảy ra hoàn toàn thu được 7,168 lít khí H2 (đktc) và 3,08 gam chất rắn không tan. Giá trị của m là
A. 14,32 B. 18,36 C. 15,28 D. 17,02
Câu 14: Thực hiện phản ứng lên men rượu từ 2,025 kg khoai chứa 80% tinh bột (còn lại là tạp chất trơ). Cho toàn bộ lượng CO2 hấp thụ hoàn toàn vào dung dịch Ca(OH)2 thu được 450 gam kết tủa, đun nóng dung dịch lại thu được 200 gam kết tủa nữa. Hiệu suất của phản ứng lên men là
A. 85,5% B. 42,5% C. 37,5% D. 30,3%
Câu 15: Cho m gam bột sắt vào dung dịch chứa 0,15 mol CuSO4 và 0,2 mol HCl. Sau khi các phản ứng xảy ra hoàn toàn, thu được 0,725m gam hỗn hợp kim loại. Giá trị của m là
A. 16,8 B. 11,2 C. 17,6 D. 16,0
Câu 16: Hòa tan Fe3O4 trong dung dịch HCl (vừa đủ) thu được dung dịch X. Khi cho các chất sau tác dụng với dung dịch X: Cu, Mg, Al, AgNO3, Na2CO3, NaNO3, NaOH, NH3, KI, H2S có bao nhiêu trường hợp phản ứng hóa học xảy ra không phải là phản ứng oxi hóa - khử
A. 6 B. 5 C. 4 D. 3
Câu 17: Cho các chất glucozo, saccarozo, tinh bột, glixerol và các phát biểu sau:
(a) Có 2 chất tác dụng được với dung dịch AgNO3/NH3, to.
(b) Có 2 chất có phản ứng thủy phân trong môi trường kiềm.
(c) Có 3 chất mà dung dịch của nó có thể hòa tan được Cu(OH)2.
(d) Cả 4 chất đều có nhóm –OH trong phân tử.
Số phát biểu đúng là:
A. 2 B. 1 C. 3 D. 4
Câu 18: Để phân biệt 3 dung dịch H2NCH(CH3)COOH, CH3COOH và C2H5NH2 chỉ cần dùng một thuốc thử là
A. natri kim loại B. dung dịch HCl C. dung dịch NaOH D. Quỳ tím
Câu 19: Cho 28,88 gam hỗn hợp gồm Al, Cu và Ag tác dụng vừa đủ với 1 lít dung dịch HNO3 1,45M thu được dung dịch chứa m gam muối và 5,6 lít hỗn hợp khí X (đktc) gồm NO và N2O. Tỷ khối của X so với H2 là 16,4. Giá trị của m là
A. 98,20 B. 97,20 C. 99,52 D. 98,75
Câu 20: Cho dãy các kim loại: Fe, Au, Al,Cu. Kim loại dẫn điện kém nhất là
A. Au B. Fe C. Cu D. Al
Câu 21: X là một amino axit no (phân tử chỉ có một nhóm –NH2 và một nhóm -COOH). Cho 0,06 mol X tác dụng với dung dịch chứa 0,1 mol HCl thu được dung dịch Y. Thêm 0,2 mol NaOH vào Y sau phản ứng đem cô cạn thu được 15,79 gam chất rắn khan. X là
A. valin B. lysin C. glyxin D. alanin
Câu 22: Có 5 kim loại là Mg, Ba, Zn, Fe, Ag. Chỉ dùng thêm dung dịch H2SO4 loãng thì có thể nhận biết được các kim loại
A. Mg, Ba, Zn, Fe B. Mg, Ba, Zn, Fe, Ag
C. Mg, Ba, Zn D. Mg, Ba, Cu
Câu 23: Chọn phát biểu sai trong các phát biểu sau:
A. Những kim loại có độ hoạt động trung bình như Mg, Fe, Sn,...thường được điều chế bằng phương pháp nhiệt luyện.
B. Nguyên tắc để điều chế kim loại là khử ion kim loại trong hợp chất thành nguyên tử.
C. Trong tự nhiên chỉ có một số ít kim loại như vàng, platin,... tồn tại ở trạng thái tự do.
D. Có thể điều chế các kim loại hoạt động trung bình hoặc yếu bằng cách điện phân dd muối của chúng.
Câu 24: Thực hiện các thí nghiệm sau:
(1) Thả một đinh Fe vào dung dịch HCl
(2) Thả một đinh Fe vào dung dịch Ni(NO3)2
(3) Thả một đinh Fe vào dung dịch FeCl3
(4) Nối một dây Fe với một dây Cu rồi để trong không khí ẩm
(5) Đốt một dây Fe trong bình kín chỉ chứa đầy khí O2
(6) Thả một đinh Fe vào dung dịch chứa Cu(SO4) và H2SO4 loãng.
Trong các thí nghiệm trên thì các thí nghiệm mà Fe bị ăn mòn điện hóa học là:
A. (2),(3),(4),(6) B. (2),(4),(6)
C. (1),(3),(5) D. (1),(3),(4),(5)
Câu 25: Nhóm các vật liệu nào dưới đây được chế tạo từ polime trùng ngưng
A. Nilon-6,6, tơ lapsan, tơ enang B. Nilon-6,6, tơ lapsan, tơ visco
C. Cao su Buna,nilon-6,6, tơ nitron D. Tơ axetat, nilon-6,6, nilon-7.
Câu 26: Tiến hành điện phân V lít dung dịch NaCl 1M và CuSO4 1,8M bằng điện cực trơ tới khi nước bắt đầu điện phân ở cả hai cực thì dừng điện phân, thấy khối lượng dung dịch giảm m gam. Dung dịch sau phản ứng hòa tan tối đa 8,84 gam Al2O3. Giá trị của m là:
A. 34,5 B. 34,8 C. 34,6 D. 34,3
Câu 27: Chất nào sau đây là polime có cấu trúc mạch phân nhánh:
A. Amilozo B. Xenlulozo C. Saccarozo D. Amilopectin
Câu 28: Cho các phương trình phản ứng hóa học sau (các phản ứng đều ở điều kiện và xúc tác thích hợp):
X + 2NaOH → X1 + X2 + H2O
X2 + CuO → X3 + Cu + H2O
X3 + 4AgNO3 + 6NH3 + H2O → (NH4)2CO3 + 4Ag + NH4NO3
X1 + 2NaOH → X4 + 2Na2CO3
2X4 → X5 + 3H2
Phát biểu nào sau đây là sai
A. X có 8 nguyên tử H trong phân tử.
B. X2 rất độc không được sử dụng để pha vào đồ uống.
C. X1 tan trong nước tốt hơn so với X.
D. X5 có phản ứng tạo kết tủa với AgNO3/NH3
Câu 29: Để làm mềm một mẫu nước cứng chứa x mol Mg2+, y mol Ca2+ và 0,06 mol HCO3- người ta phải dùng một thể tích vừa đủ dung dịch nào dưới đây:
A. 30ml dung dịch Na2CO3 2M. B. 30ml dung dịch HCl 2M.
C. 20ml dung dịch Na3PO4 1M D. 30ml dung dịch NaCl 1M.
Câu 30: Nhận định nào sau đây không đúng?
A. Khi thay nhóm OH ở nhóm cacboxyl của axit cacboxylic bằng nhóm OR thì được este.
B. Lipit là những hợp chất hữa cơ có trong tế bào sống tan nhiều trong nước và không tan trong dung môi hữu cơ không phân cực.
C. Phản ứng thủy phân este trong môi trường kiềm là phản ứng một chiều và gọi là phản ứng xà phòng hóa.
D. Tên của este RCOOR gồm tên gốc R cộng thêm tên gốc axit RCOO (đuôi "at").
Câu 31: Phần trăm khối lượng của nguyên tố oxi trong lysin là
A. 35,96% B. 43,54% C. 27,35% D. 21,92%
Câu 32: Thủy phân m gam tinh bột trong môi trường axit (giả sử sự thủy phân chỉ tạo glucozo). Sau phản ứng, đem trung hòa axit bằng kiềm rồi thực hiện phản ứng tráng bạc thu được m gam Ag. Hiệu suất của phản ứng thủy phân tinh bột là:
A. 66,67% B. 80% C. 75% D. 50%
Câu 33: Khi nhúng thanh Mg có khối lượng m gam vào dung dịch hỗn hợp X chứa a mol Cu(NO3)2 và b mol HCl, ta có đồ thị biểu diễn sự phụ thuộc của khối lượng thanh Mg vào thời gian phản ứng được biểu diễn như hình vẽ dưới đây.
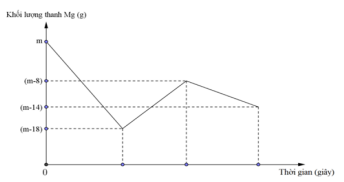
Sau khi phản ứng xảy ra hoàn toàn rút thanh Mg ra, thu được NO là sản phẩm khử duy nhất của N+5 tỉ lệ a : b là
A. 1:10 B. 1:6 C. 1:12 D. 1:8
Câu 34: Phát biểu nào sau đây là đúng:
A. Cu có thể tan được trong dung dịch FeSO4.
B. Ở nhiệt độ thường, sắt không khử được nước.
C. Trong công nghiệp nhôm được sản xuất từ quặng đolomit.
D. K3PO4 không có khả năng làm mất tính cứng vĩnh cửu của nước.
Câu 35: Khi tiến hành đồng trùng hợp buta-1,3-đien với stiren, xúc tác Na thu được một loại cao su buna-S. Cứ 42 gam cao su buna-S phản ứng hết với 32 gam Br2 trong CCl4. Tỉ lệ mắt xích buta-1,3-dien và stiren trong cao su buna-S là
A. 1:2 B. 3:5 C. 1:3 D. 2:3
Câu 36: Hỗn hợp X gồm 3 peptit mạch hở A,B,C (mỗi peptit được cấu tạo từ một loại α-aminoaxit, tổng số nhóm –CO-NH- trong 3 phân tử A,B,C là 9) với tỉ lệ số mol nA : nB : nC = 2 : 1 : 3. Biết số liên kết peptit trong mỗi phân tử A,B,C đều lớn hơn 1. Khi thủy phân hoàn toàn m gam X thu được 33,75 gam glyxin, 106,8 gam alanin và 263,25 gam valin. Giá trị của m là:
A. 394,8 B. 384,9 C. 348,9 D. 349,8
Câu 37: X, Y là hai axit no, đơn chức đồng đẳng liên tiếp, Z là ancol 2 chức, T là este thuần chức tạo bởi X, Y, Z. Đốt cháy 0,1 mol hỗn hợp E chứa X, Y, Z, T cần dùng 0,47 mol khí O2 thu được lượng CO2 nhiều hơn H2O là 10,84 gam. Mặt khác 0,1 mol E tác dụng vừa đủ với 0,11 mol NaOH thu được dung dịch G và một ancol có tỉ khối so với H2 là 31. Cô cạn G rồi nung nói với xút có mặt CaO thu được m gam hỗn hợp khí. Giá trị của m gần nhất với
A. 3,5 B. 4,5 C. 2,5 D. 5,5
Câu 38: Hòa tan hoàn toàn hỗn hợp gồm FeS2 và Fe3O4 bằng 100 gam dung dịch HNO3 a % vừa đủ thu được 15,344 lít hỗn hợp khí gồm NO và NO2 có khối lượng 31,35 gam và dung dịch chỉ chứa 30,15 gam hỗn hợp muối. Giá trị của a gần nhất với
A. 57 B. 63 C. 43 D. 46
Câu 39: Hỗn hợp E chưa peptit X mạch hở (tạo bởi gly và ala) và este (thuần chức) mạch hở (tạo bởi etylenglicol và một axit đơn chức, không no chứa một liên kết C=C). Đun nóng m gam hỗn hợp E với dung dịch NaOH vừa đủ thu được 25,32 gam hỗn hợp muối F. Lấy toàn bộ F đem đốt cháy thu được Na2CO3, N2, 30,8 gam CO2, 10,44 gam H2O. Biết số mắt xích của X nhỏ hơn 8. Giá trị của m gần nhất với giá trị nào sau đây.
A. 18 B. 21 C. 19 D. 20
Câu 40: Cho 9,9 gam hỗn hợp Al, Mg tác dụng vừa đủ với dung dịch chứa 1,8 mol HNO3 tạo ra sản phẩm khử X duy nhất. Làm bay hơi dung dịch sau phản ứng thu được m gam muối khan. Giá trị của m là:
A. 78,64 gam B. 65,7 gam C. 87,69 gam D. 56,24 gam.
Đáp án đề thi thử THPT Quốc gia năm 2017 môn Hóa học
1-D | 2-C | 3-D | 4-C | 5-C | 6-A | 7-A | 8-C | 9-A | 10-A |
11-B | 12-B | 13-B | 14-B | 15-D | 16-D | 17-A | 18-D | 19-C | 20-B |
21-A | 22-B | 23-D | 24-B | 25-A | 26-D | 27-D | 28-A | 29-C | 30-B |
31-D | 32-C | 33-A | 34-B | 35-D | 36-D | 37-C | 38-A | 39-B | 40-B |
LỜI GIẢI CHI TIẾT
Câu 1: Đáp án D
Dựa vào dãy điện hóa, kim loại đứng trước (từ Al) có thể đẩy kim loại đứng sau ra khỏi muối của nó
Câu 2: Đáp án C
Phương pháp: bảo toàn e.
Lời giải:
Xét 11g A : Bảo toàn e : ne = 2nH2 = 0,8 mol = 2nFe + 3nAl
Và mFe + mAl = 11g
=> nFe = 0,1; nAl = 0,2 mol
=> 22g A có: nFe = 0,2 mol; nAl = 0,4 mol
Bảo toàn e: 3nFe + 3nAl = 3nNO => nNO = 0,6 mol
=> VNO = 13,44 lit
Câu 3: Đáp án D
TQ: CxHyOz + (x + 0,25y – 0,5z)O2 -> xCO2 + 0,5yH2O
Để nCO2 = nO2 => x + 0,25y – 0,5z = x
=> y = 2z
Các chất thỏa mãn: andehit fomic (CH2O); axit axetic (C2H4O2); glucozo (C6H12O6); saccarozo (C12H22O11); vinyl fomat (C3H4O2)
Câu 4: Đáp án C
X + NaOH => Al dư, Fe2O3 hết (do các phản ứng xảy ra hoàn toàn)
Fe2O3 + 2Al -> 2Fe + Al2O3
x -> 2x
Al + NaOH + H2O -> NaAlO2 + 1,5H2
=> nAl dư = 0,06 mol
Bảo toàn khối lượng: mX = mFe2O3 + mAl pứ + mAl dư
=> 12,32 = 160x + 27.2x + 27.0,06 => x = 0,05 mol
=> a = 27.(0,05.2 + 0,06) = 4,32g
Tài liệu vẫn còn, mời các bạn tải về









