Đề thi tốt nghiệp THPT 2020 môn Hóa Trường Chuyên Gia Định, Hồ Chí Minh



Đề thi tốt nghiệp THPT 2020 môn Hóa Trường Chuyên Gia Định, Hồ Chí Minh được VnDoc.com là đề thi thử THPT Quốc gia phát triển dựa trên nội dung cấu trúc đề minh họa của Bộ GD&ĐT đưa ra trước đó, mong muốn giúp các em ôn tập, củng cố kiến thức, các trường Sở đã liên tục đưa ra các đề thi thử.
Đề thi thử THPT Quốc gia 2020 môn Hóa
Để tải Đề thi thử THPT 2020 môn Hóa vui lòng kéo xuống ấn link tải về
Đề chuẩn bị cho kì thì quan trọng sắp diễn ra vào 10/8/2020 VnDoc đã tổng hợp biên soạn các để thi thử THPT 2020 môn Hóa học các trường, Sở trên cả nước để giúp các bạn có tài liệu ôn tập cũng như luyện đề. Chuẩn bị tốt cho kì thi THPT Quốc gia sắp tới.
Mời các bạn tham khảo nội dung Đề thi thử Hóa THPT 2020 chi tiết dưới đây
1. Đáp án Đề thi tốt nghiệp THPT 2020 môn Hóa Chuyên Gia Định, Hồ Chí Minh
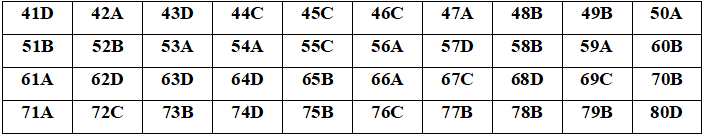
2. Hướng dẫn giải Đề thi tốt nghiệp THPT 2020 môn Hóa Chuyên Gia Định, Hồ Chí Minh
Câu 41: Kim loại nào sau đây không tác dụng với dung dịch Fe2(SO4)3?
A. Cu.
B. Fe.
C. Mg.
D. Ag.
Hướng dẫn giải

Câu 45: Chất nào sau đây có thể được dùng để làm mềm nước có tính cứng tạm thời?
A. MgCl2.
B. Ca(NO3)2.
C. Ca(OH)2.
D. MgCO3.
Hướng dẫn giải
 (M là Mg; Ca)
(M là Mg; Ca)
Câu 46: Hoà tan hoàn toàn m gam hỗn hợp gồm Fe và FeCO3 trong lượng dư dung dịch HCl được 4,48 lít hỗn hợp hai khí (ở đktc) có tỉ khối so với H2 bằng 11,5. Giá trị của m là
A. 11,2.
B. 8,6.
C. 17,2.
D. 13,4.
Hướng dẫn giải
Khí gồm H2 (0,1) và CO2 (0,1) ![]()
Câu 51: Có các nhận xét sau:
(a) Các kim loại Na và Ba đều là kim loại nhẹ.
(b) Độ cứng của Cr lớn hơn độ cứng của Al.
(c) Cho K vào dung dịch CuSO4 thu được Cu.
(d) Độ dẫn điện của các kim loại giảm dần theo thứ tự Ag, Cu, Al.
(e) Có thể điều chế Mg bằng cách cho khí CO khử MgO ở nhiệt độ cao.
Trong các nhận xét trên, số nhận xét đúng là
A. 4.
B. 3.
C. 5.
D. 2.
Hướng dẫn giải
(a); (b) đúng
(c) sai: K khử H2O trước
(d) đúng
(e) sai: CO không khử được MgO
Câu 53: Hấp thụ hết 0,3 mol khí CO2 vào 500ml dung dịch chứa Na2CO3 0,2M và NaOH 1M. Sau khi các phản ứng xảy ra hoàn toàn, số mol Na2CO3 thu được là
A. 0,30.
B. 0,10.
C. 0,20.
D. 0,25.
Hướng dẫn giải
![]()
=> Tạo 2 muối Na2CO3 (0,3) và NaHCO3 (0,1)
Câu 54: Phản ứng nào chứng minh hợp chất Fe(III) có tính oxi hóa?
A. Fe2O3 + 3CO → 2Fe + 3CO2.
B. FeCl3 + 3AgNO3 → Fe(NO3)3 + 3AgCl.
C. Fe2O3 + 6HNO3 → 2Fe(NO3)3 + 3H2O.
D. 2Fe(OH)3 → Fe2O3 + 3H2O.
Hướng dẫn giải
Chứng minh Fe(III) có tính oxi hóa thì phản ứng phải tạo thành Fe có số oxi hóa thấp hơn +3
Câu 56: Cho m gam hỗn hợp gồm Fe và Cu (tỉ lệ mol 1:1) tác dụng hết với lượng dư dung dịch Cu(NO3)2, thu được 12,8 gam Cu. Giá trị của m là
A. 12,0.
B. 5,6.
C. 18,0.
D. 7,8.
Hướng dẫn giải
nFe = nCu = x => Sau phản ứng nCu = 2x = 0,2 => x = 0,1 => m = 12 gam
Câu 58: Thuỷ phân este C2H5OOCCH3 trong NaOH dư, thu được muối có công thức là
A. C2H5COONa.
B. CH3COONa.
C. HCOONa.
D. C3H7COONa.
Hướng dẫn giải
![]()
Câu 59: Ở điều kiện thường, kim loại Al không phản ứng với chất hoặc dung dịch nào sau đây?
A. CuO.
B. HCl.
C. NaOH.
D. CuSO4
Hướng dẫn giải

Câu 65: Cho 6,6 gam Gly-Gly phản ứng với 200 ml dung dịch NaOH 1M. Cô cạn dung dịch sau phản ứng, thu được m gam chất rắn khan. Giá trị của m là
A. 9,7.
B. 13,7.
C. 10,6.
D. 14,6.
Hướng dẫn giải
![]()
BTKL: mGly-Gly + mNaOH = mrắn => mrắn = 13,7 gam
.........................
(Hướng dẫn giải được VnDoc cập nhật TRONG FILE TẢI VỀ, vui lòng Theo dõi bài viết/ Tải tài liệu để nhận đầy đủ nội dung và đáp án Đề thi tốt nghiệp THPT 2020 môn Hóa Trường Chuyên Gia Định, Hồ Chí Minh)
Mời các bạn tham khảo thêm một số đề thi thử mới nhất 2020:
- Đề thi thử THPT Quốc gia 2020 môn Hóa Trường chuyên Vĩnh Phúc lần 3
- Đề thi thử tốt nghiệp THPT năm 2020 môn Hóa Sở GD&ĐT Bắc Kạn
Trên đây VnDoc đã gửi Đề thi tốt nghiệp THPT 2020 môn Hóa Trường Chuyên Gia Định, Hồ Chí Minh tới bạn đọc tham khảo. Nhìn chung đề thi này không quá khó để các bạn được điểm 8, chỉ cần lưu ý ở các bài tập đếm, một phần dễ mất điểm đáng tiếc.
Các bạn có thể các em cùng tham khảo thêm một số đề thi thử các môn tại: Thi thpt Quốc gia môn Toán, Thi THPT Quốc gia môn Vật Lý, Thi thpt Quốc gia môn Sinh, Thi thpt Quốc gia môn Tiếng Anh....
Ngoài ra, VnDoc.com đã thành lập group chia sẻ tài liệu ôn tập THPT Quốc gia miễn phí trên Facebook: Quyết tâm đỗ Đại Học Mời các bạn học sinh tham gia nhóm, để có thể nhận được những tài liệu, đề thi mới nhất.



