Giải bài tập Hóa học 11 SBT bài 31
Giải bài tập Hóa học 11 SBT bài Luyện tập: Anken và Ankadien
VnDoc xin giới thiệu tới các bạn học sinh Giải bài tập Hóa học 11 SBT bài 31. Tài liệu được giải chi tiết sẽ giúp các bạn giải Hóa 11 hiệu quả hơn. Mời các bạn tham khảo chi tiết bài viết dưới đây nhé.
- Giải bài tập Hóa học 11 SBT bài 30
- Giải bài tập Hóa học 11 SBT bài 29
- Giải bài tập Hóa học 11 SBT bài 27
Giải bài tập Hóa học 11 SBT bài 31 Luyện tập: Anken và Ankadien vừa được VnDoc.com sưu tập và xin gửi tới bạn đọc cùng tham khảo. Bài viết được tổng hợp gồm có lời giải của 4 bài tập trong sách bài tập môn Hóa học lớp 11 bài Luyện tập: Anken và Ankadien. Qua bài viết bạn đọc có thể thấy được công thức cấu tạo của một số tên chất, cách xác định công thức phân tử và phần trăm về khối lượng trong hỗn hợp... Mời các bạn cùng tham khảo chi tiết và tải về tại đây nhé.
Bài tập trắc nghiệm 6.20, 6.21 trang 45 sách bài tập (SBT) hóa học 11
6.20. Ghép tên chất với công thức cấu tạo cho đúng.
Tên chất | Công thức cấu tạo | ||
1 | 4-etyl-2-metylhexan | A | |
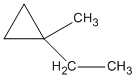
2 | 1,1-etylmetylxiclopropan | B | |
3 | 3,3-dimetylbut-1-en | C | |
4 | divinyl | D | |
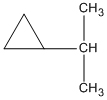
5 | isopropylxiclopropan | E | |
6 | isopren | G |
|
7 | 2,2,4,4-tetrametylpentan | H |
|
8 | 2,3-dimetylbut-2-en | I | |
6.21. Hợp chất CM2 - CH - CH - CH = CH2 có tên là gì?
A. 2-etyl-3-metylpent-4-en.
B. 4-etyl-3-metylpen-1-en.
C. 3,4-đimetyl-hex-5-en.
D. 3,4-đimetyl-hex-1-en.
Hướng dẫn trả lời:
6.20.
7-A ; 1-B ; 8-C ; 3-D ; 6-E ; 2-G ; 5-H ; 4-I
6.21. D
Bài tập trắc nghiệm 6.22, 6.23 trang 45 sách bài tập (SBT) hóa học 11
6.22. Hợp chất 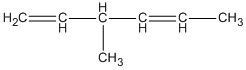 có tên là gì?
có tên là gì?
A. 3-metylhex-1,2-đien.
B. 4-metylhex-1,5-đien.
C. 3-metylhex-l,4-đien.
D. 3-metylhex-1,3-đien.
6.23. Trong các chất dưới đây, chất nào là ankađien liên hợp?
A. CH2 = CH - CH2 - CH = CH2
B. 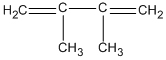
C. CH2 = CH - CH2 - CH = CH - CH3
D. CH2 = C = CH2
Hướng dẫn trả lời:
6.22. C
6.23. B
Bài tập 6.24 trang 45 sách bài tập (SBT) hóa học 11
6.24. Hỗn hợp khí A chứa nitơ và hai hiđrocacbon kế tiếp nhau trong một dãy đồng đẳng. Khối lượng hỗn hợp A là 18,3 g và thể tích của nó là 11,2 lít. Trộn A với một lượng dư oxi rồi đốt cháy, thu được 11,7 gam H2O và 21,28 lít CO2. Các thể tích đo ở đktc.
Hãy xác định công thức phân tử và phần trăm về khối lượng của từng hiđrocacbon trong hỗn hợp A.
Hướng dẫn trả lời:
Số mol ![]()
Khối lượng C trong A là: 0,95.12 = 11,4 (g).
Số mol ![]()
Khối lượng H trong A là: 0,65.2 = 1,3 (g).
Tổng khối lượng của C và H chính là tổng khối lượng 2 hiđrocacbon. Vậy, khối lượng N2 trong hỗn hợp A là: 18,30 - (11,4 + 1,3) = 5,6 (g)
Số mol ![]()
Số mol 2 hidrocacbon ![]()
Đặt lượng CxHy là a mol, lượng Cx+1Hy+2 là b mol:
a + b = 0,2 (1)
Số mol C = số mol CO2, do đó:
xa + (x + 1)b = 0,95 (2)
Số mol H = 2.số mol H2O, do đó:
ya + (y+ 2)b = 2.0,65= 1,3
Từ (2) ta có x(a + b) + b = 0,95 ⇒ b = 0,95 - 0,3x
Vì 0 < b < 0,3, nên 0 < 0,95 - 0,3x < 0,3
Từ đó tìm được 2,16 < x < 3,16 ⇒ x = 3.
⇒ (b = 0,95 - 3.0,3 = 10-2 ⇒ a = 0,3 - 0,05 = 0,25
Thay giá trị tìm được của a và b vào (3), ta có y = 4.
% về khối lượng của C3H4 trong hỗn hợp A: ![]() . 100% = 54,6%
. 100% = 54,6%
% về khối lượng của C4H6 trong hỗn hợp A: ![]() . 100% = 14,7%
. 100% = 14,7%
Để có kết quả học tập lớp 11 tốt hơn. VnDoc Mời các bạn tham khảo thêm các bài viết dưới đây của chúng tôi:
- Giải bài tập Hóa học 11 SBT bài 30
- Trắc nghiệm Hóa học lớp 11 bài 31: Luyện tập Anken và Ankađien
- Giải bài tập trang 137, 138 SGK Hóa học lớp 11: Luyện tập Anken và ankađien
----------------------------------
Trên đây VnDoc đã giới thiệu tới bạn đọc Giải bài tập Hóa học 11 SBT bài 31 Luyện tập: Anken và Ankadien. Để có kết quả cao hơn trong học tập, VnDoc xin giới thiệu tới các bạn học sinh tài liệu Giải bài tập Sinh học 11, Giải bài tập Vật lý 11, Giải bài tập Hóa học 11, Giải bài tập Toán 11 mà VnDoc tổng hợp và đăng tải.
Mời bạn đọc cùng tham gia nhóm Tài liệu học tập lớp 11 để có thêm tài liệu học tập nhé