Giải Sách bài tập Hóa học 9 bài 11
Giải Sách bài tập Hóa học 9 bài 11: Phân bón hóa học
Giải Sách bài tập Hóa học 9 bài 11: Phân bón hóa học được VnDoc sưu tầm và đăng tải, tổng hợp các câu hỏi trong sách bài tập nằm trong chương trình giảng dạy môn Hóa học 9. Hi vọng rằng đây sẽ là những tài liệu hữu ích trong công tác giảng dạy và học tập của quý thầy cô và các bạn học sinh. Mời quý thầy cô cùng các bạn tham khảo tài liệu dưới đây
Bài 11.1 trang 14 Sách bài tập Hóa học 9: Ba nguyên tố cơ bản là chất dinh dưỡng cho thực vật, đó là: nitơ (N), photpho (P), kali (K).
Hợp chất của nitơ làm tăng trưởng lá cây và tinh bột trong ngũ cốc. Hợp chất của photpho kích thích bộ rễ phát triển và hoa quả chín sớm.
Hợp chất của kali tăng cường sức chịu đựng cho thực vật.
Dưới đây là hàm lượng của N, P, K có trong 4 mẫu phân bón kép NPK:
| MẦU PHÂN BÓN | %N | %P | %K |
| 1 | 10 | 10 | 20 |
| 2 | 6 | 15 | 15 |
| 3 | 14 | 6 | 20 |
| 4 | 8 | 12 | 8 |
Dùng số liệu của bảng, hãy:
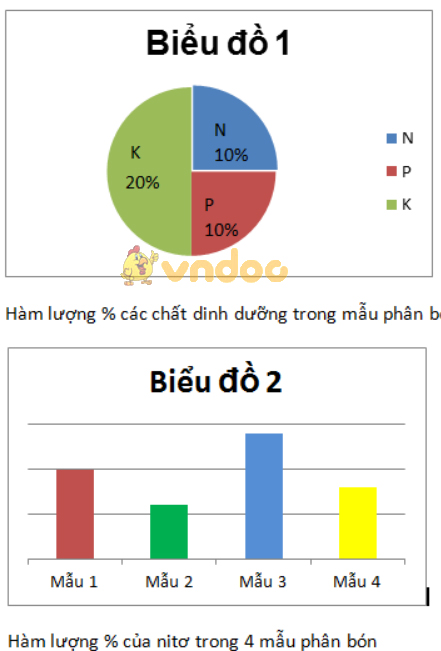
a) Vẽ biểu đồ biểu thị chất dinh dưỡng trong mẫu phân bón 1.
b) Vẽ biểu đồ so sánh hàm lượne của nitơ có trong 4 loại phân bón.
c) Giới thiệu mẫu phân bón cho ngô, khoai để có hàm lượng nitơ bằng hàm lượng photpho và có hàm lượng kali cao.
Lời giải:
a) Xem biểu đồ 1.
b) Xem biểu đồ 2.
c) Mẫu phân bón số 1.
Bài 11.2 trang 14 Sách bài tập Hóa học 9: Có ba mẫu phân bón hoá học không ghi nhãn là: phân kali KCl, phân đạm NH4NO3 và phân lân Ca(H2PO4)2. Hãy nhận biết mỗi mẫu phân bón trên bằng phương pháp hoá học và viết các phương trình hoá học.
Lời giải:
Lấy một lượng nhỏ mỗi mẫu phân bón vào ống nghiệm. Thêm 4 - 5 ml nước, khuấy kĩ và lọc lấy nước lọc.
Lấy 1 ml nước lọc của từng loại phân bón vào ống nghiệm. Nhỏ vào mỗi ống vài giọt dung dịch Na2CO3, nếu có kết tủa trắng thì phân bón hoá học đó là Ca(H2PO4)2:
Na2CO3 + Ca(H2PO4)2 → CaCO3 + 2NaH2PO4
- Lấy 1 ml nước lọc của hai loại phân bón còn lại, thử bằng dung dịch AgNO3, nếu có kết tủa trắng thì phân bón đó là KCl:
KCl + AgNO3 → AgCl + KNO3
- Nước lọc nào không có phản ứng hoá học với hai thuốc thử trên là NH4NO3.
Ghi chú: Ngoài ra còn có những phương pháp hoá học khác.
Bài 11.3 trang 14 Sách bài tập Hóa học 9: Trong công nghiệp, người ta điều chế phân đạm urê bằng cách cho khí amoniac NH3 tác dụng với khí cacbon đioxit CO2:
2NH3 + CO2 → CO(NH2)2 + H2O
Để có thê sản xuất được 6 tấn urê, cần phải dùng
a) Bao nhiêu tấn NH3 và CO2?
b) bao nhiêu m3 khí NH3 và CO2(đktc)?
Lời giải:
2NH3 + CO2 → CO(NH2)2 + H2O
![]() = 6x2.17/60 = 3,4 (tấn)
= 6x2.17/60 = 3,4 (tấn)
![]() = 6,44/60 = 4,4 tấn
= 6,44/60 = 4,4 tấn
2NH3 + CO2 → CO(NH2)2 + H2O
nure = m/M = 6000000/60 = 100000 mol
![]() = 100000x2/1 = 200000
= 100000x2/1 = 200000
![]() = n.22,4 = 200000x22,4= 4480000 = 4480 (m3)
= n.22,4 = 200000x22,4= 4480000 = 4480 (m3)
![]() = 100000 mol
= 100000 mol
![]() = 100000 x 22,4 = 2240000l = 2240 (m3)
= 100000 x 22,4 = 2240000l = 2240 (m3)
Bài 11.4 trang 15 Sách bài tập Hóa học 9: Điều chế phân đạm amoni nitrat NH4NO3 bằng phản ứng của canxi nitrat Ca(NO3)2 với amoni cacbonat (NH4)2CO3.
a) Viết phương trình hoá học.
b) Phản ứng này thuộc loại phản ứng nào? Vì sao phản ứng này có thể xảy ra được?
c) Cần phải dùng bao nhiêu tấn canxi nitrat và amoni cacbonat đế sản xuất được 8 tấn phân đạm amoni nitrat?
Lời giải:
a) Phương trình hoá học:
Ca(NO3)2 + (NH4)2CO3 → CaCO3 + 2NH4NO3
b) Phản ứng này thuộc loại phản ứng trao đổi giữa hai dung dịch muối. Phản ứng xảy ra được vì tạo thành chất kết tủa là CaCO3.
c) Tính khối lượng các chất tham gia:
Để sản xuất được 80 x 2 = 160 (tấn) NH4NO3 cần 96 tấn (NH4)2CO3 và 164 tấn Ca(NO3)2. Để sản xuất được 8 tấn NH4NO3 cần:
96x8/160 = 4,8 tấn (NH4)2CO3
Và 168x8/160 = 8,2 tấn Cu(NO3)2
Bài 11.5 trang 15 Sách bài tập Hóa học 9: Cho 6,8 kg NH3 tác dụng với dung dịch H3PO4 thấy tạo ra 36,2 kg hỗn hợp hai muối NH4H2PO4 và (NH4)2HPO4 theo phương trình hoá học:
2NH3 + H3PO4 → (NH4)2HPO4
NH3 + H3PO4 → (NH4)2HPO4
a) Hãy tính khối lượng axit H3PO4 đã tham gia phản ứng
b) Tính khối lượng mỗi muối được tạo thành.
Lời giải:
a) Theo định luật bảo toàn khối lượng, ta có:
![]() = mmuoi
= mmuoi
Vậy ![]() = 36,2 - 6,8 = 29,4g
= 36,2 - 6,8 = 29,4g
b) Gọi khối lượng muối (NH4)2HPO4 là x kg => ![]() p/u là 34x/132kg
p/u là 34x/132kg
NH4H2PO4 là y kg → mNH3 p/u là 17y/115kg
Ta có:
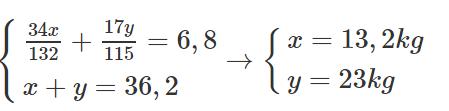
Mời các bạn tham khảo tài liệu sau: Hóa học lớp 9, Giải bài tập Hóa học 9, Tài liệu học tập lớp 9, Đề thi giữa kì 1 lớp 9, Đề thi học kì 1 lớp 9