Sơ lược phương pháp giải Toán hỗn hợp chất khử tác dụng với H+ và No3-
Hóa học lớp 8
1
s¬ lîc ph¬ng ph¸p gi¶i to¸n
HçN HîP chÊt khö t¸c dông víi h
+
,NO
3
-
I- KIẾN THỨC CẦN NHỚ.
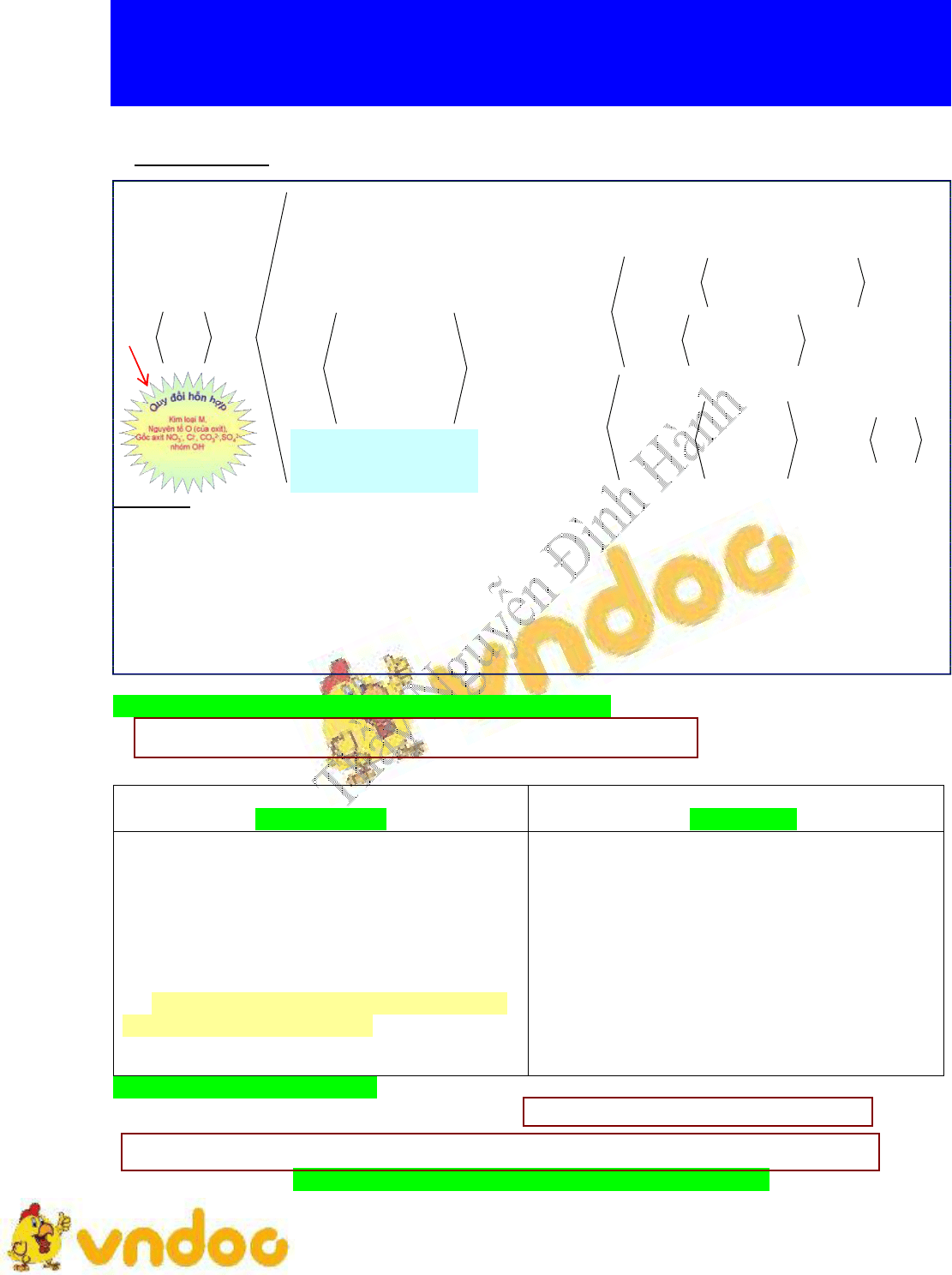
1. Sơ đồ bài toán (thường gặp nhất)
2 2 2 2
E 3
E 1 E 8 E 10 E 2
3
1
E 8
3
NaOH
Kh NO , NO, N O, N , H
d.
H
(X)
Cation
NO
ddY , H
E
NO
+ 2
2 2
2
+
4
2
4
tèi ®a (I)
Ý Z ( )
Na , AlO , ZnO ,
dÞch Y
Gèc
kim lo¹i
N
sè E nhËn ®Ó t¹o 1mol spk
H
, SO ,Cl
3
AgNO
3
Kim
K NH
OH
NO
Caction
AgCl
d.
Ag
1
0
3 4
3
d (II)
axit trong Y
lo¹i k tan
Õt tña
(thêng cho khÝ nµy)...
KL
dÞch Y NH KÕt tña
NO
Trong đó:
X là hỗn hợp chứa chất khử:
Kim loại: Mg, Al, Cu, Fe ...
Các hợp chất chứa nguyên tố có mức oxi hóa chưa cao: FeS
2
, FeO, Fe
3
O
4
, Fe(OH)
2
, muối Fe
2+
,
muối sunfua ...
Một số chất khác (không bị oxi hóa bởi HNO
3
): CuO, MgO, Al
2
O
3
, Fe
2
O
3
, Fe(NO
3
)
3
...
Nguồn cung cấp H
+
: HNO
3
, HCl, H
2
SO
4
loãng, HSO
4
-
Nguồn cung cấp NO
3
-
: HNO
3
, muối nitrat (chứa gốc NO
3
-
)
2. Trao đổi electron trong phản ứng.
2.1. Cách tính E
1mol
của chất khử hoặc sản phẩm khử (SPK)
E
1mol
= (OXH cao – OXH thấp) chỉ số nguyên tử tham gia trao đổi E.
Ví dụ:
Các chất khử
(Nhường electron)
Các sản phẩm khử
(Sản phẩm nhận electron của N
+5
)
Kim loại M
0
M
x+
M
E (x 0) 1 x
Fe
2+
Fe
3+
2
Fe
E (3 2) 1 1
Fe
3
O
4
Fe
3+
3 4
Fe O
E (3 8 : 3) 3 1
0 6
2
4
S
O E 6 0 6
S S
Fe
0
Fe
3+
Fe
E 3 0 3
* Khi dư H
+
và NO
3
-
thì Fe và các chất khử của
Fe đều chuyển thành muối Fe
3+
.
2
2
4
2
2
4
2 NO
2
NO
5 1
3 2 N O
3
4
NH
0
N
0
H
2
2
N O E (5 4) 1
N O E (5 2) 3
H N O N O E (5 1).2 8
N H E 5 ( 3) 8
N E (5 0).2 10
H ( E (1 0).2 2
+
[ ]
H
2.2- Bảo toàn số mol Electron:
Vì số mol E nhường = Số mol E nhận nên ta có n
chất khử
E
(của chất khử)
= n
SPK
E
(của SPK)
ơ
2
3 4 2 2 2 4 2
M Fe O NO H NO N O NH N
Fe
n hóa n 1 n 1 .... 1n 2n 3n 8n 8n 10n
trÞ +
(*)
(Vắng chất nào thì bỏ ra, có thêm chất nào thì cộng vào công thức trên (*))
Khi X có đơn ch
ất KL
:
Mg,
Al,Zn thì SPK thường có
NH
4
+

2
3. Phương pháp giải toán.
a) Sử dụng các định luật bảo toàn:
Bảo toàn eletron: n
E
(nhường) = n
E
(nhận)
2 2 2 4 2
2 2 2 4 2
1 2 NO H NO N O NH N
Ag
KL NO H NO N O NH N
Ag
n E n E .... 1n 2n 3n 8n 8n 10n n
1n 2n 3n 8n 8n 10n n
chÊt khö 1 chÊt khö 2
trong hçn hîp gèc, nhãm trong hçn hîp
+ +
HoÆc: n hãa trÞ n hãa trÞ +
Bảo toàn nguyên tố:
Số mol nguyên tố A (trước phản ứng) = Số mol nguyên tố A (sau phản ứng)
(Số mol nguyên tố A được tính theo công thức: n
A
= n
chất
chỉ số của A )
Bảo toàn điện tích trong cùng dung dịch Y
1
, Y
2
, Y
3
:
Tổng số mol điện tích dương = tổng số mol điện tích âm
Số mol điện tích = số mol ion điện tích ion
Bảo toàn khối lượng
m
các chất phản ứng
= m
các chất sản phẩm
Hoặc: m
các chất trước phản ứng
= m
các chất sau phản ứng
m
hỗn hợp
= m
các thành phần tạo nên hỗn hợp
m
hợp chất
= m
các thành phần tạo nên chất
.
b) Sử dụng quy đổi
Quy đổi hỗn hợp chứa chất khử thành: KL, O, OH, gốc axit ...
Quy đổi Fe và các oxit sắt thành Fe, O hoặc Fe, Fe
2
O
3
Quy đổi sản phẩm khử thành oxi, giả thiết đốt X:
2 3 2 5 2 2
X E oxit CO SO N O Cl H O
m 8n m n m m m
KL
m
(CO
2
, SO
3
, N
2
O
5
, Cl
2
, H
2
O là sản phẩm tương ứng khi trong hỗn hợp có CO
3
, SO
4
, NO
3
, Cl, OH)
c) Một số chú ý:
Công thức liên hệ giữa số mol H
+
và các sản phẩm khử (cái gì không có thì bỏ ra khỏi công thức)
( O 2 H NO NO N O N
2 2 2 2
H CO NH
3 4
n 2n 2n 2n 2n 4n 10n 10n 12n
ph¶n øng)
Khi sản phẩm khử có H
2
thì trong dung dịch sau phản ứng đó không còn gốc NO
3
-
.
Các ion H
+
, NO
3
-
, Fe
2+
không đồng thời tồn tại trong dung dịch.
Khi cho kim loại (Cu, Fe, Mg...) vào Y
1
nếu giải phóng spk của N
+5
thì Y
1
không có muối Fe
2+
.
Khi cho NaOH tối đa vào dung dịch Y
1
chứa (H
+
, NH
4
+
, Al
3+
, Na
+
, cation của kim loại không tan trong
nước, các gốc axit):
3
NaO
(trong
H
Na
3
Al
Na NaOH hòa tan Al(OH)
n n – n n
OH NaOH trao các catio
*
n Na*
)
)
1
Y )
gèc axit
cña trao ®æi ®iÖn tÝch víi c¸c gèc axit vµ kÕt tña
hãa trÞ gèc
cña ®æi ®iÖn tÝch víi cã s½n tro(trõ ng
3
4
2
NaOH OH( trong KT)
Al NH
2
axit
AlO
Na
trong dd
n n 4n n
Dung : Na trong Na , axit, AlO
n n hóa n
) ( ), ( )*
1
2 1
gèc 1
Y )
dÞch cuèi cïng (Y ) chØ chøa Y gèc
trÞ gèc
cña
(trong Y + tro
k
ng ki
iÒm
Òm)
Khi cho AgNO
3
dư vào dung dịch Y
1
nếu có sinh sản phẩm khử của N
+5
(thường là NO) thì chứng tỏ
trong Y
1
có H
+
.
3Fe
2+
+ 4H
+
+ NO
3
-
3Fe
3+
+ 2H
2
O + NO
Fe
2+
+ Ag
+
Fe
3+
+ Ag
Cl
-
+ Ag
+
AgCl
2
BTE
NO Ag
Fe
BTKL
KT AgCl Cl
Ag
Ag
BTĐT
NO
Ag
BTKL
n 3n n
m 108n 143,5n 108n 35,5n
n n n
m m
(II)
(II)
®iÖn tÝch kim lo¹i 3
c¶ QT
c¸c chÊt ph¶n øng 2 giai ®o¹n c¸c khÝ tho¸t ra 2 g
(trong Y )=
2
H O KT
m m m
3
iai ®o¹n muèi NO dung dÞch cuèi
Cả QT
3
II- BÀI TẬP VẬN DỤNG
Ví dụ 1: Hỗn hợp E gồm Fe, FeO, Fe
3
O
4
, Fe
2
O
3
, Fe(OH)
2
(trong đó Fe(OH)
2
chiếm 8,35% khối lượng). Hòa
tan hết 21,56 gam E trong dung dịch chứa 0,2 mol HNO
3
và 0,96 mol HCl, thu được 0,15 mol khí X và dung
dịch Y. Cho Cu vào dung dịch Y thấy có m gam Cu phản ứng và thoát ra 0,448 lít khí X (đktc). Biết NO là sản
phẩm khử duy nhất của quá trình, các phản ứng xảy ra hoàn toàn. Giá trị của m là
A. 9,60. B. 10,24. C. 11,84. D. 6,72.
(Nguồn đề: Sưu tầm, không rõ tác giả)
Hướng dẫn giải:
BTKL
BT
2
Fe OH
Fe
2
0,96 0,03 m m
n 0,02 mol n – (0,495 – )
2 64 64
Quy
m
21,56 m 0,17.3.8 1,25m (0,495 – ).72
64
§T dung dÞch cuèi
(mol)
®æi NO thµnh oxi, gi¶ sö cho Cu vµo hçn hîp ®Çu råi ®em ®èt
=
0,02.18 m 11,84 gam
Ví dụ 2: Để m gam hỗn hợp E gồm Al, Fe và Cu trong không khí sau một thời gian, thu được 34,4 gam hỗn hợp X
gồm các kim loại và oxit của chúng. Cho 6,72 lít CO qua X nung nóng, thu được hỗn hợp rắn Y và hỗn hợp khí Z có
tỉ khối so với H
2
là 18. Hòa tan hoàn toàn Y trong dung dịch chứa 1,7 mol HNO
3
, thu được dung dịch chỉ chứa
117,46 gam muối và 4,48 lít hỗn hợp khí T gồm NO và N
2
O. Tỉ khối của T so với H
2
là 16,75. Các thể tích khí đều
đo ở điều kiện tiêu chuẩn. Giá trị của m là
A. 27. B. 31. C. 32. D. 28.
(Nguồn đề: sưu tầm trên facebook)
Hướng dẫn giải:
2
2 2
BTKL
Y
NO N O
BTKL
H O H O
m 34, 4 0,3.28 – 0,3.36 32 gam
n 0,15 mol ; 0, 05 mol
32 1,7.63 117, 46 0, 2.33,5 18n n 0,83
32 – m 1,7 – 0,83.2
2 0, 05.10 0,15.4 10. 1, 7 m 28
16 4
(1)
(2)
+
Sè m ol H
n
m ol
(ga
m)
Ví dụ 3: Hòa tan hết 23,18 gam hỗn hợp X gồm Fe, Mg và Fe(NO
3
)
3
vào dung dịch chứa 0,92 mol HCl và 0,01 mol
NaNO
3
, thu được dung dịch Y (chất tan chỉ có 46,95 gam hỗn hợp muối) và 2,92 gam hỗn hợp Z gồm ba khí không
màu (trong đó hai khí có số mol bằng nhau). Dung dịch Y phản ứng được tối đa với 0,91 mol KOH, thu được 29,18
gam kết tủa. Biết các phản ứng xảy ra hoàn toàn. Phần trăm thể tích của khí có phân tử khối lớn nhất trong 2 là
A. 75,34% B. 51,37% C. 58,82% D. 45,45%.
(Đề thi THPT QG 2019, Mã 217)
Hướng dẫn giải:
2 2
H O H O
KOH 3
Cl Na
3
BTKL 23,18 0,92.36,5 0,01.85 46,95 2,92 18m n 0,43 mol
n 0,92 n – n 0,92 mol Y không có anion NO
m 62a 23,18
KL: m(gam)
m 18b 46,95 – 0,01.23 – 0,92.35,5
NO :a(mol)
m 17.(0
NH +
4
=
§Æt X ; n = b (mol)
2
N N
2
O
1
m 13,88
a 0,15
,91– b) 29,18 b 0,01
H :0,01
BT Z n 0,15 0,01 0,01 0,15 Z NO: 0,05 %n
N :0,05
n 0,16.3 0,43 0,05 0,15 / 2
H
2
cÆp khÝ ®ång mol
n = (0,92 0,43.2 0,01.4):2 = 0,01
mol H,N,O
O
45,(45)%
Ví dụ 4: Hòa tan hoàn toàn 22,4 gam hỗn hợp X gồm Fe, Cu, CuO, Fe
3
O
4
FeO (trong đó oxi chiếm 12,142% khối
lượng) trong HNO
3
loãng dư, thu được dung dịch Y và 6,72 lít (đktc) hỗn hợp khí Z gồm NO, NO
2
có tỉ khối so với
He là
61
6
. Cho dung dịch NaOH dư vào dung dịch Y, thu được m (gam) kết tủa. Giá trị của m gần nhất với
A. 33,5. B. 34,0 . C.34,5. D.45,0.
(Thầy Nguyễn Đình Hành – THCS&THPT Y Đôn, Gia Lai)
Sơ lược phương pháp giải Toán hỗn hợp chất khử tác dụng với H+ và No3- lớp 8
Sơ lược phương pháp giải Toán hỗn hợp chất khử tác dụng với H+ và No3- được VnDoc sưu tầm và đăng tải. Đây là tài liệu hay dành cho quý thầy cô cùng các bạn học sinh ôn tập, chuẩn bị tốt bài giảng trước khi đến lớp. Mời các quý thầy cô cùng các bạn học sinh tham khảo
- Phản ứng hóa học của Mangan (Mn) và Hợp chất của Mangan - Cân bằng phương trình hóa học
- Phản ứng hóa học của Vàng (Au) và Hợp chất của Vàng - Cân bằng phương trình hóa học
- Phản ứng hóa học của Crom (Cr) và Hợp chất của Crom - Cân bằng phương trình hóa học
............................................
Ngoài Sơ lược phương pháp giải Toán hỗn hợp chất khử tác dụng với H+ và No3-. Mời các bạn học sinh còn có thể tham khảo các đề thi học kì 1 lớp 8, đề thi học kì 2 lớp 8 các môn Toán, Văn, Anh, Lý, Địa, Sinh mà chúng tôi đã sưu tầm và chọn lọc. Với tài liệu lớp 8 sẽ giúp các bạn ôn tập tốt hơn. Chúc các bạn học tập tốt









