Đề thi thử THPT Quốc Gia môn Hóa chuyên ĐH Vinh lần 4 năm 2015 (Có lời giải chi tiết)
Đề thi thử đại học môn Hóa (Có lời giải chi tiết)
Nhằm mục tiêu giúp các bạn học sinh lớp 12 có tài liệu ôn tập và rèn luyện cho kì thi THPT Quốc gia, VnDoc xin giới thiệu tới bạn đọc Đề thi thử THPT Quốc Gia môn Hóa chuyên ĐH Vinh lần 4 năm 2015 (Có lời giải chi tiết). Hi vọng đây là một tài liệu hữu ích cho các bạn trong quá trình ôn tập. Chúc các bạn thi tốt!
Mời các bạn tham khảo thêm bài test: Đề thi thử THPT Quốc gia môn Hóa năm 2016 Trường THPT Chuyên Đại học Vinh (Lần 3)
- ĐỀ THI GỒM 50 CÂU (TỪ CÂU 1 ĐẾN CÂU 50) DÀNH CHO TẤT CẢ CÁC THÍ SINHCho biết nguyên tử khối của các nguyên tố: H = 1; C = 12; N = 14; O = 16; Na = 23; Mg = 24; Al = 27; P = 31; S = 32; Cl = 35,5; K = 39; Ca = 40; Fe = 56; Cu = 64; Zn = 65; Br = 80; Ag = 108; Ba = 137.
- Câu 1:Polime nào sau đây được dùng để chế tạo thủy tinh hữu cơ plexiglas?
- Câu 2:Thủy phân hoàn toàn m gam hỗn hợp M gồm tetrapeptit X và pentapeptit Y (đều mạch hở) bằng dung dịch KOH vừa đủ, rồi cô cạn cẩn thận thì thu được (m + 11,42) gam hỗn hợp muối khan của Val và Ala. Đốt cháy hoàn toàn muối sinh ra bằng một lượng oxi vừa đủ thu được K2CO3; 2,464 lít N2 (đktc) và 50,96 gam hỗn hợp gồm CO2 và H2O. Phần trăm khối lượng của Y trong hỗn hợp M có thể là:
- Câu 3:Đốt cháy hoàn toàn 0,25 mol hỗn hợp X gồm ba ancol, cần dùng vừa đủ V lít O2 thu được H2O và 12,32 lít CO2. Mặt khác, cho 0,5 mol X trên tác dụng hết với Na, sau khi các phản ứng xảy ra hoàn toàn thu được 12,32 lít H2. Các thể tích khí đều đo ở đktc. Giá trị của V gần nhất với:+ Thí nghiệm 2: 0,5mol X-----------> H2: 12,55 : 22,4 = 0,55 mol => nOH trong X = 2nH2 = 1,1mol
+ Thí nghiệm 1: Dùng 0,25 mol X => nOH trong X = 1,1 : 2 = 0,55mol và nCO2 = 0,55mol
=> X luôn có số C = số nhóm –OH.
Vậy hỗn hợp X phải gồm các ancol no (k = 0) => nX = nH2O - nCO2 => nH2O = 0,25 + 0,55 = 0,8 mol
Áp dụng bảo toàn nguyên tố O, ta có: nO2 = (2nCO2 + nH2O - nO trong X)/2 = 0,675mol
=> VO2 = 0,675 . 22,4 = 15,12 lit ---------> 15,11 lít - Câu 4:Phát biểu nào sau đây là sai?Chọn A. Lưu ý: Al, Fe và Cr bị thụ động trong HNO3 đặc, nguội và H2SO4 đặc, nguội.
- Câu 5:Cho dãy các chất sau: C2H2, C6H5OH (phenol), C2H5OH, HCOOH, CH3CHO, CH3COCH3, C2H4. Khẳng định nào sau đây là đúng khi nói về các chất trong dãy trên?A. Đúng. 2 chất tráng bạc gồm : HCOOH; CH3CHO. Lưu ý: C2H2 phản ứng với AgNO3/NH3 là phản ứng thế ion kim loại không phải phản ứng tráng bạc.
B. Sai vì chỉ có 2 chất phản ứng NaOH : C6H5OH và HCOOH.
C. Sai vì có 5 chất làm mất màu nươc brom gồm: C2H2, C6H5OH (phenol), HCOOH, CH3CHO, C2H4
D. Sai vì có chỉ có 4 chất có khả năng phản ứng với H2 (Ni, to): C2H2, CH3CHO, CH3COCH3, C2H4 - Câu 6:Thực hiện các thí nghiệm sau:
(1) Nung hỗn hợp gồm Fe và NaNO3 trong khí trơ.
(2) Cho luồng khí H2 đi qua bột CuO nung nóng.
(3) Đốt dây Al trong bình kín chứa đầy khí CO2.
(4) Nhúng dây Ag vào dung dịch HNO3 loãng.
(5) Nung hỗn hợp bột gồm CuO và Al trong khí trơ.
Số thí nghiệm có thể xảy ra phản ứng oxi hóa kim loại là:Chọn B. Lưu ý: phản ứng oxi hóa kim loại nên phải có mặt kim loại đơn chất => loại (2). Các thí nghiệm còn lại đều thỏa mãn. Nhiều bạn sẽ lúng túng ở thí nghiệm (1) cho rằng Fe không phản ứng với NaNO3, nhưng lưu ý ở thí nghiệm (1) nung NaNO3 sẽ sinh O2, sau đó O2 sẽ oxi hóa Fe.
- Câu 7:Hỗn hợp M gồm axit cacboxylic X, ancol Y (đều đơn chức) và este Z được tạo ra từ X và Y (trong M, oxi chiếm 43,795% về khối lượng). Cho 10,96 gam M tác dụng vừa đủ với 40 gam dung dịch NaOH 10%, tạo ra 9,4 gam muối. Công thức của X và Y lần lượt là:
- Câu 8:Phát biểu nào sau đây là sai?A. Đúng. Vì mantozơ cho phản ứng tráng bạc (kết tủa Ag), còn saccarozơ thì không phản ứng.
B. Đúng. Vì glucozơ và mantozơ (mở vòng) đều mang nhóm –CHO nên đều bị khử bởi H2 (Ni, to).
C. Sai. Vì saccarozơ không mang nhóm –CHO
D. Đúng. Vì fructozơ trong phân tử chứa nhóm –CO– nên không làm mất màu nước brom. - Câu 9:
Hỗn hợp M gồm CH3CH2OH, CH2=CHCH2OH, CH3COOH, CH2=CHCOOH, HCOOCH3.
Đốt cháy hoàn toàn m gam M cần dùng vừa đủ 0,4 mol O2, thu được 0,35 mol CO2 và 0,35 mol H2O. Mặt khác, cho m gam M trên tác dụng vừa đủ với 50 gam dung dịch Ba(OH)2 nồng độ x%. Giá trị của X là: - Câu 10:Nhiệt phân Fe(NO3)2 trong môi trường khí trơ. Sau khi các phản ứng xảy ra hoàn toàn, thu được sản phẩm gồm:Nhiệt phân muối hoặc hiđroxit của sắt đến khối lượng không đổi thì thu được Fe2O3.
- Câu 11:Hòa tan hoàn toàn 9,75 gam Zn trong lượng dư dung dịch HNO3 đặc, nóng. Sau khi phản ứng xảy ra hoàn toàn thu được dung dịch X và V lít NO2 (sản phẩm khử duy nhất, đktc). Giá trị của V là:2nZn = 2nNO2 <=> VnNO2 = (2. 9,75 . 22,4)/65 = 6,72 lít.
- Câu 12:Cho phản ứng hóa học:
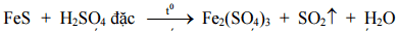
Sau khi cân bằng phản ứng hoá học trên với hệ số của các chất là những số nguyên dương, tối giản thì tổng hệ số của H2SO4 và FeS là: - Câu 13:Etyl axetat không tác dụng với:Etyl axetat: CH3COOC2H5 (este no) không phải ứng với H2 (Ni, to).
- Câu 14:Cho hình vẽ mô tả thí nghiệm điều chế khí Y từ chất rắn X như sau:
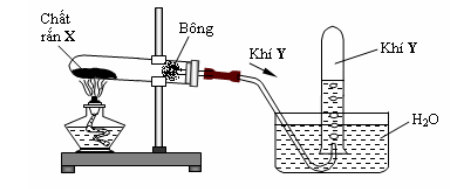
Hình vẽ trên minh họa cho phản ứng nào sau đây?+ Từ hình vẽ => loại D (vì mô hình điều chế khí từ quá trình nung chất rắn).
+ Loại B và C do NH3, HCl và SO2 tan tốt trong H2O (mô hình thu khí dẫn qua H2O) nên không thu được khí. - Câu 15:X, Y, Z là ba axit cacboxylic đơn chức cùng dãy đồng đẳng (MX < MY < MZ ), T là este tạo bởi X, Y, Z với một ancol no, ba chức, mạch hở E. Đốt cháy hoàn toàn 26,6 gam hỗn hợp M gồm X, Y, Z, T (trong đó Y và Z có cùng số mol) bằng lượng vừa đủ khí O2 , thu được 22,4 lít CO2 (đktc) và 16,2 gam H2O. Mặt khác, đun nóng 26,6 gam M với lượng dư dung dịch AgNO3/NH3. Sau khi các phản ứng xảy ra hoàn toàn, thu được 21,6 gam Ag. Mặt khác, cho 13,3 gam M phản ứng hết với 400 ml dung dịch NaOH 1M và đun nóng, thu được dịch N. Cô cạn dung dịch N thu được m gam chất rắn khan. Giá trị của m gần nhất với:
- Câu 16:Hợp chất nào sau đây là loại hợp chất hữu cơ tạp chức?
- Câu 17:Chất nào sau đây không tác dụng với dung dịch NaOH?
- Câu 18:Hỗn hợp X gồm axit oxalic, axit axetic, axit acrylic và axit malonic (HOOCCH2COOH). Cho 0,25 mol X phản ứng hết với lượng dư dung dịch NaHCO3, thu được 0,4 mol CO2. Đốt cháy hoàn toàn 0,25 mol X trên cần dùng vừa đủ 0,4 mol O2, thu được CO2 và 7,2 gam H2O. Phần trăm khối lượng của axit oxalic trong X là:
- Câu 19:Phát biểu nào sau đây là đúng?A. Sai vì vinyl axetat CH3COOCH=CH2 làm mất màu dung dịch brom
B. Sai. Lưu ý: các este không tạo được liên kết hiđro giữa các phân tử este với nhau nhưng vẫn tạo được liên kết hiđro giữa các phân tử este với phân tử H2O nhưng rất kém.
C. Sai vì chất giặt rửa có khả năng làm giảm sức căng bề mặt của chất bẩn trên vải, da…do đó vết bẩn được phân tán thành nhiều phần nhỏ hơn rồi được phân tán vào nước và bị rửa trôi đi; không phải do phản ứng hóa học.
D. Đúng. Theo SGK 12 cơ bản – trang 8 - Câu 20:Ở trạng thái cơ bản, cấu hình electron lớp ngoài cùng của nguyên tử nguyên tố X là 3s2 3p1 . Vị trí (chu kì, nhóm) của X trong bảng tuần hoàn các nguyên tố hóa học là:
- Câu 21:Hấp thụ hoàn toàn 11,2 lít CO2 (đktc) vào dung dịch chứa x mol Ca(OH)2; y mol NaOH và x mol KOH. Sau khi các phản ứng xảy ra hoàn toàn, thu được dung dịch chứa 32,3 gam muối (không có kiềm dư) và 15 gam kết tủa. Bỏ qua sự thủy phân của các ion, tỉ lệ x : y có thể là:Đặt:
Ca2+: x mol
Na+: y mol
K+ : x mol
OH- : (3x + y)mol
Áp dụng bảo toàn điện tích và khối lượng muối, ta có:
2(x - 0,15) + y + x = 0,35 mol
40(x - 0,15) + 23y + 39x + 0,35.61 = 32,3 gam
=> x = 0,2 mol
y = 0,05 mol
=> x : y = 4 : 1 - Câu 22:Cho cân bằng hóa học sau (xảy ra trong bình kín dung tích không đổi):
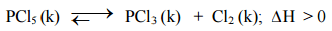
Trong các yếu tố: (1) tăng nhiệt độ của hệ phản ứng; (2) thêm một lượng khí Cl2; (3) thêm một lượng khí PCl5; (4) tăng áp suất chung của hệ phản ứng; (5) dùng chất xúc tác. Những yếu tố nào đều làm cân bằng chuyển dịch theo chiều thuận (giữ nguyên các yếu tố khác)?ΔH > 0 => phản ứng thuận là phản ứng thu nhiệt.
(1) tăng nhiệt độ cân bằng chuyển dịch theo chiều của phản ứng thu nhiệt, nghĩa là chiều thuận.
(2) thêm một lượng khí Cl2 cân bằng chuyển dịch thoe chiềm giảm nồng độ Cl2 nghĩa là chiều nghịch.
(3) thêm một lượng khí PCl5 cân bằng chuyển dịch theo chiều giảm nồng đọ PCl5, nghĩa là chiều thuận.
(4) tăng áp suất chung của hệ cân bằng chuyển dịch theo chiều làm giảm số mol khí, nghĩa là chiều nghịch.
(5) chất xúc tác không làm ảnh hưởng đến chuyển dịch cân bằng. - Câu 23:Một học sinh nghiên cứu dung dịch X và thu được kết quả như sau: Dung dịch X tác dụng được với dung dịch Ba(OH)2, sinh ra kết tủa trắng. Khi cho dung dịch X tác dụng với dung dịch HCl, sinh ra khí không làm mất màu dung dịch KMnO4. Dung dịch X tác dụng với dung dịch natri panmitat, sinh ra kết tủa. Vậy dung dịch X là dung dịch nào sau đây?+ X tác dụng với HCl sinh khí không làm mất màu dung dịch KMnO4 => loại A, C (vì sinh SO2 làm mất màu dung dịch KMnO4.
+ X phản ứng với natri pammitat sinh được kết tủa => loại B. (các muối của kim loại kiềm đều tan). - Câu 24:Phát biểu nào sau đây là sai?Lưu ý: Các muối amoni đều tan
- Câu 25:Cho phản ứng hóa học: Br2 + 5Cl2 + 6H2O --------> 2HBrO3 + 10HCl
Câu nào sau đây diễn tả đúng tính chất của các chất phản ứng? - Câu 26:Chất nào sau đây không có phản ứng tráng bạc?
- Câu 27:Phát biểu nào sau đây là đúng?
- Câu 28:Cho 2,13 gam P2O5 tác dụng với 80 ml dung dịch NaOH 1M. Sau khi các phản ứng xảy ra hoàn toàn, thu được dung dịch X chứa m gam muối. Bỏ qua sự thủy phân của các ion, giá trị của m là:Từ tỉ lệ số mol trên => sinh 2 muối nNaOH = nH2O = 0,08 mol
Áp dụng bảo toàn khối lượng, ta có: mmuối = 0,03.98 (H3POO4)+ 0,08.40 (KOH) - 0,08.18 (H2O) = 4,7 gam. - Câu 29:Ở dạng lỏng, phenol và ancol benzylic đều phản ứng với:
- Câu 30:Phát biểu nào sau đây là sai?Sai vì Gly-Ala-Gly chỉ chứa 2 liên kết peptit.
- Câu 31:Tiến hành các thí nghiệm sau:
(1) Cho lá hợp kim Fe - Cu vào dung dịch H2SO4 loãng.
(2) Cho lá Cu vào dung dịch AgNO3.
(3) Cho lá Zn vào dung dịch HNO3 loãng.
(4) Đốt dây Mg trong bình đựng khí Cl2.
Số thí nghiệm có xảy ra ăn mòn hóa học là:Cả 4 thí nghiệm đều xảy ra ăn mòn hóa học. - Câu 32:Cho các phát biểu sau:
(1) Khi đốt cháy hoàn toàn một ancol X bất kì, nếu thu được số mol CO2 nhỏ hơn số mol H2O thì X là ancol no, đơn chức, mạch hở.
(2) Tơ nilon – 6,6 và tơ visco đều là tơ tổng hợp.
(3) CH3COOH và H2NCH2CH2NH2 có khối lượng phân tử bằng nhau nên là các chất đồng phân với nhau.
(4) Các chất: CHCl=CHCl, CH3CH=CHCH2OH, CH3CH=CHCOOH đều có đồng phân hình học.
Những phát biểu sai là:(1) Sai vì đốt cháy ancol thu được mol CO2 < mol H2O thì chỉ kết luận được ancol no, mạch hở.
(2) Sai vì tơ axetat là tơ bán tổng hợp (tơ nhân tạo)
(3) Sai vì thành phần nguyên tố khác nhau.
(4) Đúng. Các chất đều thỏa mãn điều kiện có đồng phân hình học. - Câu 33:Phát biểu nào sau đây là sai?Dễ thấy A Sai vì Be và Mg không tác dụng với H2O ở nhiệt độ thường.
- Câu 34:Cho m gam bột Fe vào 100 ml dung dịch CuSO4 1M. Sau khi phản ứng xảy ra hoàn toàn, thu được dung dịch X và 9,2 gam chất rắn Y. Giá trị của m là:nCu2+ = 0,1 mol => 0,164 + mFe dư = 9,2 gam => mFe dư = 2,8 gam
mFe phản ứng = 0,1. 56 = 5,6 gam
=> mFe = 2,8 + 5,6 = 8,4 gam - Câu 35:Hỗn hợp M gồm C2H5NH2, CH2=CHCH2NH2, H2NCH2CH2CH2NH2, CH3CH2CH2NH2 và CH3CH2NHCH3. Đốt cháy hoàn toàn 5,6 lít M, cần dùng vừa đủ 25,76 lít O2, chỉ thu được CO2; 18 gam H2O và 3,36 lít N2. Các thể tích khí đều đo ở điều kiện tiêu chuẩn. Phần trăm khối lượng của C2H5NH2 trong M là:Đề lần này có vẻ “kết” cái gu cho hỗn hợp nhiều chất. Nhiều bạn sẽ hoảng khi thấy hỗn hợp nhiều chất nhưng thật ra “bình tĩnh” lại cái bạn sẽ thấy trong hỗn hợp M chỉ có C2H5NH2 (a mol) có 2C; các chất còn lại đều có 3C (b mol).
Áp dụng bảo toàn nguyên tố O, ta có: nCO2 = (2,3 - 1)/2 = 0,65 mol
Theo bảo toàn khối lượng: mM = 12nCO2 + 2nH2O + 14nN = 12.0,65 + 2.1 + 14.0,15.2 = 14 gam
Theo giả thuyết và bảo toàn nguyên tố C, ta có:
a + b = 0,25 mol
2a + 3b = nCO2 = 0,65 mol
=> a = 0,1 mol
b = 0,15 mol
Vậy %mC2H5NH2 = 100% . (0,1 . 45)/14 = 32,14% - Câu 36:Hòa tan hoàn toàn m gam hỗn hợp X gồm K, K2O, KOH, KHCO3, K2CO3 trong lượng vừa đủ dung dịch HCl 14,6%, thu được 6,72 lít (đktc) hỗn hợp gồm hai khí có tỉ khối so với H2 là 15 và dung dịch Y có nồng độ 25,0841%. Cô cạn dung dịch Y, thu được 59,6 gam muối khan. Giá trị của m là:
- Câu 37:Cho 38,55 gam hỗn hợp X gồm Mg, Al, ZnO và Fe(NO3)2 tan hoàn toàn trong dung dịch chứa 0,725 mol H2SO4 loãng. Sau khi các phản ứng xảy ra hoàn toàn, thu được dung dịch Y chỉ chứa 96,55 gam muối sunfat trung hòa và 3,92 lít (đktc) khí Z gồm hai khí trong đó có một khí hóa nâu ngoài không khí. Biết tỉ khối của Z so với H2 là 9. Phần trăm số mol của Mg trong hỗn hợp X gần nhất với giá trị nào sau đây?
- Câu 38:Cho 300 ml dung dịch Ba(OH)2 1M vào 200 ml dung dịch chứa AlCl3 0,75M và HCl 0,5M. Sau khi các phản ứng xảy ra hoàn toàn, thu được m gam kết tủa. Giá trị của m là:OH- : 0,6 mol
Al3+: 0,15 mol
H+ : 0,1 mol
1 < nOH- /nAl3+ = (0,6 - 0,1)/0,15 = 1,67 < 3
Al(OH)3 : a mol
[Al(OH)4]- : b mol
Áp dụng bảo toàn nguyên tố Al và gốc –OH, ta có:
a + b = nAl3+ = 0,15 mol
3a + 4b = nOH- = 0,5 mol
=> a = 0,1 mol
b = 0,05 mol
=> m↓ = 7,8 gam - Câu 39:Phương trình hóa học nào sau đây là sai?
- Câu 40:Cho sơ đồ phản ứng sau:
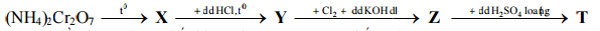
Trong đó X, Y, Z, T đều là các hợp chất khác nhau của crom. Chất T là: - Câu 41:Cho 20,8 gam hỗn hợp M gồm hai chất hữu cơ, tác dụng vừa đủ với dung dịch NaOH, thu được dung dịch N gồm hai muối R1COONa, R2COONa và m gam R'OH (R2 = R1 + 28; R1, R2, R' đều là các gốc hiđrocacbon). Cô cạn N rồi đốt cháy hết toàn bộ lượng chất rắn, thu được H2O; 15,9 gam Na2CO3 và 7,84 lít CO2 (đktc). Biết tỉ khối hơi của R'OH so với H2 nhỏ hơn 30; công thức của hai chất hữu cơ trong M là:
- Câu 42:Nhỏ rất từ từ dung dịch HCl vào dung dịch chứa a mol KOH, b mol NaOH và c mol K2CO3, kết quả thí nghiệm được biểu diễn trên đồ thị sau:
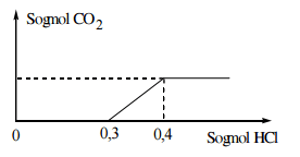
Tổng (a + b) có giá trị là: - Câu 43:Hòa tan hoàn toàn m gam MSO4 (M là kim loại) vào nước thu được dung dịch X. Điện phân dung dịch X (điện cực trơ, hiệu suất 100%) với cường độ dòng điện 7,5A không đổi, trong khoảng thời gian 1 giờ 4 phút 20 giây, thu được dung dịch Y và khối lượng catot tăng a gam. Dung dịch Y tác dụng vừa đủ với 200 ml dung dịch chứa KOH 1M và NaOH 1M, sinh ra 4,9 gam kết tủa. Coi toàn bộ lượng kim loại sinh ra đều bám hết vào catot. Giá trị của m và a lần lượt là:
- Câu 44:Chất nào sau đây không phản ứng với dung dịch CuSO4?
- Câu 45:Có 3 dung dịch: Na2SO3, NaNO3, NH4NO3 đựng riêng biệt trong 3 ống nghiệm mất nhãn. Thuốc thử duy nhất cần dùng để nhận biết 3 ống nghiệm trên bằng phương pháp hóa học là:Dùng Ba(OH)2: Ống tạo kết tủa là Na2SO3(BaSO3), ống tạo khí có mùi khai là NH4NO3 (NH3), còn lại NaNO3
- Câu 46:Cho các phát biểu sau:
(1) Khí SO2 gây ra hiện tượng hiệu ứng nhà kính.
(2) Khí CO2 gây ra hiện tượng mưa axit
(3) Các dạng nhiên liệu như than, dầu mỏ và khí tự nhiên được gọi là nhiên liệu hóa thạch. (4) Khi được thải ra khí quyển, freon (chủ yếu là CFCl3 và CF2Cl2) phá hủy tầng ozon.
(5) Các nguồn năng lượng: thủy điện, gió, mặt trời đều là những nguồn năng lượng sạch. Những phát biểu đúng là:(1) sai vì CO2 là thù phạm gây hiệu ứng nhà kính. (2) sai vì SO2 mới gây ra mưa axit. - Câu 47:Cho m gam hỗn hợp bột X gồm FexOy, CuO và Cu (x, y nguyên dương) vào 600 ml dung dịch HCl 1M, thu được dung dịch Y (không chứa HCl) và còn lại 6,4 gam kim loại không tan. Cho Y tác dụng với lượng dư dung dịch AgNO3, thu được 102,3 gam kết tủa. Biết các phản ứng đều xảy ra hoàn toàn. Giá trị của m gần nhất với giá trị nào sau đây?
- Câu 48:Nung nóng hỗn hợp X gồm ba hiđrocacbon có các công thức tổng quát là CnH2n + 2, CmH2m, Cn + m + 1H2m (đều là hiđrocacbon mạch hở và ở điều kiện thường đều là chất khí; n, m nguyên dương) và 0,1 mol H2 trong bình kín (xúc tác Ni). Sau khi các phản ứng xảy ra hoàn toàn, thu được hỗn hợp Y. Cho Y tác dụng với lượng dư dung dịch Br2 trong CCl4, thấy có tối đa 24 gam Br2 phản ứng. Mặt khác, đốt cháy hoàn toàn Y, thu được a mol CO2 và 0,5 mol H2O. Giá trị của a là:
- Câu 49:Số đồng phân cấu tạo bền, mạch hở có cùng công thức phân tử C3H6O2 đều tác dụng với kim loại Na là:
- Câu 50:Dãy nào sau đây chỉ gồm các kim loại vừa tác dụng với dung dịch HCl, vừa tác dụng với dung dịch NaOH?Loại B, D vì Cr không phản ứng với NaOH; loại C vì Cu không phản ứng với HCl
- Đáp án đúng của hệ thống
- Trả lời đúng của bạn
- Trả lời sai của bạn








