Điền từ còn thiếu vào chỗ trống
“Nguyên tử là hạt vô cùng nhỏ và (1) về điện. Nguyên tử gồm hạt nhân mang điện tích dương và vỏ tạo bởi (2) mang (3)”
Trắc nghiệm Hóa học 8 bài 4
Trắc nghiệm Hóa học 8 bài 4 có đáp án
Trắc nghiệm Hóa học 8 bài 4 gồm 15 câu hỏi trắc nghiệm kèm theo đáp án, hỗ trợ học sinh ôn luyện kiến thức môn Hóa 8 nhằm nâng cao kết quả các bài kiểm tra chương trình học lớp 8.
Mời các bạn tham gia nhóm Tài liệu học tập lớp 8 để nhận thêm những tài liệu hay: Tài liệu học tập lớp 8
Bộ câu hỏi Trắc nghiệm Hóa học 8 được xây dựng theo nội dung kiến thức trọng tâm của từng bài học, mỗi bài sẽ gồm những câu hỏi lí thuyết kèm theo bài tập theo từng cấp độ, giúp các em luyện tập dễ dàng tại nhà.
- Câu 1.
- Câu 2.
Chọn đán án đúng nhất
- Câu 3.
Cho biết số p, số e, số lớp e và số e lớp ngoài cùng của (I)
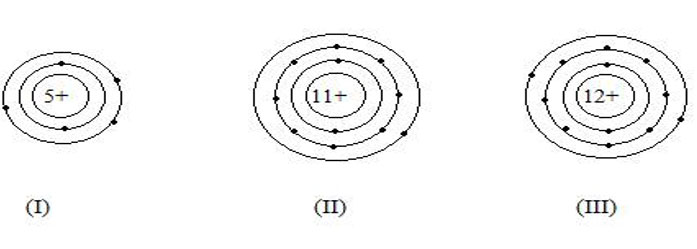
- Câu 4.
Chọn đáp án sai:
- Câu 5.
Đường kính của nguyên tử là
- Câu 6.
Nguyên tử có khả năng liên kết với nhau. Tại sao? Chọn đáp án đúng
- Câu 7.
Vì sao khối lương nguyên tử được coi bằng khối lượng hạt nhân. Chọn đáp án đúng
- Câu 8.
Trong khoảng không gian giữa hạt nhân và lớp vỏ electron của nguyên tử có những gì?
- Câu 9.
Hạt nhân được cấu tạo bởi:
- Câu 10.
Điền từ vào chỗ trống
“Trong tự nhiên, hidro có một người anh em sinh đôi là (1).Nguyên tử (2) còn được gọi là ‘hidro (3), chỉ khác có thêm 1 (4)” - Câu 11.
Trong nguyên tử hạt nào mang điện tích dương
- Câu 12.
Khối lượng tính theo gam của nguyên tử clo là
- Câu 13.
Nguyên tố cacbon (C) là tập hợp những nguyên tố có cùng
- Câu 14.
- Câu 15.
Tổng số hạt trong nguyên tử X là 40, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 12. Tính số hạt electron trong nguyên tử X.