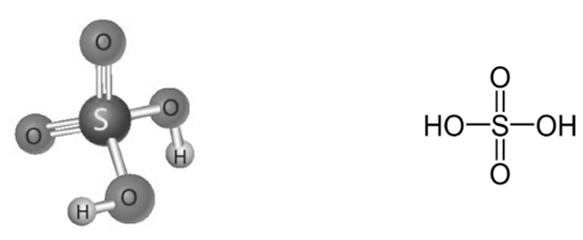Cho các nhận định sau về sulfuric acid đặc (H2SO4 đặc):
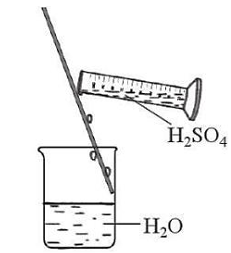
a. Khi pha loãng H2SO4 đặc cần rót từ từ acid đặc theo đũa thuỷ tinh vào nước, sau đó khuấy đều (mô tả ở dưới dưới). Đúng||Sai
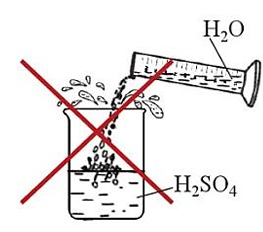
b. Không pha loãng H2SO4 đặc bằng cách đổ trực tiếp nước vào acid đặc vì phản ứng tỏa nhiệt mạnh, làm nước sôi đột ngột kéo theo những giọt acid bắn ra ngoài gây nguy hiểm (mô tả ở hình dưới). Đúng||Sai
c. Sulfuric acid đặc gây bỏng khi rơi vào da, do vậy cần tuân thủ các nguyên tắc trước khi thực hành thí nghiệm. Đúng||Sai
d. Khi bị bỏng bởi H2SO4 đặc cần nhanh chóng rửa sạch vị trí dính acid nhiều lần với dung dịch sodium hydroxide (NaOH), sau đó băng bó tạm thời bằng băng sạch rồi đến ngay cơ sở y tế gần nhất. Sai||Đúng
Cho các nhận định sau về sulfuric acid đặc (H2SO4 đặc):
a. Khi pha loãng H2SO4 đặc cần rót từ từ acid đặc theo đũa thuỷ tinh vào nước, sau đó khuấy đều (mô tả ở dưới dưới). Đúng||Sai

b. Không pha loãng H2SO4 đặc bằng cách đổ trực tiếp nước vào acid đặc vì phản ứng tỏa nhiệt mạnh, làm nước sôi đột ngột kéo theo những giọt acid bắn ra ngoài gây nguy hiểm (mô tả ở hình dưới). Đúng||Sai

c. Sulfuric acid đặc gây bỏng khi rơi vào da, do vậy cần tuân thủ các nguyên tắc trước khi thực hành thí nghiệm. Đúng||Sai
d. Khi bị bỏng bởi H2SO4 đặc cần nhanh chóng rửa sạch vị trí dính acid nhiều lần với dung dịch sodium hydroxide (NaOH), sau đó băng bó tạm thời bằng băng sạch rồi đến ngay cơ sở y tế gần nhất. Sai||Đúng
a. Đúng
b. Đúng
c. Đúng
d. Sai vì
Khi bị bỏng bởi H2SO4 đặc, tuyệt đối không được dùng dung dịch NaOH để rửa.
Vì NaOH là base mạnh, phản ứng trung hòa với acid sẽ:
Tỏa nhiệt mạnh → làm vết bỏng nặng hơn
Gây tổn thương sâu hơn cho mô da