Câu 1:
Trong phòng thí nghiệm, người ta thường điều chế clo bằng cách:
Đề thi thử THPT Quốc gia môn Hóa tháng 6/2016 Trường THPT Trần Hưng Đạo, TP Hồ Chí Minh là một bài test mẫu mà VnDoc chia sẻ với mục tiêu giúp các bạn học sinh lớp 12 ôn tập và rèn luyện, chuẩn bị cho kì thi THPT Quốc gia năm 2016 sắp tới. Chúc các bạn làm bài tốt!
Điểm khả dụng: 0 điểm
Bạn sẽ dùng 50 điểm để đổi lấy 1 lượt làm bài.
Bạn không đủ điểm để đổi.
Câu 1:
Trong phòng thí nghiệm, người ta thường điều chế clo bằng cách:
Câu 2:
Chất nào sau đây không có phản ứng tráng bạc?
Câu 3:
Cho hỗn hợp gồm 0,1 mol HCHO và 0,1 mol HCOOH tác dụng với lượng dư AgNO3 trong dung dịch NH3, đun nóng. Sau khi các phản ứng xảy ra hoàn toàn, khối lượng Ag tạo thành là (Ag = 108):
Câu 4:
Liên kết hóa học trong phân tử nào sau đây là liên kết ion?
Câu 5:
Trong số các loại tơ sau: tơ tằm, tơ visco, tơ nilon-6,6, tơ axetat, tơ nilon-6, tơ enang. Những loại tơ nào thuộc loại tơ nhân tạo là:
Câu 6:
Ancol và amin nào sau đây cùng bậc?
Câu 7:
Thứ tự sắp xếp theo sự tăng dần tính axit của CH3COOH; C2H5OH; dd HCl và C6H5OH là:
Câu 9:
Cho các phương trình phản ứng
(a) 2Fe + 3Cl2 → 2FeCl3 (b) NaOH + HCl → NaCl + H2O
(c) Fe3O4 + 4CO → 3Fe + 4CO2 (d) AgNO3 + NaCl → AgCl + NaNO3
Trong các phản ứng trên, số phản ứng oxi hóa - khử là:
Câu 10:
Cho hỗn hợp X gồm Fe3O4, ZnO và Cu tác dụng với dung dịch HCl dư thu được dung dịch Y và phần không tan Z. Cho NaOH dư vào dung dịch Y (trong điều kiện không có không khí) thu được kết tủa nào sau đây?.
Câu 11:
Tinh bột, xenlulozơ, saccarozơ, mantozơ đều có khả năng thamgia phản ứng:
Câu 13:
Hoà tan hoàn toàn 3,22g hỗn hợp X gồm Fe, Mg, Zn bằng một lượng vừa đủ H2SO4 loãng thấy thoát 1,344 lít H2 ở đktc và dung dịch chứa m gam muối. Giá trị của m là (cho H = 1; O = 16;S = 32)
Câu 14:
Khí thiên nhiên được dùng làm nhiên liệu và nguyên liệu cho các nhà máy sản xuất điện, sứ, đạm, ancol metylic,...Thành phần chính của khí thiên nhiên là metan. Công thức phân tử của metan là:
Câu 15:
Kim loại Mg không phản ứng với dung dịch chất nào sau đây?
Câu 16:
Để khử mùi tanh của cá (gây ra do một số amin) ta có thể rửa cá với:Câu 17:
Thành phần hoá học chính của quặng boxit là:Câu 18:
Cấu hình e của 24Cr2+ là:Câu 19:
Chất béo là trieste của axit béo với:Câu 20:
Khí X làm đục nước vôi trong và được dùng làm chất tẩy trắng bột gỗ trong công nghiệp giấy. Chất X là:Câu 21:
Ở điều kiện thường, dãy kim loại nào sau đây đều phản ứng với nước?Câu 22:
Este X có công thức phân tử C2H4O2. Đun nóng 9,0 gam X trong dung dịch NaOH vừa đủ đến khi phản ứng xảy ra hoàn toàn thu được m gam muối. Giá trị của m là (Cho H=1; C=12; O=16; Na=23):Câu 23:
Dãy cation kim loại được xếp theo chiều tăng dần tính oxi hóa từ trái sang phải là:Câu 24:
Dãy gồm các hợp chất được sắp xếp theo thứ tự tăng dần lực bazơ là:Câu 25:
Khử hoàn toàn 17,6 gam hỗn hợp X gồm Fe, FeO, Fe2O3 cần 2,24 lít CO (ở đktc). Khối lượng sắt thu được là (Cho C=12; O=16; Fe=56):Câu 26:
Anđehit thể hiện tính khử khi tác dụng với chất nào trong số các chất sau?Câu 27:
Cho 3,6gam Mg tác dụng hết với dung dịch HNO3 (dư),sinh ra 2,24 lít khí X(sản phẩm khử duy nhất, ở đktc). Khí X là (Cho Mg =24, H = 1, N = 14, O = 16)Câu 28:
Axit HCOOH không tác dụng được với dung dịch nào sau đây?Câu 29:
Ở trạng thái cơ bản, cấu hình electron của nguyên tử Na (Z = 11) là:Câu 30:
Polime nào sau đây được tổng hợp bằng phản ứng trùng ngưng:Câu 31:
Đốt cháy hoàn toàn 4,64gam một hiđro cacbon X (chất khí ở điều kiện thường) rồi đem toàn bộ sản phẩm cháy hấp thụ hết vào bình đựng dung dịch Ba(OH)2. Sau các phản ứng thu được39,4gam kết tủa và khối lượng phần dung dịch giảm bớt 19,912gam. Công thức phân tử của X là (Cho C = 12, H = 1, Ba = 137, O = 16)Câu 32:
Nhằm đạt lợi ích về kinh tế, một số trang trại chăn nuôi heo đã bất chấp thủ đoạn dùng một số hóa chất cấm trộn vào thức ăn với liều lượng cao trong đó có Salbutamol. Salbutamol giúp heo lớn nhanh, tỉ lệ nạc cao, màu sắc thịt đỏ hơn. Nếu con người ăn phải thịt heo được nuôi có sử dụng Salbutamol sẽ gây ra nhược cơ, giảm vận động của cơ, khớp khiến cơ thể phát triển không bình thường. Salbutamol có công thức cấu tạo thu gọn nhất như sau: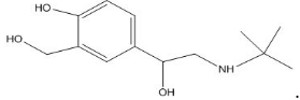
Câu 33:
Cho hỗn hợp X gồm ancol metylic và hai axit cacboxylic (no, đơn chức, kế tiếp nhau trong dãy đồng đẳng) tác dụng hết với Na, giải phóng ra 6,72 lít khí H2 (đktc). Nếu đun nóng hỗn hợp X (có H2SO4 đặc làm xúc tác) thì các chất trong hỗn hợp phản ứng vừa đủ với nhau tạo thành 25 gam hỗn hợp este (giả thiết phản ứng este hoá đạt hiệu suất 100%). Hai axit trong hỗn hợp X là (Cho H = 1, O = 16, C = 12, Na = 23)Câu 34:
Hỗn hợp X gồm Al, Fe2O3, Fe3O 4, CuO trong đó oxi chiếm 25,39% khối lượng hỗn hợp. Cho m gam hỗn hợp X tác dụng với 8,96 lít CO (điều kiện tiêu chuẩn) sau một thời gian thu được chất rắn Y và hỗn hợp khí Z có tỉ khối so với hiđro là 19. Cho chất rắn Y tác dụng với dd HNO3 loãng dư thu được dd T và 7,168 lít NO (điều kiện tiêu chuẩn, sản phẩm khử duy nhất). Cô cạn dd T thu được 3,456m gam muối khan. Giá trị của m gần với giá trị nào sau đây nhất?Câu 35:
Hỗn hợp X gồm chất Y (C2H10O3N2) và chất Z (C2H7O2N). Cho 14,85 gam X phản ứng vừa đủ với dung dịch NaOH và đun nóng, thu được dung dịch M và 5,6 lít (đktc) hỗn hợp T gồm 2 khí đều làm xanh quỳ tím ẩm. Cô cạn toàn bộ dung dịch M thu được m gam muối khan. Giá trị của m là (Cho H=1; C=12; O=16; Na=23; N=14):Câu 36:
Đốt cháy hoàn toàn 0,2 mol hỗn hợp X gồm một ankan và một anken, thu được 0,35 mol CO2 và 0,4 mol H2O. phần trăm số mol anken trong X là (Cho C = 12, O = 16, H = 1)Câu 37:
Tiến hành điện phân (với điện cực trơ, hiệu suất 100%, dòng điện có cường độ không đổi) với dung dịch X gồm 0,2mol CuSO4 và 0,15 mol HCl, sau một thời gian điện phân thu được dung dịch Y có khối lượng giảm 14,125g so với khối lượng dung dịch X. Cho 15g bột Fe vào Y đến khi kết thúc các phản ứng thu được m gam chất rắn. Biết các khí sinh ra hòa tan không đáng kể trong nước. Giá trị của m là (Cho Cu=64; O=16; H=1; S=32; Cl=35,5; O=16):Câu 38:
Hỗn hợp M gồm axit X, rượu Y và este Z được tạo ra từ X và Y, tất cả đều đơn chức; trong đó số mol X gấp hai lần số mol Y. Biết 17,35 gam M tác dụng vừa đủ với dung dịch chứa 0,2 mol NaOH, đồng thời thu được 16,4 gam muối khan và 8,05 gam rượu. Phần trăm khối lượng của Y là ( Cho H=1; C=12; O=16; Na=23)Câu 39:
Phát biểu nào sau đây sai:Câu 40:
Hỗn hợp X gồm hai chất hữu cơ no , mạch hở (đều chứa C, H, O), trong phân tử mỗi chất có hai nhóm chức trong số các nhóm –OH, -CHO, -COOH. Cho m gam X phản ứng hoàn toàn với lượng dư dung dịch AgNO3 trong NH3, thu được 4,05 gam Ag và 1,86 gam một muối amoni hữu cơ. Cho toàn bộ lượng muối amoni hữu cơ này vào dung dịch NaOH (dư, đun nóng), thu được 0,02 mol NH3. Giá trị của m là (Cho C = 12, O = 16, H = 1, Ag = 108, N = 14)Câu 41:
Thực hiện phản ứng nhiệt nhôm hỗn hợp gồm m gam Al và 4,56gam Cr2O3 (trong điều kiện không có O2), sau khi phản ứng kết thúc, thu được hỗn hợp X. Cho toàn bộ X vào một lượng dư dung dịch HCl (loãng, nóng), sau khi các phản ứng xảy ra hoàn toàn, thu được 2,016 lít H2 (đktc). Còn nếu cho toàn bộ X vào một lượng dư dung dịch NaOH (đặc, nóng), sau khi các phản ứng kết thúc thì số mol NaOH đã phản ứng là (Cho Al = 27, Cr = 52, O = 16, Cl = 35,5, H = 1, Na = 23)Câu 42:
Thủy phân một lượng pentapeptit mạch hở X chỉ thu được 3,045 gam Ala-Gly-Gly; 3,48 gam Gly-Val; 7,5 gam Gly; 2,34 gam Val; x mol Val-Ala và y mol Ala.Biết X có công thức Ala-Gly-Gly-Val-Ala. Tỷ lệ x:y là (C=12, H=1, N=14, O=16):Câu 43:
Thủy phân dung dịch chứa 34,2 gam mantozơ một thời gian. Lấy toàn bộ các chất thu được sau phản ứng thủy phân cho tác dụng với lượng dư dung dịch AgNO3 trong NH3, sau phản ứng hoàn toàn thu được 31,32 gam Ag. Hiệu suất của phản ứng thủy phân mantozơ là:Câu 44:
Tiến hành thí nghiệm như hình vẽ. Khí A trong bình có thể là khí nào dưới đây?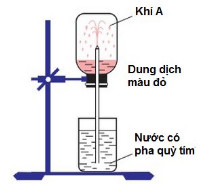
Câu 45:
Biết X là axit cacboxylic đơn chức, Y là ancol no, cả hai chất đều mạch hở, có cùng số nguyên tố cacbon. Đốt cháy hoàn toàn 0,4 mol hỗn hợp gồm X và Y (trong đó số mol của X lớn hơn số mol của Y) cần vừa đủ 30,24 lít khí O2, thu được 26,88 lít khí CO2 và 19,8 gam H2O. Biết thể tích các khí đó ở điều kiện tiêu chuẩn. Khối lượng của Y trong 0,4 mol hỗn hợp trên là (C=12, H=1, O=16):Câu 46:
Cho các phản ứng sau: (1) glucozơ + Br2 + H2O; (2) fructozơ + H2 (xt Ni, to); (3) fructozơ + dd AgNO3/NH3; (4) glucozơ + dd AgNO3/NH3; (5) fructozơ + Br2 + H2O; (6) dd saccarozơ + Cu(OH)2. Hãy cho biết có bao nhiêu phản ứng xảy ra?Câu 47:
Hỗn hợp X gồm Na và Al, cho m gam X vào lượng dư H2O thu được 5 lít khí. Nếu cũng cho m gam X vào dd NaOH dư thì thu được 8,75 lit khí (các thể tích khí đo ở cùng điều kiện về nhiệt độ và áp suất). Tính % về khối lượng của Na có trong hỗn hợp X. (cho Na=23; Al=27)Câu 48:
Hòa tan hoàn toàn 2,7 gam hỗn hợp X gồm Fe, Cr, Al bằng dung dịch HCl dư, thu được 1,568 lít khí H2 (đktc). Mặt khác, cho 2,7 gam X phản ứng hoàn toàn với khí Cl2 dư, thu được 9,09 gam muối. Khối lượng Al trong 2,7 gam X là bao nhiêu?Câu 49:
Hòa tan hết m gam chất rắn X gồm Fe, FeS, FeS2 bằng dung dịch HNO3 dư, sau khi phản ứng xảy ra hoàn toàn thu được 4,48 lít (đktc) hỗn hợp sản phẩm khử chỉ gồm hai khí NO và NO2 có tỉ khối so với H2 là 17,4 và dung dịch Y chỉ chứa hai chất tan. Giá trị m là (Cho Fe=56; S=32;O=16; H=1; N=14)Câu 50:
Tiến hành các thí nghiệm sau:Theo Nghị định 147/2024/ND-CP, bạn cần xác thực tài khoản trước khi sử dụng tính năng này. Chúng tôi sẽ gửi mã xác thực qua SMS hoặc Zalo tới số điện thoại mà bạn nhập dưới đây: