Đề thi giải toán trên Máy tính cầm tay tỉnh Bạc Liêu môn Hóa lớp 12 năm học 2009 - 2010 (Có đáp án)
Vndoc.com xin giới thiệu đến các bạn: Đề thi giải toán trên Máy tính cầm tay tỉnh Bạc Liêu môn Hóa lớp 12 năm học 2009 - 2010 (Có đáp án).
Đề thi giải toán trên Máy tính môn Hóa:
SỞ GIÁO DỤC VÀ ĐÀO TẠO
|
KỲ THI GIẢI TOÁN MTCT LỚP 12 VÒNG TỈNH
|
MÔN THI: HÓA HỌC - LỚP 12
(Thời gian làm bài 150 phút không kể thời gian giao đề)
--------------------------------------------------------------------------------
Câu 1 (5 điểm):
Tính bán kính của nguyên tử Fe ở 200C,biết ở nhiệt độ đó khối lượng riêng của Fe là 7,87g/cm3, giả thiết trong tinh thể Fe kim loại, các nguyên tử Fe là những hình cầu chiếm 75% thể tích tinh thể, phần còn lại là các khe rỗng giữa các quả cầu.
Cho khối lượng nguyên tử của Fe là 55,85; π = 3.1416, số Avogadro NA = 6,02.1023.
Câu 2 (5 điểm):
Một nguyên tố X có khả năng tạo nhiều oxi axit. Thành phần phần trăm khối lượng các nguyên tố trong một muối của X được ghi trong bảng sau:
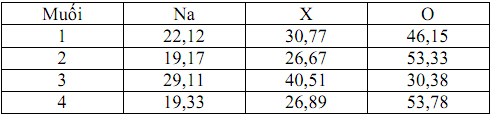
Xác định công thức phân tử của 4 muối trên.
Câu 3 (5 điểm):
Tính khối lượng riêng của nguyên tử hiđro và nguyên tử kẽm, biết khối lượng nguyên tử của hiđro là 1,008 đvC và của kẽm là 65,38 đvC, bán kính nguyên tử của H là 0,53.10-8cm và của nguyên tử kẽm là 1,37.10-8cm; 1đvC = 1,66.10-24gam, các nguyên tử H và Zn là những hình cầu.
So sánh khối lương riêng của nguyên tử H và của khí H2 (đktc), khối lượng riêng của nguyên tử Zn và của kim loại Zn, biết khối lượng riêng của kim loại Zn là 7,113g/cm3. Giải thích.
Câu 4 (5 điểm):
A là dung dịch HCl 0,2M; B là dung dịch NaOH 0,2M; C là dung dịch CH3COOH 0,2M (có hằng số axit Ka = 1,8.10-5).
a) Tính pH của dung dịch X là dung dịch tạo thành khi trộn dung dịch B với dung dịch C theo tỉ lệ thể tích 1: 1.
b) Tính thể tích dung dịch B (theo ml) cần thêm vào 20ml dung dịch A để thu được dung dịch có pH bằng 10.
Câu 5 (5 điểm):
Tìm nhiệt tạo thành tiêu chuẩn của Ca3(PO4)2 tinh thể. Biết:
- 12gam Ca cháy tỏa 45,57kcal.
- 6,2gam P cháy tỏa 37,00kcal.
- 168gam CaO tác dụng với 142gam P2O5 tỏa 160,50kcal.
(Hiệu ứng nhiệt đo trong điều kiện đẳng áp).
Câu 6 (5 điểm):
Thêm 1g MgSO4 vào 100g dung dịch bão hòa MgSO4 ở 200C làm 1,58g MgSO4 kết tinh trở lại dạng khan.
Xác định công thức phân tử muối MgSO4 ngậm nước. Biết ở 200C, độ tan của MgSO4 khan trong 100g H2O là 35,1g.
Câu 7 (5 điểm):
Tính:
a) Khoảng cách giữa 2 nguyên tử cacbon đầu mạch của propan, biết độ dài liên kết C-C là 1,540A; các nguyên tử cacbon đều lai hóa sp3.
b) Khoảng cách giữa 2 nguyên tử clo trong phân tử C2H2Cl2, biết độ dài liên kết C=C là 1,330A , liên kết C-Cl là 1,760A.
Câu 8 (5 điểm):
Đốt cháy hoàn toàn hỗn hợp A (gồm x mol muối natri của 2axit cacboxylic no đơn chức mạch hở X1, X2 đồng đẳng kế tiếp nhau và 0,01mol HCOONa). Cho sản phẩm cháy (CO2 và hơi nước) lần lượt qua bình 1 chứa H2SO4 đặc và bình 2 chứa KOH dư thấy khối lượng bình 2 tăng nhiều hơn bình 1 là 3,51(g). Phần chất rắn B còn lại sau khi đốt là 2,65(g) Na2CO3.
Xác định công thức phân tử của 2 muối natri.
Câu 9 (5 điểm):
Cho phản ứng: Cu(r) + CuCl2(dung dịch) -> 2CuCl(r)
Ở 25oC phản ứng xảy ra theo chiều nào, nếu trộn một dung dịch chứa CuSO4 0,2M; NaCl 0,4M với bột Cu lấy dư.![]()
Câu 10 (5 điểm):
Đốt cháy một hiđrocacbon A (khí) với oxi trong một bình kín. Nếu giữ nguyên nồng độ của A và tăng nồng độ oxi gấp đôi thì tốc độ phản ứng cháy tăng gấp 32 lần.
