Giải SBT KHTN 9 Cánh diều Bài 17
Bài 17: Tách kim loại. Sử dụng hợp kim
Giải SBT KHTN 9 Bài 17: Tách kim loại. Sử dụng hợp kim hướng dẫn trả lời câu hỏi trong sách bài tập Khoa học tự nhiên 9 Cánh diều, giúp các em học sinh củng cố kiến thức được học môn KHTN Bài 17. Sau đây mời các bạn tham khảo.
17.1
Phát biểu nào sau đây về quá trình tách kim loại là đúng?
A. Là quá trình biến đổi khoáng vật trong quặng thành một hợp chất của kim loại. Sau đó, dùng các phương pháp thích hợp để tách được kim loại từ hợp chất đó.
B. Là quá trình dùng các phản ứng hóa học để tách được kim loại từ hợp chất của kim loại.
C. Sử dụng quá trình biến đổi vật lí để thu được hợp chất của kim loại từ khoáng vật. Sau đó dùng các phản ứng hóa học để tách được kim loại từ hợp chất của kim loại.
D. Là quá trình sử dụng phương pháp điện phân hoặc phương pháp nhiệt luyện hay phương pháp thủy luyện để tách được kim loại từ hợp chất từ kim loại.
Hướng dẫn giải:
Là quá trình biến đổi khoáng vật trong quặng thành một hợp chất của kim loại. Sau đó, dùng các phương pháp thích hợp để tách được kim loại từ hợp chất đó.
Đáp án A
17.2
Phát biểu nào sau đây về các phương pháp tách kim loại từ hợp chất của kim loại là không đúng?
A. Phương pháp điện phân nóng chảy thường được dùng để tách các kim loại có mức độ hoạt động hóa học mạnh như Na, Mg, Al,…
B. Phương pháp nhiệt luyện thường được dùng để tách các kim loại có mức độ hoạt động hóa học trung bình như Zn, Fe, Pb,…
C. Phương pháp thủy luyện thường được dùng để tách các kim loại có mức độ hoạt động hóa học yếu như Cu, Ag, Au,…
D. Các kim loại có độ hoạt động hóa học khác nhau đáng kể thường được tách ra khỏi hợp chất của chúng bằng phương pháp khác nhau.
Hướng dẫn giải:
Phương pháp nhiệt luyện thường được dùng để tách các kim loại có mức độ hoạt động hóa học trung bình và yế như Zn, Fe, Pb, Cu,…
Đáp án B
17.3
Phát biểu nào sau đây là không đúng khi nói về sodium chloride (NaCl) và phương pháp tách natri ra khỏi sodium chloride?
A. Vì natri có độ hoạt động hóa học mạnh nên hợp chất sodium chloride rất bền.
B. Cần điện phân sodium chloride nóng chảy theo phương trình hóa học sau để thu được natri:
![]()
C. Có thể thực hiện phản ứng ở nhiệt độ cao để thu được Na: ![]()
D. Sau khi thu được natri từ hợp chất, cần bảo quản natri bằng cách lập tức ngâm nó trong dầu hỏa khan.
Hướng dẫn giải:
C sai, vì Zn yếu hơn Na.
Đáp án C
17.4
Phát biểu nào sau đây là không đúng khhi nói về magnesium oxide (MgO), zinc oxide (ZnO), iron(III) oxide (Fe2O3) và phương pháp tách kim loại ra khỏi mỗi oxide.
A. Do Zn và Fe có độ hoạt động hóa học trung bình, Mg có độ hoạt động hóa học mạnh nên ZnO, Fe2O3 là các oxide kém bền hơn so với MgO.
B. Trong công nghiệp, việc tách Zn và Fe ra khỏi oxide theo phương trình hóa học sau:
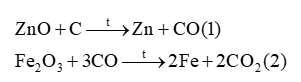
C. Nếu thực hiện phản ứng:![]() thì dự đoán rằng phản ứng (3) sẽ tốn ít năng lượng hơn so với phản ứng (2).
thì dự đoán rằng phản ứng (3) sẽ tốn ít năng lượng hơn so với phản ứng (2).
D. (1) và (2) là phản ứng tách kim loại theo phương pháp nhiệt luyện.
Hướng dẫn giải:
C sai, vì MgO không phản ứng với carbon.
Đáp án C
17.5
Phát biểu nào sau đây là không đúng về gang và thép?
A. Gang và thép đều là vật liệu kim loại tạo bởi kim loại cơ bản là sắt.
B. Gang được sử dụng phổ biến hơn thép.
C. Hàm lượng carbon trong thép nhỏ hơn hàm lượng carbon trong gang.
D. Gang và thép cứng hơn kim loại sắt.
Hướng dẫn giải:
D sai vì gang giòn hơn sắt.
Đáp án D
17.6
Ở Mĩ, người ta xử lí nước biển để thu được muối magnesium chloride (MgCl2). Dựa vào độ hoạt động hóa học của magnesium, đề xuất phương pháp tách mg từ magnesium chloride. Viết phương trình hóa học của phản ứng xảy ra.
Hướng dẫn giải:
Dùng phương pháp điện phân nóng chảy muối MgCl2 để thu được magnesium.
PTHH: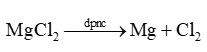
17.7
Thực hiện thí nghiệm theo mô tả hình bên. Nung nóng ống nghiệm một thời gian, để nguội thu được chất rắn có màu đen và màu nâu đỏ xen lẫn.
a) Viết phương trình hóa học của phản ứng diễn ra.
b) Dự đoán thành phần của hỗn hợp rắn trong ống nghiệm sau khi để nguội.
c) Gọi tên của phương pháp tách kim loại trên.
Hướng dẫn giải:
a) ![]()
b) Hỗn hợp rắn trong ống nghiệm: Cu và CuO.
c) Phương pháp nhiệt luyện.
17.8
Hòa tan hoàn toàn 2,4 gam magnesium trong dung dịch hydrochloric acid dư.
a) Tính số mol khí hydrogen thu được.
b) Dẫn toàn bộ lượng khí hydrogen trên vào một ống thủy tinh nằm ngang chứa 8,0 gam bột CuO, đun nóng để thực hiện phản ứng điều chế Cu theo phương trình hóa học: CuO + H2 Cu + H2O
Thực tế, chỉ có 75% lượng khí hydrogen phản ứng với CuO. Sau khi dừng phản ứng: ![]()
Thu được hỗn hợp chất rắn A gồm các chất nào?
Khối lượng chất rắn A là bao nhiêu gam?
c) Cần cho chất rắn A trong lượng dư của chất nào sau đây để thu được kim loại đồng: nước, dung dịch hydrochloric acid, dung dịch sodium hydroxide? Giải thích.
Hướng dẫn giải:
a) n Mg = 2,4 : 24 = 0,1 mol
Mg + 2HCl → MgCl2 + H2
0,1 0,1
V H2 = 0,1.24,79 = 2,479 lít.
b) Hỗn hợp chất rắn A gồm Cu và CuO.
![]()
0,1
m Cu = 0,1.75%.64 = 4,8g
m CuO dư = 8 – 0,075.80 = 2g
m A = 4,8 + 2 = 6,8g
c) Cần cho vào dung dịch HCl để hòa tan CuO, thu được kim loại đồng.
17.9
Vật trang trí bằng đồng thường bị đen do lớp đồng bên ngoài phản ứng với oxygen trong không khí.
a) Người ta có thể dùng bông thấm dung dịch hydrochloric acid loãng chà lên các vết đen ấy. Vì sao? Viết các phương trình hóa học của phản ứng xảy ra.
b) Có thể thay dung dịch hydrochloric acid bằng giấm hoặc nước cốt chanh được không? Vì sao?
Hướng dẫn giải:
a) Vì các vết đen đó hình thành do Cu bị oxi hóa trong không khí tạo thành CuO. Khi dùng dung dịch HCl loãng có thể hòa tan CuO.
CuO + 2HCl ![]() \(\to\)CuCl2 + H2O
\(\to\)CuCl2 + H2O
b) Có thể thay thế HCl thành giấm hoặc nước cốt chanh. Vì giấm hoặc nước cốt chanh có môi trường acid hòa tan được CuO.
17.11
Điền 10 thông tin phù hợp (từ (1) đến (10)) vào các chỗ trống trong đoạn mô tả gang và quá trình sản xuất gang dưới đây.
Gang là vật liệu kim loại tạo bởi kim loại cơ bản là …(1)… cùng với khoảng …(2)… % carbon theo khối lượng.
Nguyên liệu chính để sản xuất là quặng, sắt, …(3)… và đá vôi. Các nguyên liệu này được xếp thành từng lớp xen kẽ và được cho di chuyển chậm từ …(4)… xuống đáy lò, tiếp xúc với luồng không khí nóng đi ngược từ phía đáy lò lên. Các phản ứng hóa học chính diễn ra trong quá trình nguyên liệu di chuyển từ đỉnh lò xuống đáy lò là:
C + …(5)… ![]() \(\to\)CO2
\(\to\)CO2
CO2 + …(6)… ![]() \(\to\)CO
\(\to\)CO
Fe2O3+ CO ![]() \(\to\)…(7) + …(8)…
\(\to\)…(7) + …(8)…
Gần đáy lò, sắt ở trạng thái …(9)… hòa tan một lượng nhỏ …(10)… cùng một số nguyên tố khác nhau như Mn, Si, P,…tạo thành gang lỏng, chảy xuống đáy lò và sau đó được dẫn ra ngoài qua cửa tháo gang.
Hướng dẫn giải:
(1): sắt; (2): 2 – 5; (3): than; (4): đỉnh lò; (5): O2; (6): C; (7): Fe (hoặc CO2); (8): CO2 (hoặc Fe); (9): nóng chảy; (10): carbon.
17.12
Điền 5 thông tin phù hợp (từ (1) đến (5)) vào các chỗ trống trong đoạn mô tả thép và quá trình sản xuất thép dưới đây.
Thép là hợp kim phổ biến của nguyên tố …(1)… với khoảng dưới …(2)… %carbon và lượng nhỏ của một số kim loại khác.
Nguyên liệu để sản xuất thép thường là gang, sắt phế liệu và khí …(3)… khí này được sục vào lò chứa hỗn hợp gang và sắt phế liệu nóng chảy, phản ứng với một phần nguyên tố …(4)… tạo thành khí …(5)… thoát ra khỏi lò. Nhờ quá trình này, đã biến nguyên liệu ban đầu thành thép nóng chảy.
Hướng dẫn giải:
(1): sắt; (2): 2; (3): oxygen; (4): carbon; (5): CO2.
17.13
Hãy tìm hiểu và cho biết thành phần cơ bản và tính chất quan trọng của hợp kim dùng để chế tạo:
a) Vỏ máy bay (lớp phủ của thân và cánh máy bay).
b) Dụng cụ phẫu thuật.
c) Mỏ neo của tàu biển.
Hướng dẫn giải:
a) Hợp kim của nhôm (Al với mg, Mn): nhẹ, bền
b) Inox (hợp kim của Fe với C, Cr, Mo, Ni): không gỉ, cứng, sáng bóng, chống mài mòn.
c) Thép (hợp kim của Fe với C, Ni, Mg, Cr): khối lượng riêng lớn, bền trong môi trường nước biển và nước sông; khả năng chống mài mòn cao.

