H = 1; Li = 7; Be = 9; C = 12; N = 14; P = 31; O = 16; Na = 23; Mg = 24; Al = 27; S = 32; Cl = 35,5; K = 39; Ca = 40; Fe = 56; Cu = 64; Zn = 65; Rb = 85; Sr = 88; Ag = 108; Ba = 137.
Cho 10 gam hỗn hợp CaCO3 và KHCO3 tác dụng với dung dịch HCl dư thu được V lít khí CO2 (đktc). Giá trị V là:
Đun nóng dung dịch chứa m gam glucozơ với lượng dư dung dịch AgNO3 trong NH3, đến khi phản ứng xảy ra hoàn toàn thu được 21,6 gam Ag. Giá trị của m là:
Chất nào không là đipeptit?
Cho dãy các chất: Al, Al(OH)3, Al2O3, AlCl3, NaHCO3. Số chất lưỡng tính trong dãy là:
Dung dịch FeCl2 không tác dụng được với kim loại:
Phản ứng nào dưới đây thuộc loại phản ứng nhiệt nhôm?
Dãy gồm các kim loại được xếp theo chiều tính khử giảm dần là:
Este X có tỉ khối so với H2 bằng 37. Thủy phân X trong dung dịch NaOH thu được CH3COONa. Công thức của este X là:
Dãy chất nào sau đây mà dung dịch của chúng làm quỳ tím chuyển xanh?
Chất nào không tham gia phản ứng trùng hợp?
Cho các chất sau: etanol, metylamin, metyl axetat, alanin, axit axetic. Số chất tác dụng với dung dịch NaOH là:
H2S không thể hiện tính khử khi phản ứng với:
Phenol không phản ứng được với chất nào sau đây?
Đốt cháy hoàn toàn m gam C2H5NH2 thu được sản phẩm gồm H2O, CO2 và 1,12 lít khí N2 (đktc). Tổng khối lượng CO2 và H2O thu được là:
Cho 11,2 gam Fe tác dụng với dung dịch HNO3 loãng, dư thu được sản phẩm khử NO duy nhất. Thể tích khí NO (đktc) thu được là:
Ion X2- có cấu hình 1s22s22p6. Nguyên tố X là:
Dung dịch nào sau đây dùng để phân biệt dung dịch NaCl với dung dịch Na2SO4?
Chất làm mềm nước có tính cứng toàn phần là:
Cho 0,1 mol glyxin tác dụng vừa đủ với dung dịch HCl. Khối lượng muối khan thu được là:
Cacbohiđrat nào sau đây thuộc loại đisaccarit?
Tơ nào sau đây thuộc loại tơ nhân tạo?
Chất X tác dụng được với dung dịch HCl. Khi chất X tác dụng với dung dịch NaOH sinh ra kết tủa. Chất X là:
Phản ứng giữa triolein với NaOH là phản ứng:
Cho từ từ dung dịch NH3 đến dư vào dung dịch AlCl3 thấy xuất hiện:
Cho dãy các kim loại: K, Mg, Cu, Al, Fe, Ag. Số kim loại trong dãy phản ứng được với dung dịch HCl là:
Cho 8,0 gam hỗn hợp X gồm Fe và Cu phản ứng với dung dịch HCl loãng (dư), đến khi phản ứng xảy ra hoàn toàn thu được 2,24 lít khí H2 (đktc). Khối lượng của Cu trong 8,0 gam hỗn hợp X là:
Dẫn hỗn hợp khí gồm CO2, O2, N2 và H2 qua dung dịch NaOH. Khí bị hấp thụ là:
Lên men m gam glucozơ để điều chế ancol etylic, hiệu suất phản ứng 80%, thu được 17,92 lít khí CO2 (đktc). Giá trị của là:
Cặp chất là đồng phân của nhau là:
Đốt cháy 5,6 gam Fe bằng khí clo dư, khối lượng muối thu được là:
Tiến hành các thí nghiệm sau:
(a) Cho dung dịch AgNO3 vào dung dịch FeCl2;
(b) Sục H2S dư vào dung dịch hỗn hợp FeCl2 và CuCl2 (không có mặt của oxi);
(c) Cho dung dịch AgNO3 dư vào dung dịch hỗn hợp NaBr và NaF;
(d) Cho Ba tan hết trong dung dịch Mg(HCO3)2.
Thí nghiệm thu được 2 kết tủa là:
Có các phát biểu sau:
(a) Có thể dùng nước brom để phân biệt glucozơ và fructozơ.
(b) Trong môi trường axit, glucozơ và fructozơ có thể chuyển hoá lẫn nhau.
(c) Các dung dịch glucozơ và saccarozơ đều có phản ứng tráng bạc.
(d) Dung dịch saccarozơ hoà tan Cu(OH)2 ở nhiệt độ thường cho dung dịch màu xanh lam.
(e) Phân tử saccarozơ được cấu tạo bởi hai gốc α-glucozơ.
(f) Hợp chất hữu cơ chứa N đều độc.
(g) Tất cả các peptit đều có phản ứng màu biure.
Số phát biểu đúng là:
Thổi hơi nước qua than nóng đỏ thu được hỗn hợp khí gồm CO, CO2, H2 có tỉ khối so với H2 là 7,875. Phần trăm thể tích CO2 trong khí trên là:
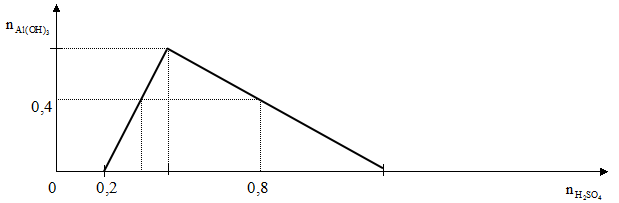
Hòa tan 1,2 gam kim loại M vào nước được dung dịch X. Cho X vào 100 ml dung dịch AlCl3 0,1M thì thấy tạo ra kết tủa, sau đó kết tủa tan một phần. Kim loại M là:
Tiến hành các thí nghiệm sau:
(a) Nhiệt phân đá vôi; (b) Cho metan tác dụng với clo, chiếu sáng;
(c) Nhiệt phân bạc nitrat; (d) Cho clo tác dụng vôi sữa để điều chế clorua vôi;
(e) Nhiệt phân kali pemanganat; (f) Dẫn etilen qua dung dịch thuốc tím.
Số thí nghiệm có phản ứng oxi hóa – khử là:
Hòa tan hoàn toàn hỗn hợp gồm x mol Fe và x mol Fe2O3 trong dung dịch H2SO4 loãng dư thấy thoát ra 2,688 lít khí H2 (đktc) và thu được dung dịch Y. Để oxi hóa hoàn toàn Fe2+ trong dung dịch Y cần dùng 180 ml dung dịch KMnO4 0,2M. Giá trị của x là:
Amino axit X có công thức H2NR(COOH)2. Cho 0,1 mol X vào 0,2 lít dung dịch gồm H2SO4 0,5M và HCl 1M thu được dung dịch Y. Cho Y phản ứng vừa đủ với V lit dung dịch gồm NaOH 1M và KOH 3M. Giá trị V là:
Hỗn hợp X gồm etilen, axetilen và hiđro. Đốt cháy hoàn toàn X thu được số mol CO2 bằng số mol H2O. Mặt khác dẫn V lít X qua Ni nung nóng thu được 0,8V lít hỗn hợp Y. Cho toàn bộ Y tác dụng với dung dịch brom dư thì có 32 gam brom đã phản ứng. Biết các thể tích khí đều đo ở đktc. Giá trị của V là:
Hỗn hợp X gồm HCHO (0,15 mol) và anđehit Y. Đốt cháy hoàn toàn hỗn hợp X thu được 12,32 lít (đktc) CO2 và m gam H2O. Mặt khác, nếu cho hỗn hợp X tác dụng với lượng dư dung dịch AgNO3/NH3 thu được tối đa 1,40 mol Ag. Giá trị của m là:
Có hỗn hợp FeO + Al2O3 được chia thành 2 phần bằng nhau:
Phần 1: Tan vừa đủ trong dung dịch có 0,9 mol HCl
Phần 2: Đem nung nóng rồi thổi H2 qua, sau một thời gian được 20,2 gam hỗn hợp gồm ba chất rắn và sinh ra 0,9 gam nước.
Phần trăm khối lượng Al2O3 trong hỗn hợp ban đầu là:
Thuỷ phân hoàn toàn m gam một pentapeptit mạch hở M thu được hỗn hợp gồm hai amino axit X1, X2 (đều no, mạch hở, phân tử chứa một nhóm –NH2 và một nhóm -COOH). Đốt cháy toàn bộ lượng X1, X2 ở trên cần dùng vừa đủ 0,1275 mol O2, chỉ thu được N2, H2O và 0,11 mol CO2. Giá trị của m là:
Một hỗn hợp T gồm 2 este X, Y mạch hở (MX< MY). Nếu đun nóng 15,7 gam hỗn hợp T với dung dịch NaOH dư thì thu được một muối của axit hữu cơ đơn chức và 7,6 gam hỗn hợp 2 ancol no đơn chức kế tiếp nhau trong dãy đồng đẳng. Nếu đốt cháy 15,7 gam hỗn hợp T cần dùng vừa hết 21,84 lít O2 và thu được 17,92 lít CO2. Các khí đo ở đktc. Phần trăm khối lượng của X trong hỗn hợp T là:
Hỗn hợp M gồm 3 chất hữu cơ X, Y, Z đều có cùng loại nhóm chức với công thức phân tử tương ứng là CH4O, C2H6O, C3H8O3. Đốt cháy hoàn toàn m gam hỗn hợp M, sau phản ứng thu được 2,24 lít CO2 (ở đktc) và 2,7 gam H2O. Mặt khác, 40 gam M hòa tan được tối đa 9,8 gam Cu(OH)2. Phần trăm khối lượng của X trong M là:
Đốt cháy hoàn toàn 34 gam hổn hợp X gồm CH2(COOH)2 ,CxHyCOOH và HCOOH, rồi hấp thụ hoàn toàn sản phẩm cháy vào dung dịch nước vôi trong (dư) thu được 110 gam kết tủa và khối lượng dung dịch giảm 47,2 gam. Lấy 17 gam X tác dụng hết với dung dịch NaHCO3 (dư), thu được V lít khí CO2 (đktc). Giá trị của V là:
Hòa tan m gam CuSO4.5H2O vào nước thu được dung dịch X. Điện phân (với điện cực trơ, hiệu suất 100%) dung dịch X bằng cường độ dòng điện 1,93A. Nếu thời gian điện phân là t giây, thì thu được 156,8 ml khí (ở đktc) ở anot. Nếu thời gian điện phân là 2t giây, thì tổng thể tích khí thu được ở cả hai điện cực là 537,6 ml (ở đktc). Giá trị của m và t lần lượt là:
Thủy phân hoàn toàn m1 gam este X mạch hở bằng dung dịch NaOH dư, thu được m2 gam ancol Y và 21,6 gam hỗn hợp muối của hai axit cacboxylic đơn chức. Đốt cháy hoàn toàn m2 gam Y bằng lượng vừa đủ 0,35 mol oxi, thu được 0,3 mol CO2 và 0,4 mol H2O. Giá trị của m1 là:
Nhúng thanh Fe có khối lượng m gam vào dung dịch chứa 0,1 mol AgNO3 và 0,15 mol Cu(NO3)2, sau một thời gian, lấy thanh sắt ra, thấy khối lượng thanh sắt tăng 10% và thu được dung dịch Y. Thêm dung dịch HCl dư vào dung dịch Y, thấy thoát ra 1,12 lít khí NO (đktc). Giá trị của m là:
Từ 100 ml rượu 11,50 thực hiện phản ứng lên men giấm, sau một thời gian thu được dung dịch X. Trung hòa 1/10 dung dịch X cần 40 ml dung dịch Ca(OH)2 0,15M. Hiệu suất phản ứng lên men giấm là (biết khối lượng riêng của ancol etylic nguyên chất bằng 0,8 g/ml)