TOP 10 phản ứng hóa học trong cuộc sống hàng ngày
Top 10 phản ứng hóa học Hay trong cuộc sống
10 phản ứng hóa học trong cuộc sống hàng ngày được VnDoc tổng hợp biên soạn là 10 phản ứng hóa học thực tế xảy ra thường xuyên ở xung quanh chúng ta, nhiều khi chúng ta không nhận thấy, mọi thứ xung quanh chúng ta luôn không ngừng biến đổi, các vật chất cũ sẽ tương tác với nhau hình thành nên các chất mới, đó gọi là phản ứng hóa học. Tài liệu dưới đây sẽ đưa ra các phản ứng quen thuộc nhất trong đời sống gần gũi vơi chúng ta nhất. Mời các bạn tham khảo.
1. Quang hợp ở thực vật
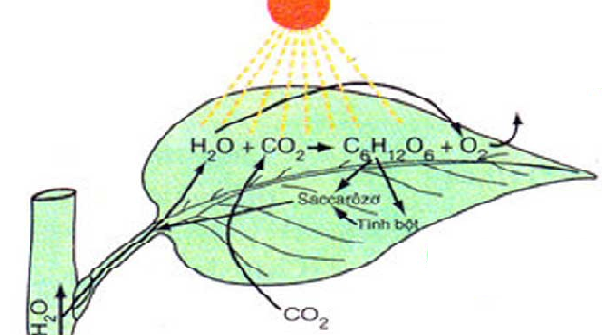
Quang hợp ở thực vật là quá trình sử dụng năng lượng ánh sáng mặt trời đã được diệp lục hấp thụ để tổng hợp cacbohidrat và giải phóng ôxi từ khí cacbonic và nước.
Phương trình tổng quát của quang hợp:
6 CO2 + 12H2O → C6H12O6 + 6O2 + 6H2O
(as MT, dlục)
Toàn bộ sự sống trên hành tinh chúng ta đều phụ thuộc vào quang hợp:
Sản phẩm quang hợp là nguồn chất hữu cơ làm thức ăn cho mọi sinh vật, là nguyên liệu cho công nghiệp và thuốc chữa bệnh cho con người
Cung cấp năng lượng để duy trì hoạt động sống của sinh giới.
Điều hoà không khí: giải phóng oxi và hấp thụ CO2 (góp phần ngăn chặn hiệu ứng nhà kính)
2. Gỉ sắt
a. Gỉ sắt hay rỉ sắt là kết quả của việc kim loại sắt hay hợp kim sắt bị các tác động môi trường gây ra hiện tượng ăn mòn. Nó làm bề mặt của sắt bị biến đổi sang các hợp chất khác kém chất lượng và kém bền hơn sắt nguyên chất. Trong xây dựng, sắt bị gỉ sét gây tác hại khá lớn. Nếu biết được thành phần chính của gỉ sắt bạn sẽ hạn chế được việc xử lý chống thấm dột, đặc biệt là sân thượng và nhà vệ sinh. Bởi sân thượng sẽ bị ảnh hưởng trực tiếp của thời tiết, còn nhà vệ sinh thì thường xuyên tiếp xúc với nước (nhân tố chính gây ra gỉ sắt)

b. Phản ứng hóa học của sắt trong quá trình bị tạo gỉ
Sắt dụng cụ là Fe có lẫn tạp chất (như cacbon cùng một số kim loại và phi kim khác).
Khi tiếp xúc với khí ẩm, có chứa O2, CO2, hơi H2O,…
Fe – 2e → Fe²+ (1)
Các electron sẽ di chuyển sang điện cực khác (như cacbon) phát sinh ra dòng điện, tại đó:
H2O + 1/2O2 +2e → 2OH- (2)
Từ (1) & (2) ta có:
Fe + H2O + 1/2H2O → Fe(OH)2 (kt).
Fe(OH)2 bị oxi hóa tiếp trong không khí ẩm tạo Fe(OH)3.
Fe(OH)3 bị loại nước dần chuyển thành Fe2O3 theo thời gian:
2Fe(OH)3 → Fe2O3 + 3H2O.
Vì gỉ sắt Fe2O3.nH2O xốp, nên quá trình ăn mòn tiếp diễn vào lớp bên trong đến khi toàn bộ khối kim loại đều bị gỉ. Bong từng lớp từng lớp.
3. Phản ứng của xà phòng, các chất tẩy rửa
a. Xà phòng: là hỗn hợp các muối natri hoặc kali của các axit béo. Là sản phẩm của phản ứng xà phòng hóa.
Muối natri của các axit có KLPT nhỏ tan nhiều còn muối natri của các axit có KLPT lớn không tan trong dung dịch natri clorua. Chúng được tách ra gọi là xà phòng tổng hợp. Xà phòng tổng hợp có tính chất giặt rửa tương tự xà phòng thường.
Thành phần của xà phòng và sử dụng xà phòng:
Thành phần chính của xà phòng là các muối natri/kali của axit béo, thường là natri stearat C17H35COONa, natripanmitat C15H31COONa, natrioleat C17H33COONa… Các phụ gia thường gặp là chất màu, chất thơm.
Xà phòng dùng trong tắm gội, giặt giũ…Ưu điểm là không gây hại cho da và môi trường do dễ bị phân hủy bởi vi sinh vật có trong thiên nhiên. Nhược điểm là khi dùng với nước cứng thì các muối canxi stearat, canxi panmitat…sẽ kết tủa làm giảm tác dụng giặt rửa và ảnh hưởng đến chất lượng vải sợi.

b. Chất giặt rửa tổng hợp:
Chất giặt rửa tổng hợp: là chất giặt rửa không phải muối của natri hay kali của các axit béo, nhưng có tính chất giặt rửa tương tự xà phòng, được tổng hợp theo hình mẫu “phân tử xà phòng”, gồm đầu phân cực (ưa nước) gắn với đuôi dài không phân cực (ưa dầu mỡ).
Sản xuất chất giặt rửa tổng hợp:
Chất giặt rửa tổng hợp được điều chế từ các sản phẩm của dầu mỏ.
VD: oxi hóa parafin được axit cacboxylic, hidro hóa axit thu được ancol, cho ancol phản ứng với H2SO4 rồi trung hòa thì được chất giặt rửa loại ankyl sunfat.
Thành phần và sử dụng các chế phẩm từ chất giặt rửa tổng hợp:
Các chế phẩm như bột giặt, kem giặt…. bao gồm các thành phần: chất giặt rửa tổng hợp, các phụ gia chất thơm, chất màu, còn có thể có chất tẩy trắng như natri hipoclorit. Chất này có hại cho da khi giặt bằng tay.
Ưu điểm của chất giặt rửa tổng hợp là dùng được với nước cứng vì chúng ít bị kết tủa bởi ion canxi.
Nhược điểm: Những chất giặt rửa tổng hợp có chứa gốc hidrocacbon phân nhánh gây ô nhiễm môi trường, vì chúng rất khó bị các vi sinh vật phân hủy.
4. Sự cháy

Trong khí (gas) thường dùng có thành phần chính là khí propan (C3H8) và butan (C4H10).
C3H8 + 5O2 → 3CO2 + 4H2O
2C4H10 + 13O2 → 8CO2 + 10H2O
Khi bị đốt cháy, gas luôn cháy hết kể cả trong trường hợp cháy có ngọn lửa đỏ.
Sản phẩm cháy chỉ tạo ra dioxit cacbon (CO2) và hơi nước- những thành phần khác hoàn toàn không độc hại.
Vấn đề nguy hiểm chỉ xảy ra khi dùng bếp gas, bình gas trong phòng kín.
Nếu do sơ suất gas rò rỉ ra ngoài hơi gas sẽ lan truyền, dâng từ dưới lên trên (vì nặng hơn không khí), choán chỗ, đẩy dần không khí ra ngoài, gây ngạt.
Cũng tương tự, khí CO2 sinh ra sau khi gas cháy trong phòng kín, nếu không thông gió thích hợp sẽ tích luỹ dần, làm giảm nồng độ oxy trong không khí.
Do đó, cần tuân thủ nghiêm ngặt các quy định đối với người sử dụng.
5. Phản ứng axit - bazo
Khi ta kết hợp một loại axit (như giấm, chanh) với một bazo (như baking soda, xà phòng), thì ta đang thực hiện một phản ứng axit - bazo. Đây là những phản ứng trung hòa, tạo ra muối và nước.
Ví dụ về phương trình hóa học tổng quát của phản ứng axit-bazo tạo ra kali clorua:
HCl + KOH → KCl + H2O.
6. Bột nở
Bột nở là nguyên liệu quen thuộc mà bất cứ đầu bếp, chuyên gia làm bánh, người nội trợ hay những người yêu thích ẩm thực đều biết đến và thường xuyên sử dụng.
Bột nở (Baking Powder). Thành phần của bột nở gồm có ¼ Baking Soda, được kết hợp với một số loại muối axit, tinh bột ngô ngoài ra có thể hiểu như một loại nguyên liệu sử dụng trong quá trình làm bánh để tạo độ tơi, xốp.

Vì sao trong công nghiệp thực phẩm, muối (NH4)2CO3 được dùng làm bột nở?
(NH4)2CO3 được dùng làm bột nở vì khi trộn thêm vào bột mì, lúc nướng bánh (NH4)2CO3 phân huỷ thành các chất khí và hơi nên làm cho bánh xốp và nở.
(NH4)2CO3 → 2NH3 + CO2 + H2O
7. Quá trình hình thành thạch nhũ trong hang động
Thành phần chính của núi đá vôi là CaCO3. Khi gặp nước mưa và CO2 trong không khí, CaCO3 chuyển hóa thành Ca(HCO3)2 tan trong nước, chảy qua khe đá vào trong hang động. Dần dần Ca(HCO3)2 lại chuyển hóa thành CaCO3 rắn, không tan. Cứ như vậy tạo ra thạch nhũ.
2CaCO3 + H2O + CO2 ⇆ Ca(HCO3)2(dd)

8. Hô hấp kị khí
Hô hấp kị khí lại ngược lại với hô hấp hiếu khí, hô hấp kị khí là một loạt các phản ứng hóa học cho phép tế bào lấy lại năng lượng từ các phân tử phức hợp mà không có oxi. Các tế bào trong cơ thể chúng ta thực hiện hô hấp kị khí bất cứ khi nào mà bạn tiêu hao khí oxi vận chuyển tới chúng, chẳng hạn như lúc lao động cơ bắp trong thời gian dài với cường độ cao.
Hô hấp kị khí diễn ra trong quá trình lên men, sản xuất ê-ta-nol, khí CO2 và các loại hóa chất khác để sản xuất ra pho-mat, rượu, bia, sữa chua, bánh mì và nhiều sản phẩm thông dụng khác.
Phương trình hóa học:
C6H12O6 → 2C2H5OH + 2CO2 + năng lượng.

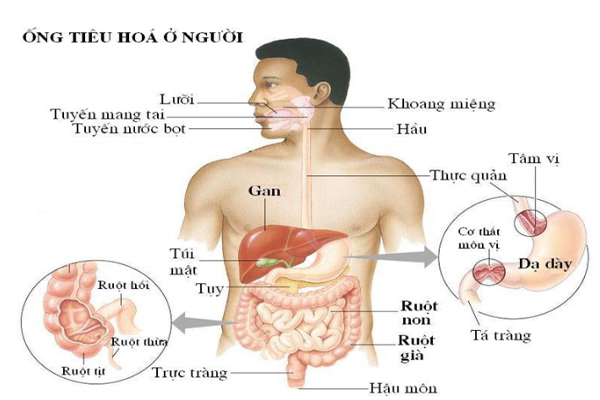
9. Quá trình tiêu hóa
Hàng nghìn phản ứng hóa học xảy ra trong suốt quá trình tiêu hóa. Ngay sau khi bạn đưa thức ăn vào trong miệng, một loại enzym trong nước bọt có tên là amylaza bắt đầu phá vỡ các phân tử đường và các cacbonhydrat thành các phân tử nhỏ hơn cơ thể chúng ta có thể hấp thu. Axit HCl trong dạ dày phản ứng với thức ăn nhằm phá vỡ chúng, đồng thời các enzym cũng bẻ gẫy các liên kết hóa học của các phân tử protein và chất béo, để cơ thể có hấp thụ chúng qua thành ruột ngấm vào máu.
10. Pin
Khi chúng ta sử dụng một dụng cụ điện nào đó có chứa pin thì xảy ra 1 phản ứng hóa học. Đó là phản ứng điện hóa học hay còn gọi là phản ứng oxy hóa – khử để tạo ra điện năng từ năng lượng hóa học. Phản ứng oxy hóa tự nhiên thường xảy ra trong tế bào điện, còn phản ứng nhân tạo thì xảy ra trong bình điện phân.

Trên đây VnDoc đã gửi tới các bạn Top 10 phản ứng hóa học xảy ra trong cuộc sống hằng ngày mà các bạn có thể quan sát thấy.
