Hóa học 11 Cánh Diều bài 1
Theo lộ trình thực hiện Chương trình giáo dục phổ thông 2018 của Bộ Giáo dục và Đào tạo, từ năm học 2023-2024, học sinh các khối lớp 11 sẽ học theo chương trình, sách giáo khoa mới. Để giúp các thầy cô và các em học sinh làm quen với từng bộ sách mới, VnDoc xin giới thiệu tài liệu Hóa học 11 Cánh Diều bài 1. Mời quý bạn đọc cùng tham khảo.
Hóa học 11 Cánh Diều bài 1: Mở đầu về cân bằng hóa học
Mở đầu trang 6 Hoá học 11
Khí NO2 (màu nâu đỏ) liên tục chuyển hoá thành khí N2O4 (không màu) và ngược lại, tại một điều kiện xác định. Tại điều kiện này, khí NO2 cũng như khí N2O4 trong các bình riêng biệt (Hình 1.1), sau một thời gian đều chuyển thành hỗn hợp khí có thành phần như nhau và không đổi theo thời gian.
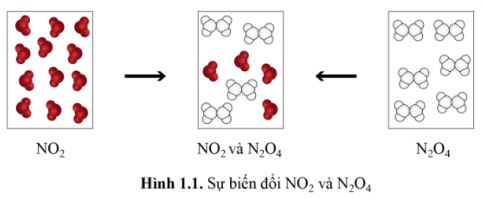
Tại thời điểm hỗn hợp khí trong hai bình có thành phần như nhau, có phản ứng diễn ra trong hai bình này không?
Lời giải:
Tại thời điểm hỗn hợp khí trong hai bình có thành phần như nhau, phản ứng vẫn tiếp diễn trong hai bình.
Tuy nhiên, nồng độ của một chất bất kì trong phản ứng không đổi là do lượng mất đi và lượng sinh ra chất đó là bằng nhau.
I. Khái niệm phản ứng thuận nghịch và trạng thái cân bằng
Câu hỏi 1 trang 7 Hoá học 11
Hãy nêu một số ví dụ về phản ứng thuận nghịch mà em biết.
Lời giải:
Một số ví dụ về phản ứng thuận nghịch:
+ Phản ứng của khí chlorine với nước:
Cl2(aq) + H2O(l) ⇌ HCl(aq) + HClO(aq).
+ Phản ứng hình thành hang động, thạch nhũ trong tự nhiên:
CaCO3(s) + CO2(aq) + H2O(l) ⇌ Ca(HCO3)2(aq)
+ Phản ứng của hơi iodine với khí hydrogen:
H2(g) + I2(g) ⇌ 2HI(g)
Luyện tập 1 trang 7 Hoá học 11
Phản ứng thuận nghịch có xảy ra hoàn toàn được không? Vì sao?
Lời giải:
Phản ứng thuận nghịch xảy ra không hoàn toàn. Do phản ứng thuận nghịch xảy ra đồng thời sự chuyển chất phản ứng thành chất sản phẩm và sự chuyển chất sản phẩm thành chất phản ứng (ở cùng điều kiện).
Câu hỏi 2 trang 7 Hoá học 11
Xét ví dụ 2:
a) Giải thích vì sao màu tím của hỗn hợp khí lại nhạt dần so với lúc mới bắt đầu trộn hai khí H2 và I2 với nhau.
b) Sau một khoảng thời gian, màu tím của hỗn hợp không thay đổi, chứng tỏ nồng độ của chất nào không thay đổi?
Lời giải:
Quá trình trộn khí hydrogen với hơi iodine được thể hiện qua phản ứng thuận nghịch:
H2(g) + I2(g) ⇌ 2HI(g)
a) Tại thời điểm ban đầu, ngay khi vừa mới trộn khí H2 và hơi I2 với nhau, chưa có HI tạo thành, nồng độ H2 và I2 là lớn nhất. Nồng độ của I2 lớn nhất nên màu tím của hỗn hợp là đậm nhất.
Sau khi trộn khí H2 và hơi I2, phản ứng thuận diễn ra và nồng độ H2 và I2 giảm dần nên màu tím của hỗn hợp khí cũng nhạt dần.
b) Sau một khoảng thời gian, màu tím của hỗn hợp không thay đổi, chứng tỏ nồng độ của một chất bất kì trong phản ứng không đổi (do lượng mất đi và lượng sinh ra chất đó là bằng nhau).
Câu hỏi 3 trang 8 Hoá học 11
Cho hai đồ thị (a) và (b) dưới đây. Mỗi đồ thị biểu diễn sự thay đổi tốc độ của phản ứng thuận và tốc độ của phản ứng nghịch theo thời gian.
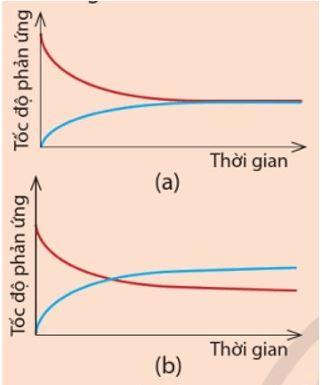
Hãy cho biết đồ thị nào thể hiện đúng Ví dụ 2. Đường màu xanh trong đồ thị đó biểu diễn tốc độ phản ứng thuận hay tốc độ phản ứng nghịch?
Lời giải:
Đồ thị (a) thể hiện đúng Ví dụ 2. Do sau một khoảng thời gian nhất định, tốc độ của phản ứng thuận bằng tốc độ của phản ứng nghịch.
Đường màu xanh trong đồ thị biểu diễn tốc độ phản ứng nghịch. Do sau khi trộn hai khí, phản ứng thuận diễn ra, nồng độ H2 và I2 giảm dần nên vthuận giảm dần. Trong khi đó, lượng HI sinh ra theo phản ứng thuận càng nhiều và nồng độ HI tăng nên vnghịch tăng dần.
Câu hỏi 4 trang 8 Hoá học 11
Vì sao giá trị ![]() \(\frac{k_{t} }{k_{n} }\) là một hằng số ở nhiệt độ xác định?
\(\frac{k_{t} }{k_{n} }\) là một hằng số ở nhiệt độ xác định?
Lời giải:
kt, kn lần lượt là hằng số tốc độ phản ứng thuận, hằng số tốc độ phản ứng nghịch mà giá trị của kt, kn chỉ phụ thuộc vào nhiệt độ và bản chất của các chất tham gia phản ứng, nên tại một nhiệt độ xác định giá trị ktkn là hằng số.
II. Biểu thức hằng số cân bằng và ý nghĩa
Câu hỏi 5 trang 9 Hoá học 11
Viết biểu thức hằng số cân bằng KC cho phản ứng thuận nghịch:
a) N2(g) + 3H2(g) ⇌ 2NH3(g)
b) CaCO3(s) ⇌ CaO(s) + CO2(g)
Lời giải:
a) N2(g) + 3H2(g) ⇌ 2NH3(g)
Biểu thức hằng số cân bằng: ![]() \(K_{C}=\frac{[NH_{3}] ^{2} }{[N_{2}].[H_{2} ]^{3} }\)
\(K_{C}=\frac{[NH_{3}] ^{2} }{[N_{2}].[H_{2} ]^{3} }\)
b) CaCO3(s) ⇌ CaO(s) + CO2(g)
Biểu thức hằng số cân bằng: KC = [CO2]
Câu hỏi 6 trang 9 Hoá học 11
Viết biểu thức hằng số cân bằng KC cho phản ứng (*), (**) dưới đây.
H2(g) + I2(g) ⇌ 2HI(g) (*)
![]() \(\frac{1}{2}\)H2g +
\(\frac{1}{2}\)H2g + ![]() \(\frac{1}{2}\)I2g⇌HIg **
\(\frac{1}{2}\)I2g⇌HIg **
Theo em, giá trị hai hằng số cân bằng này có bằng nhau không?
Lời giải:
H2(g) + I2(g) ⇌ 2HI(g) (*)
Biểu thức hằng số cân bằng cho phản ứng (*): ![]() \(K_{C}=\frac{[HI] ^{2} }{[H_{2}].[I_{2} ]}\)
\(K_{C}=\frac{[HI] ^{2} }{[H_{2}].[I_{2} ]}\)
![]() \(\frac{1}{2}\)H2g +
\(\frac{1}{2}\)H2g + ![]() \(\frac{1}{2}\)I2g⇌HIg **
\(\frac{1}{2}\)I2g⇌HIg **
Biểu thức hằng số cân bằng cho phản ứng (**): ![]() \(K_{C}=\frac{[HI]}{[H_{2}]^{\frac{1}{2} }.[I_{2}] ^{\frac{1}{2} } }\)
\(K_{C}=\frac{[HI]}{[H_{2}]^{\frac{1}{2} }.[I_{2}] ^{\frac{1}{2} } }\)
Theo em, giá trị hai hằng số cân bằng này bằng nhau. Do giá trị KC chỉ phụ thuộc vào bản chất của các chất trong cân bằng và nhiệt độ.
Luyện tập 2 trang 9 Hoá học 11
Trong công nghiệp, halogen được sản xuất từ phản ứng:
CH4(g) + H2O(g) ⇌ 3H2(g) + CO(g)
a) Tính hằng số cân bằng KC của phản ứng trên ở 760 oC.
Biết ở nhiệt độ này, tất cả các chất đều ở thể khí và nồng độ mol của CH4, H2O, H2 và CO ở trạng thái cân bằng lần lượt là 0,126 M; 0,242 M; 1,150 M và 0,126 M.
b*) Ở 760 oC, giả sử ban đầu chỉ có CH4 và H2O có nồng độ bằng nhau và bằng x M. Xác định x, biết nồng độ của H2 ở trạng thái cân bằng là 0,6 M.
Lời giải:
a) Hằng số cân bằng KC của phản ứng ở 760 oC là:
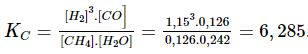
b) Ta có: CH4(g) + H2O(g) ⇌ 3H2(g) + CO(g)
Ban đầu: x x 0 0 M
Phản ứng: 0,2 0,2 0,6 0,2 M
Cân bằng: (x – 0,2) (x – 0,2) 0,6 0,2 M
Do giá trị KC chỉ phụ thuộc vào bản chất của các chất trong cân bằng và nhiệt độ. Nên:
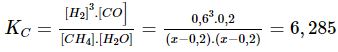
⇒ 0,0432 = 6,285x2 – 2,514x + 0,2514
⇒ 6,285x2 – 2,514x + 0,2082 = 0
⇒ x = 0,283 (thoả mãn); x = 0,12 (loại do 0,12 < 0,2).
Vận dụng 1 trang 10 Hoá học 11
Hãy cho biết trong công nghiệp, để thu được nhiều NH3 hơn thì cần tăng hay giảm nồng độ N2 và H2.
Lời giải:
Biểu thức hằng số cân bằng của phản ứng: N2(g) + 3H2(g) ⇌ 2NH3(g) là:
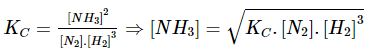
Vậy để thu được nhiều NH3 hơn cần tăng nồng độ của N2 và H2.
Câu hỏi 7 trang 10 Hoá học 11
Hai acid HA và HB cùng nồng độ ban đầu là 0,5 M, phân li trong nước theo các cân bằng:
HA ⇌ H+ + A-
HB ⇌ H+ + B-
Với các hằng số cân bằng (hay gọi là hằng số phân li acid) tương ứng là KC(HA) = 0,2 và KC(HB) = 0,1. Tính nồng độ H+ của mỗi dung dịch acid. Rút ra kết luận về mối liên hệ giữa độ mạnh của acid với độ lớn của hằng số phân li acid. Biết rằng acid càng mạnh khi càng dễ tạo ra H+.
Lời giải:
- Tính nồng độ H+ của dung dịch acid HA:
Ta có: HA ⇌ H+ + A-
Ban đầu: 0,5 0 0 M
Phản ứng: x x x M
Cân bằng: (0,5 – x) x x M
KC(HA) = 0,2 ⇒ ![]() \(x^{2}=\frac{x^{2} }{(0.5-x)}=0.2\)
\(x^{2}=\frac{x^{2} }{(0.5-x)}=0.2\)
⇒ x2 + 0,2x - 0,1 = 0
⇒ x = 0,231 (thoả mãn).
- Tính nồng độ H+ của dung dịch acid HB:
Ta có: HB ⇌ H+ + B-
Ban đầu: 0,5 0 0 M
Phản ứng: y y y M
Cân bằng: (0,5 – y) y y M
KC(HB) = 0,1 ⇒ ![]() \(y^{2}=\frac{y^{2} }{(0.5-y)}=0.1\)
\(y^{2}=\frac{y^{2} }{(0.5-y)}=0.1\)
⇒ y2 + 0,1y – 0,05 = 0
⇒ y = 0,179 (thoả mãn).
Nhận xét:
Hằng số phân li acid càng lớn, acid càng mạnh.
Luyện tập 3 trang 11 Hoá học 11
Methanol (CH3OH) là nguyên liệu quan trọng trong công nghiệp hoá học. Dựa vào hằng số cân bằng của các phản ứng ở 25 oC, hãy lựa chọn phản ứng thích hợp để điều chế CH3OH. Giải thích.
CO(g) + 2H2(g) ⇌ CH3OH(g) KC = 2,26.104 (1)
CO2(g) + 3H2(g) ⇌ CH3OH(g) + H2O(g) KC = 8,27.10-1 (2)
Lời giải:
Phản ứng (1) thích hợp để điều chế CH3OH.
Do phản ứng (1) là phản ứng thuận nghịch có KC = 2,26.104 rất lớn so với 1 nên phản ứng thuận diễn ra thuận lợi hơn rất nhiều so với phản ứng nghịch; các chất ở trạng thái cân bằng chủ yếu là chất sản phẩm.
III. Ảnh hưởng của nhiệt độ, nồng độ và áp suất đến cân bằng hoá học
Thí nghiệm 1 trang 11 Hoá học 11
Chuẩn bị: Ba ống nghiệm (1), (2), (3) chứa NO2 (có màu giống nhau), một cốc nước nóng (70 – 80 oC) và một cốc nước đá.
Tiến hành: Ống nghiệm thứ nhất (1) được để ở nhiệt độ phòng (khoảng 25 oC). Ống nghiệm thứ hai (2) được nhúng vào cốc nước nóng. Ống nghiệm thứ ba (3) được nhúng vào cốc nước đá.
Yêu cầu: Quan sát hiện tượng và giải thích.
Biết NO2 có thể chuyển hoá thành N2O4 theo phản ứng thuận và ngược lại N2O4 có thể chuyển lại thành NO2 theo phản ứng nghịch. Quá trình này được biểu diễn theo phản ứng thuận nghịch sau:
2NO2(g) ⇌ N2O4(g) Δr![]() \(H_{298}^{0}\)=−58 kJ (8)
\(H_{298}^{0}\)=−58 kJ (8)
màu nâu đỏ không màu
Chú ý an toàn: Khí NO2 độc nên tránh hít phải khí NO2. Nên làm thí nghiệm này trong tủ hốt.
Lời giải:
Hiện tượng:
+ Ống nghiệm thứ hai (2) nhúng vào cốc nước nóng, hỗn hợp trong ống nghiệm có màu đậm dần lên.
+ Ống nghiệm thứ ba (3) nhúng vào cốc nước đá, hỗn hợp trong ống nghiệm trở nên nhạt màu hơn.
Giải thích:
2NO2(g) ⇌ N2O4(g)
Δr![]() \(H_{298}^{0}\)= −58 kJ < 0 ⇒ Chiều thuận toả nhiệt.
\(H_{298}^{0}\)= −58 kJ < 0 ⇒ Chiều thuận toả nhiệt.
+ Khi tăng nhiệt độ, cân bằng chuyển dịch theo chiều nghịch (tức chiều phản ứng thu nhiệt) nên hỗn hợp có màu nâu đậm hơn.
+ Khi giảm nhiệt độ, cân bằng chuyển dịch theo chiều thuận (tức chiều phản ứng toả nhiệt) nên hỗn hợp trở nên nhạt màu hơn.
Câu hỏi 8 trang 11 Hoá học 11
Từ Thí nghiệm 1, hãy cho biết:
a) Dựa vào dấu hiệu nào để biết trạng thái cân bằng của phản ứng (8) bị chuyển dịch khi thay đổi nhiệt độ.
b*) Khi tăng nhiệt độ hoặc giảm nhiệt độ, cân bằng chuyển dịch theo chiều thu nhiệt hay toả nhiệt?
Lời giải:
a) Dựa vào màu sắc của khí trong ống nghiệm để biết trạng thái cân bằng của phản ứng bị dịch chuyển khi thay đổi nhiệt độ.
b) Khi tăng nhiệt độ, cân bằng chuyển dịch theo chiều làm giảm nhiệt độ, tức là chiều phản ứng thu nhiệt, nghĩa là chiều làm giảm tác động của việc tăng nhiệt độ.
Khi giảm nhiệt độ, cân bằng chuyển dịch theo chiều làm tăng nhiệt độ, tức là chiều phản ứng toả nhiệt, nghĩa là chiểu làm giảm tác động của việc giảm nhiệt độ.
Thí nghiệm 2 trang 12 Hoá học 11
Chuẩn bị: CH3COONa tinh thể; ống nghiệm, cốc thuỷ tinh.
Tiến hành: Cho một thìa thuỷ tinh tinh thể sodium acetate (CH3COONa) vào ống nghiệm A chứa khoảng 5 mL nước cất, lắc đều cho tan hết, rồi thêm vào ống nghiệm 2 – 3 giọt chất chỉ thị phenolphthalein. Rót khoảng một nửa dung dịch từ ống nghiệm A sang ống nghiệm B, sau đó đặt ống nghiệm B vào một cốc nước nóng (khoảng 70 oC – 80 oC). Sau khoảng 2 phút, quan sát và so sánh màu sắc của dung dịch trong hai ống nghiệm A và B.
Cho biết giữa ion acetate và nước có phản ứng thuận nghịch sau:
CH3COO−+H2O⇌CH3COOH+OH− (9)
Yêu cầu: Thảo luận về chiều chuyển dịch cân bằng trên khi nhiệt độ tăng lên.
Lời giải:
Hiện tượng:
Sau khoảng 2 phút, thấy ống nghiệm B có màu đậm hơn so với ống nghiệm A.
Kết quả thảo luận:
Khi nhiệt độ tăng lên, cân bằng chuyển dịch theo chiều thuận.
Luyện tập 4 trang 12 Hoá học 11
Dựa vào thí nghiệm 2, cho biết khi tăng nhiệt độ thì cân bằng (9) chuyển dịch theo chiều thuận hay chiều nghịch?
Lời giải:
Khi tăng nhiệt độ thì cân bằng (9) chuyển dịch theo chiều thuận tức chiều làm tăng nồng độ OH-, làm màu dung dịch đậm lên.
Luyện tập 5 trang 12 Hoá học 11: Cân bằng sau chuyển dịch theo chiều nào khi tăng nhiệt độ?
2SO2(g) + O2(g) ⇌ 2SO3(g) Δr![]() \(H_{298}^{0}\)= −197,8 kJ.
\(H_{298}^{0}\)= −197,8 kJ.
Lời giải:
Δr![]() \(H_{298}^{0}\)= −197,8 kJ.⇒Chiều thuận toả nhiệt.
\(H_{298}^{0}\)= −197,8 kJ.⇒Chiều thuận toả nhiệt.
Khi tăng nhiệt độ, cân bằng sẽ chuyển dịch theo chiều chống lại sự thay đổi đó, nghĩa là theo chiều giảm nhiệt độ, đó là chiều nghịch (chiều phản ứng thu nhiệt).
Câu hỏi 9 trang 12 Hoá học 11
Cân bằng 2NO2(g) ⇌ N2O4(g) chuyển dịch theo chiều nào khi tăng áp suất của hỗn hợp (bằng cách nén hỗn hợp) ở điều kiện nhiệt độ không đổi. Biết rằng áp suất tỉ lệ với số mol chất khí.
Lời giải:
Khi tăng áp suất của hỗn hợp, cân bằng sẽ chuyển dịch theo chiều chống lại sự thay đổi đó, nghĩa là theo chiều giảm áp suất (hay chính là chiều giảm số mol khí), tức chiều thuận.
Vận dụng 2 trang 13 Hoá học 11
Quá trình tổng hợp NH3 trong công nghiệp từ N2 và H2 nên thực hiện ở áp suất cao hay áp suất thấp? Giải thích. Tìm hiểu thông tin, cho biết phản ứng tổng hợp NH3 ở các nhà máy thường được thực hiện ở áp suất nào.
Lời giải:
Phản ứng tổng hợp NH3 từ N2 và H2:
N2(g) + 3H2(g) ⇌ 2NH3(g)
Dự đoán: Phản ứng nên thực hiện ở áp suất cao, do ở áp suất cao, cân bằng sẽ chuyển dịch theo chiều chống lại sự thay đổi đó, nghĩa là theo chiều giảm áp suất (hay chính là chiều giảm số mol khí), tức chiều thuận (tăng hiệu suất tổng hợp NH3).
Thực tế, phản ứng tổng hợp NH3 ở các nhà máy thường được thực hiện ở áp suất 200 – 300 atm.
Vận dụng 3 trang 13 Hoá học 11
Thành phần chính của tinh dầu chuối là ester CH3COOCH2CH2CH(CH3)2. Để thu được hỗn hợp chất chứa nhiều ester này thì cần thay đổi nồng độ các chất như thế nào trong cân bằng:
CH3COOH(aq) + ROH(aq) ⇌ CH3CHOOR(aq) + H2O(l)
Với R – là (CH3)2CHCH2CH2 –.
Lời giải:
Để nâng cao hiệu suất của phản ứng (tức thu được hỗn hợp chất chứa nhiều ester này) có thể lấy dư một trong hai chất đầu (tăng nồng độ một trong hai chất đầu) hoặc làm giảm nồng độ các sản phẩm.
Bài tập (trang 14)
Bài 1 trang 14 Hoá học 11
Phát biểu nào sau đây về một phản ứng thuận nghịch tại trạng thái cân bằng là không đúng?
A. Tốc độ của phản ứng thuận bằng tốc độ của phản ứng nghịch.
B. Nồng độ của tất cả các chất trong hỗn hợp phản ứng là không đổi.
C. Nồng độ mol của chất phản ứng luôn bằng nồng độ mol của chất sản phẩm phản ứng.
D. Phản ứng thuận và phản ứng nghịch vẫn diễn ra.
Lời giải:
Đáp án đúng là: C
Khi phản ứng thuận nghịch ở trạng thái cân bằng thì:
+ Tốc độ của phản ứng thuận bằng tốc độ của phản ứng nghịch.
+ Nồng độ của tất cả các chất trong hỗn hợp phản ứng là không đổi.
+ Phản ứng thuận và phản ứng nghịch vẫn diễn ra.
Bài 2 trang 14 Hoá học 11
Cho 0,4 mol SO2 và 0,6 mol O2 vào một bình dung tích 1 lít được giữ ở một nhiệt độ không đổi. Phản ứng trong bình xảy ra như sau:
2SO2(g) + O2(g) ⇌ 2SO3(g)
Khi phản ứng đạt đến trạng thái cân bằng, lượng SO3 trong bình là 0,3 mol. Tính hằng số cân bằng KC của phản ứng tổng hợp SO3 ở nhiệt độ trên.
Lời giải:
Do dung tích bình là 1 lít nên giá trị nồng độ bằng giá trị của số mol.
Ta có: 2SO2(g) + O2(g) ⇌ 2SO3(g)
Ban đầu: 0,4 0,6 0 M
Phản ứng: 0,3 0,15 0,3 M
Cân bằng: 0,1 0,45 0,3 M
Hằng số cân bằng KC của phản ứng tổng hợp SO3 là:
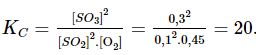
Bài 3 trang 14 Hoá học 11
Nhũ đá được hình thành trong các hang động liên quan đến cân bằng sau đây:
Ca(HCO3)2 (aq) ⇌ CaCO3(s) + CO2(aq) + H2O(l)
Nếu nồng độ CO2 hoà tan trong nước tăng lên thì có thuận lợi cho sự hình thành nhũ đá hay không? Giải thích.
Lời giải:
Nếu nồng độ CO2 hoà tan trong nước tăng lên thì không thuận lợi cho sự hình thành nhũ đá. Do nồng độ CO2 tăng, cân bằng sẽ chuyển dịch theo chiều làm giảm nồng độ CO2, tức chiều nghịch.
-------------------
Trên đây VnDoc.com vừa gửi tới bạn đọc bài viết Hóa học 11 Cánh Diều bài 1. Hi vọng qua bài viết này bạn đọc có thêm tài liệu để học tập tốt hơn môn Hóa học 11 Cánh diều.

