Hóa học 11 Cánh Diều bài 12
Theo lộ trình thực hiện Chương trình giáo dục phổ thông 2018 của Bộ Giáo dục và Đào tạo, từ năm học 2023-2024, học sinh các khối lớp 11 sẽ học theo chương trình, sách giáo khoa mới. Để giúp các thầy cô và các em học sinh làm quen với từng bộ sách mới, VnDoc xin giới thiệu tài liệu Hóa học 11 Cánh Diều bài 12. Mời quý bạn đọc cùng tham khảo.
Hóa học 11 Cánh Diều bài 12: Alkane
Mở đầu trang 72 Hoá học 11
Viết công thức cấu tạo dạng đầy đủ của các hydrocarbon có công thức phân tử là CH4, C2H6 và C3H8. Dự đoán tính chất hoá học của các chất dựa vào đặc điểm liên kết của chúng.
Lời giải:
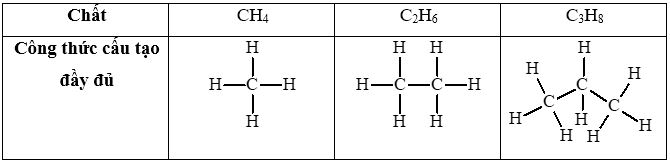
Trong phân tử alkane chỉ có các liên kết σ bền và kém phân cực. Mỗi nguyên tử carbon cũng như hydrogen đã tạo ra số liên kết cộng hoá trị lớn nhất của chúng. Vì thế, các alkane khó tham gia vào các phản ứng hoá học và các phản ứng xảy ra sẽ kèm theo việc thay thế nguyên tử hydrogen hoặc bẻ gẫy mạch carbon.
I. Khái niệm và danh pháp
Câu hỏi 1 trang 73 Hóa học 11
Mô tả hình dạng của phân tử methane và ethane.
Lời giải:
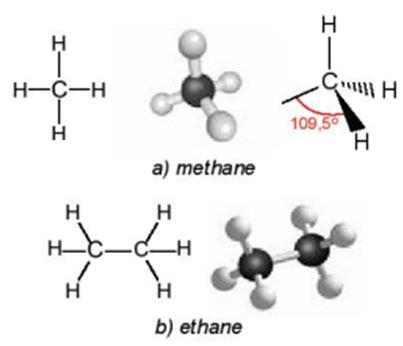
- Trong phân tử methane, bốn liên kết C – H giống nhau tạo với nhau 1 góc 109,5o và hướng về 4 đỉnh của hình tứ diện đều.
- Trong phân tử ethane, mỗi nguyên tử C tạo được 4 liên kết đơn hướng từ nguyên tử C (nằm ở tâm của hình tứ diện) về 4 đỉnh của một tứ diện với góc liên kết khoảng 109,5o.
Câu hỏi 2 trang 74 Hóa học 11
Gọi tên các hợp chất isobutane, isopentane và neopentane theo danh pháp thay thế.
Lời giải:
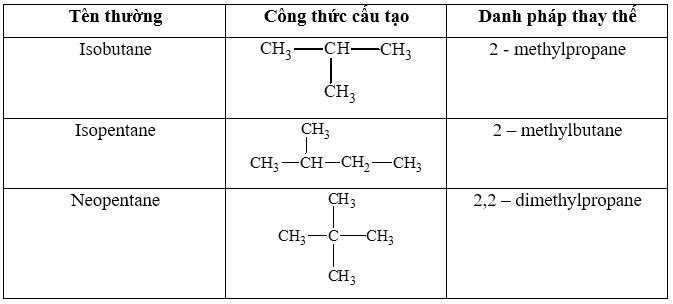
III. Tính chất hoá học
Thí nghiệm 1 trang 76 Hóa học 11
Phản ứng của hexane với bromine
Chuẩn bị: Hexane, nước bromine; ống nghiệm, cốc nước nóng và bông tẩm dung dịch NaOH.
Tiến hành: Cho vào ống nghiệm khô khoảng 1 mL hexane và nhỏ thêm vào ống nghiệm khoảng 1 mL nước bromine. Lắc nhẹ hỗn hợp phản ứng. Nút ống nghiệm bằng bông đã tẩm dung dịch NaOH rồi nhúng ống nghiệm vào trong cốc nước nóng 50 °C (đã chuẩn bị trước) hoặc để ống nghiệm ra nơi có ánh sáng Mặt Trời.
Yêu cầu: Quan sát, nhận xét màu sắc và tính đồng nhất của hỗn hợp phản ứng trước và sau khi đun nóng (hoặc để ra ngoài ánh nắng Mặt Trời).
Chú ý an toàn: Hexane, bromine và hydrogen bromide dễ bay hơi, có mùi xốc, độc.
Lời giải:
Ban đầu ống nghiệm có hai lớp, lớp dưới là bromine màu vàng, lớp trên là hexane không màu.
Sau khi đặt ống nghiệm vào cốc nước nóng, thu được hỗn hợp không có màu.
Thí nghiệm 2 trang 76 Hóa học 11
Tác dụng của potassium permanganate với hexane
Chuẩn bị: Hexane, dung dịch KMnO4 1%; ống nghiệm.
Tiến hành: Cho vào ống nghiệm khoảng 1 mL hexane, thêm tiếp vào ống nghiệm vài giọt dung dịch thuốc tím (KMnO4) 1% và lắc đều.
Yêu cầu: Quan sát, nhận xét màu sắc và tính đồng nhất của hỗn hợp phản ứng.
Lời giải:
Quan sát thấy ống nghiệm có 2 lớp, lớp dưới là dung dịch KMnO4 trong nước màu tím, lớp trên là hexane không màu.
Thí nghiệm 3 trang 78 Hóa học 11
Đốt cháy hexane
Chuẩn bị: Hexane; chén sứ, que đóm dài, diêm hoặc bật lửa.
Tiến hành: Cho khoảng 1 mL hexane vào chén sứ, dùng que đóm dài để châm lửa đốt hexane.
Yêu cầu: Quan sát, nhận xét màu ngọn lửa và viết phương trình hóa học của phản ứng oxi hoá hoàn toàn hexane.
Chú ý an toàn: Hexane bay hơi mạnh, dễ bắt lửa và cháy.
Lời giải:
Hexane bốc cháy cho ngọn lửa màu vàng.
Phương trình hoá học của phản ứng:
C6H14 +![]() \(\frac{19}{2}\)O2
\(\frac{19}{2}\)O2 ![]() \(\overset{t^{0} }{\rightarrow}\) 6CO2 + 7H2O
\(\overset{t^{0} }{\rightarrow}\) 6CO2 + 7H2O
Câu hỏi 3 trang 78 Hóa học 11
Biogas hay khí sinh học là một hỗn hợp khí (chủ yếu là methane, chiếm hơn 60%) được sinh ra từ quá trình phân huỷ kị khí của các phụ phẩm nông nghiệp (chất thải của gia súc, gia cầm, rơm, rạ,...), rác thải hữu cơ,... Mỗi m3 biogas có thể cung cấp năng lượng tương đương với 0,4 kg dầu diesel hoặc 0,6 kg xăng hoặc 0,8 kg than. Cho biết sử dụng biogas mang lại lợi ích gì?
Lời giải:
Sử dụng biogas mang lại các lợi ích:
- Tránh được mầm bệnh cho vật nuôi, tận dụng được nguồn phân bón, thu được khí gas.
- Giải phóng sức lao động cho nội trợ.
- Giữ được môi trường xanh sạch đẹp.
- Tiết kiệm được chi phí hàng tháng.
IV. Nguồn alkane trong tự nhiên, ứng dụng của alkane
Câu hỏi 3 trang 78 Hóa học 11
Biogas hay khí sinh học là một hỗn hợp khí (chủ yếu là methane, chiếm hơn 60%) được sinh ra từ quá trình phân huỷ kị khí của các phụ phẩm nông nghiệp (chất thải của gia súc, gia cầm, rơm, rạ,...), rác thải hữu cơ,... Mỗi m3 biogas có thể cung cấp năng lượng tương đương với 0,4 kg dầu diesel hoặc 0,6 kg xăng hoặc 0,8 kg than. Cho biết sử dụng biogas mang lại lợi ích gì?
Lời giải:
Sử dụng biogas mang lại các lợi ích:
- Tránh được mầm bệnh cho vật nuôi, tận dụng được nguồn phân bón, thu được khí gas.
- Giải phóng sức lao động cho nội trợ.
- Giữ được môi trường xanh sạch đẹp.
- Tiết kiệm được chi phí hàng tháng.
Câu hỏi 4 trang 79 Hóa học 11
Biện pháp nào sau đây không làm giảm ô nhiễm môi trường gây ra do sử dụng nhiên liệu từ dầu mỏ?
A. Đưa thêm hợp chất có chứa chì vào xăng để làm tăng chỉ số octane của xăng.
B. Đưa thêm chất xúc tác vào ống xả động cơ để chuyển hoá các khí thải độc.
C. Tăng cường sử dụng biogas.
D.Tổ chức thu gom và xử lí dầu cặn.
Lời giải:
Đáp án đúng là: A
Biện pháp A không làm giảm ô nhiễm môi trường do lượng chì trong xăng cao là nguyên nhân gây ô nhiễm không khí.
Vận dụng trang 79 Hóa học 11
Hãy đề xuất một số biện pháp góp phần làm giảm ô nhiễm môi trường do các phương tiện giao thông gây ra.
Lời giải:
Một số biện pháp góp phần làm giảm ô nhiễm môi trường do các phương tiện giao thông gây ra:
- Giảm bớt lượng chì (lead) có trong nhiên liệu.
- Tăng hiệu suất đốt cháy nhiên liệu động cơ.
- Đưa thêm chất xúc tác vào ống xả động cơ nhằm tiếp tục chuyển hoá alkane trong khí thải động cơ thành carbon dioxide và nước.
- Trồng nhiều cây xanh.
Bài tập (trang 80)
1. Bài 1 trang 80 Hóa học 11
Viết công thức cấu tạo và gọi tên thay thế của các hydrocarbon có công thức phân tử C5H12.
Lời giải:
CH3 – CH2 – CH2 – CH2 – CH3: pentane.
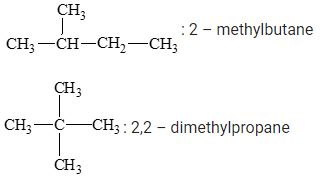
2. Bài 2 trang 80 Hóa học 11
Vì sao không được dùng nước để dập tắt đám cháy xăng, dầu mà phải dùng cát hoặc CO2?
Lời giải:
Không dùng nước để dập các đám cháy xăng, dầu mà phải dùng cát hoặc các bình chứa khí CO2 là vì: xăng, dầu nhẹ hơn nước; khi dùng nước để dập đám cháy thì xăng, dầu sẽ nổi lên trên mặt nước, lan rộng theo nước tràn làm cho đám cháy trở lên mãnh liệt hơn. Còn khi sử dụng cát hoặc bình chứa khí CO2 thì sẽ ngăn cản xăng, dầu tiếp xúc với oxygen không khí làm cho đám cháy bị dập tắt.
3. Bài 3 trang 80 Hóa học 11
Dầu thô có thành phần chính là các hydrocarbon. Người ta có thể phân tách các hydrocarbon có trong dầu thô bằng phương pháp chưng cất phân đoạn. Mỗi phân đoạn gồm một số hydrocarbon có nhiệt độ sôi gần nhau.
a) Vì sao khó thu được hydrocarbon tinh khiết bằng cách chưng cất dầu thô?
b) Undecane (C11H24) là một hydrocarbon mạch dài có trong dầu thô. Undecane có thể bị cracking tạo thành pentane và một alkene. Viết phương trình hoá học của phản ứng xảy ra.
Lời giải:
a) Khó thu được hydrocarbon tinh khiết bằng cách chưng cất dầu thô do trong dầu thô có nhiều hydrocarbon có nhiệt độ sôi gần nhau.
b) Phương trình hoá học:
C11H24 ![]() \(\overset{t^{0}, xt }{\rightarrow}\) C5H12 + C6H12.
\(\overset{t^{0}, xt }{\rightarrow}\) C5H12 + C6H12.
4. Bài 4 trang 80 Hóa học 11
Khí thải của động cơ có thể chứa những chất nào gây ô nhiễm môi trường? Có những giải pháp nào để hạn chế ô nhiễm môi trường do khí thải của động cơ?
Lời giải:
Khí thải của động cơ có thể chứa các chất gây ô nhiễm môi trường như: carbon dioxide; carbon monoxide; các oxide của nitrogen (sinh ra từ phản ứng của oxygen với nitrogen không khí), alkane chưa cháy hết.
Một số giải pháp để hạn chế ô nhiễm môi trường do khí thải của động cơ:
- Giảm bớt lượng chì (lead) có trong nhiên liệu.
- Tăng hiệu suất đốt cháy nhiên liệu động cơ.
- Đưa thêm chất xúc tác vào ống xả động cơ nhằm tiếp tục chuyển hoá alkane trong khí thải động cơ thành carbon dioxide và nước.
- Trồng nhiều cây xanh.
-------------------
Trên đây VnDoc.com vừa gửi tới bạn đọc bài viết Hóa học 11 Cánh Diều bài 12. Hi vọng qua bài viết này bạn đọc có thêm tài liệu để học tập tốt hơn môn Hóa học 11 Cánh diều.

