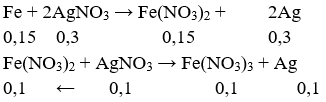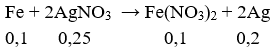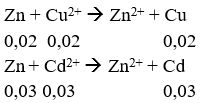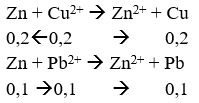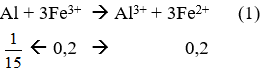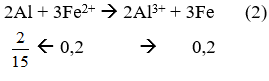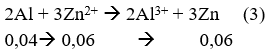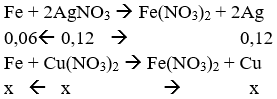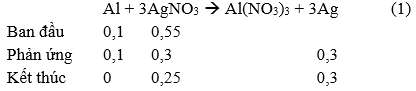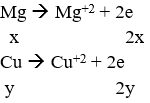1
Hòa tan m gam hỗn hợp T gồm FexOy, Fe và Cu bằng dung dịch chứa 1,8 mol HCl và 0,3 mol HNO3, sau phản ứng thu được 5,824 lít khí NO (đktc, sản phẩm khử duy nhất) và dung dịch X chứa (m + 60,24) chất tan. Cho a gam Mg vào dung dịch X, kết thúc phản ứng thu được (m - 6,04) rắn và hỗn hợp Y gồm hai khí (trong đó có một khí hóa nâu trong không khí) có tỉ khối so với He bằng 4,7. Giá trị của a gần nhất với giá trị nào sau đây?
MY = 18,8 → Y chứa NO (3y) và H2 (2y) → X chứa H+ và NO3- dư.
nNO = 0,26 mol
Bảo toàn khối lượng:
m + 1,8.36,5 + 0,3.63 = m + 60,24 + 0,26.30 + mH2O
→ nH2O = 0,92 mol
Bảo toàn nguyên tố H → nH+ dư = 0,26 mol
Đặt nNH4+ = x
Bảo toàn nguyên tố N → x + 3y + 0,26 = 0,3
nH+, dư = 10x + 4.3y + 2.2y = 0,26
→ x = y = 0,1 mol
Ban đầu: nH+, pư = 0,92.2 = 4nNO + 2.nO (A) → nO (A) = 0,4 mol4
Trong khi cho Mg vào X thu được m – 6,04 > m – 6,4 nên Mg dư.
→ mMg dư = 6,4 - 6,04 = 0,36 gam
Mg + X Dung dịch chứa Mg2+ (p mol), NH4+ (0,01 mol), Cl- (1,8 mol)
Bảo toàn điện tích → p = 0,895 mol
→ mMg bd = 24.0,895 + 0,36 = 21,84 gam
→ Đáp án C