Đề thi học kì 2 môn Hóa học lớp 12 Sở GD&ĐT Bình Thuận năm học 2016 - 2017
Đề thi học kì 2 môn Hóa học lớp 12
Nhằm hỗ trợ các bạn học sinh đang chuẩn bị cho kì thi học kỳ có thêm nhiều tài liệu học tập và luyện thi, chúng tôi xin giới thiệu đến các bạn: Đề thi học kì 2 môn Hóa học lớp 12 Sở GD&ĐT Bình Thuận năm học 2016 - 2017
Tổng hợp đề ôn thi học kì 2 môn Hóa học lớp 12 năm học 2014 - 2015
| SỞ GIÁO DỤC VÀ ĐÀO TẠO BÌNH THUẬN ĐỀ CHÍNH THỨC |
KIỂM TRA HỌC KỲ II - LỚP 12 Năm học: 2016 – 2017. Môn: Hóa Thời gian làm bài: 50 phút (không kể thời gian phát đề) |
Cho nguyên tử khối của các nguyên tố: H = 1; C = 12; N = 14; O = 16; Na = 23; K = 39; Be = 9; Mg = 24; Ca = 40; Ba = 137; Al = 27; Cl = 35,5; Fe = 56; Cu = 64; Zn = 65; Ag = 108; Cr = 52.
Câu 1: Cho dung dịch NaOH đến dư vào dung dịch FeCl2 thấy xuất hiện kết tủa
A. trắng xanh, sau đó chuyển nâu đỏ.
B. keo trắng, sau đó tan dần.
C. keo trắng không tan.
D. nâu đỏ.
Câu 2: Để bảo vệ ống thép (dẫn nước, dẫn dầu, dẫn khí đốt) bằng phương pháp điện hóa, người ta gắn vào mặt ngoài của ống thép những khối kim loại bằng
A. Ag. B. Cu. C. Pb. D. Zn.
Câu 3: Cho từ từ tới dư dung dịch chất X vào dung dịch AlCl3 thu được kết tủa keo trắng. Chất X là
A. HCl. B. NH3. C. NaOH. D. KOH.
Câu 4: Trong công nghiệp, kim loại kiềm và kim loại kiềm thổ được điều chế bằng phương pháp
A. điện phân nóng chảy.
B. điện phân dung dịch.
C. nhiệt luyện.
D. thủy luyện.
Câu 5: Ngâm một lá kẽm trong 100 ml dung dịch AgNO3 0,2M. Khi phản ứng kết thúc, khối lượng lá kẽm tăng thêm
A. 0,65 gam. B. 0,86 gam. C. 1,51 gam. D. 2,16 gam.
Câu 6: Khử hoàn toàn m gam Fe3O4 bằng CO dư ở nhiệt độ cao. Dẫn toàn bộ khí sinh ra vào dung dịch Ca(OH)2 dư, thu được 6 gam kết tủa. Giá trị của m là
A. 9,28. B. 4,64. C. 3,48. D. 13,92.
Câu 7: Để điều chế được 5,2 gam crom từ Cr2O3 bằng phương pháp nhiệt nhôm (giả sử hiệu suất phản ứng 100%) thì khối lượng bột nhôm cần lấy là
A. 5,4 gam. B. 1,8 gam. C. 2,7 gam. D. 3,6 gam.
Câu 8: Phản ứng nào sau đây không đúng?
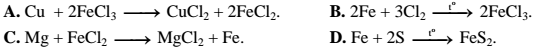
Câu 9: Ở điều kiện thường, kim loại nào sau đây không phản ứng với nước?
A. Ba. B. Be. C. Na. D. K.
Câu 10: Chất tác dụng với dung dịch HNO3 loãng có thể giải phóng khí NO là
A. Fe2O3. B. CaCO3. C. CuO. D. Fe(OH)2.
Câu 11: Chất có thể dùng để làm mềm nước có tính cứng toàn phần là
A. Na3PO4. B. CaCl2. C. HCl. D. NaHSO4.
Câu 12: Cấu hình electron lớp ngoài cùng của nguyên tử kim loại Mg (Z = 12) là
A. 2s22p4. B. 4s2. C. 3s23p1. D. 3s2.
Câu 13: Phản ứng của cặp chất nào sau đây sản phẩm có muối Fe (II)?
A. Fe3O4 + HCl. B. FeO + HNO3. C. Fe(OH)3 + H2SO4. D. FeCO3 + HNO3.
Câu 14: Chất không có tính lưỡng tính là
A. Al(OH)3. B. Al2O3 C. NaHCO3. D. AlCl3.
Câu 15: Dãy các kim loại được xếp theo chiều tính khử tăng dần là
A. Mg, Fe, Al. B. Fe, Al, Mg. C. Al, Mg, Fe. D. Fe, Mg, Al.
Câu 16: Kim loại Ni đều phản ứng được với các dung dịch nào sau đây?
A. MgSO4, CuSO4. B. AgNO3, NaCl. C. NaCl, AlCl3. D. CuSO4, AgNO3.
Câu 17: Dung dịch chất nào sau đây làm quỳ tím hóa xanh?
A. AlCl3. B. Ca(NO3)2 C. K2CO3. D. Na2SO4.
Câu 18: Hòa tan hoàn toàn 8,4 gam Fe bằng dung dịch HNO3 loãng dư, thu được V lít NO (đktc, sản phẩm khử duy nhất). Giá trị của V là
A. 1,12. B. 3,36. C. 2,24. D. 4,48
Câu 19: Chất nào sau đây không tạo kết tủa khi tác dụng với dung dịch Ca(HCO3)2?
A. NaOH. B. HCl. C. Ca(OH)2. D. Na2CO3.
Câu 20: Dung dịch NaOH không tác dụng với
A. AlCl3. B. NaHCO3. C. FeO. D. Al2O3.
Câu 21: Nung hỗn hợp gồm Mg(OH)2 và Fe(OH)2 ngoài không khí cho đến khi khối lượng không đổi thu được chất rắn có thành phần là
A. Mg và FeO. B. MgO và FeO. C. MgO và Fe2O3. D. Mg và Fe.
Câu 22: Hòa tan hoàn toàn 18 gam hỗn hợp gồm Al và Al2O3 trong dung dịch NaOH giải phóng 3,36 lít khí H2 (đktc). Khối lượng của Al2O3 trong hỗn hợp là
A. 15,30 gam. B. 13,95 gam. C. 11,93 gam. D. 10,20 gam.
Câu 23: Phát biểu nào sau đây sai?
A. Quặng hematit có thành phần chính là Fe3O4
B. Nguyên tắc sản xuất gang là khử quặng sắt oxit bằng than cốc trong lò cao.
C. Thành phần % khối lượng cacbon trong gang là từ 2 – 5%.
D. Thép không gỉ có chứa Cr và Ni.
Câu 24: Dãy gồm các chất vừa có tính khử vừa có tính oxi hoá là
A. Fe, Fe3O4. B. FeO, FeCl2. C. Fe, Fe(OH)2. D. FeSO4, Fe2(SO4)3
Câu 25: Hòa tan hoàn toàn x mol Fe vào dung dịch chứa y mol FeCl3 và z mol HCl, thu được dung dịch chỉ chứa một chất tan duy nhất. Biểu thức liên hệ giữa x, y và z là
A. x = y – 2z. B. 2x = y + z.
C. 2x = y + 2z. D. y = 2x.
Câu 26: Cho X, Y, Z, T là các chất khác nhau trong số 4 chất: Ba(HCO3)2, NaOH, AlCl3, KHSO4. Kết quả thí nghiệm của các dung dịch X, Y, Z, T với thuốc thử được ghi ở bảng sau: (dấu – là không có hiện tượng).
|
X |
Y |
Z |
T |
|
|
Quỳ tím |
xanh |
đỏ |
xanh |
đỏ |
|
Dung dịch HCl |
khí thoát ra |
- |
- |
- |
|
Dung dịch Ba(OH)2 dư |
kết tủa trắng |
kết tủa trắng |
- |
kết tủa trắng, sau tan dần |
Nhận xét nào sau đây đúng?
A. X là KHSO4. B. Y là AlCl3. C. Z là NaOH. D. T là Ba(HCO3)2.
Câu 27: Nhỏ từ từ 150 ml dung dịch hỗn hợp gồm K2CO3 0,1M và NaHCO3 0,2M vào 200 ml dung dịch HCl 0,2M và khuấy đều. Sau các phản ứng, thu được V(ml) khí CO2 (đktc). Giá trị của V là
A. 336. B. 560. C. 448. D. 672.
Câu 28: Cho sơ đồ phản ứng ![]()
Hai chất X, Y lần lượt là
A. MgCl2, Cl2. B. HCl, FeCl2. C. FeCl3, Cl2. D. Cl2, HCl.
Câu 29: Đốt nóng hỗn hợp gồm Al và Fe3O4 trong điều kiện không có không khí đến phản ứng hoàn toàn thu được hỗn hợp X. Cho X tác dụng với dung dịch NaOH dư thấy có khí thoát ra. Hỗn hợp X gồm
A. Al, Fe, Fe3O4, Al2O3. B. Al, Fe, Fe2O3, Al2O3.
C. Al, Fe, Al2O3. D. Fe, Fe3O4, Al2O3.
Câu 30: Phát biểu nào sau đây sai?
A. Hợp chất KAl(SO4)2.12H2O dùng làm trong nước được gọi là phèn chua.
B. Ruby và saphia có thành phần hóa học chủ yếu là Al2O3.
C. Nước cứng là nước có chứa các cation Ca2+ và Mg2+.
D. Thạch cao nung dùng để đúc tượng, bó bột... có công thức là CaSO4.H2O.
Câu 31: Điện phân dung dịch chứa hỗn hợp gồm HCl, FeCl3, CuCl2. Thứ tự điện phân ở catot là
A. Fe3+, Cu2+, H+, Fe2+, H2O. B. Cu2+, H+, Fe3+, H2O.
C. Fe3+, Cu2+, H+, H2O. D. Fe3+, Fe2+, Cu2+, H+, H2O.
Câu 32: Cho hỗn hợp gồm Na và Al vào nước (dư). Sau khi phản ứng xảy ra hoàn toàn, thu được khí H2, chất rắn X và dung dịch Y. Y chứa chất nào sau đây?
A. NaOH. B. NaAlO2. C. Al(OH)3. D. NaOH và NaAlO2.
Câu 33: Cho 8,4 gam hỗn hợp hai kim loại kiềm thổ liên tiếp X và Y (MX < MY) tác dụng hết với dung dịch HCl thu được 5,6 lít H2 (đktc). Nhận xét nào sau đây về X và Y không đúng?
A. X có kiểu mạng lục phương.
B. X(OH)2 không tan trong H2O.
C. Ở nhiệt độ thường Y tác dụng với H2O.
D. Thành phần % khối lượng của Y trong hỗn hợp là 28,6%.
Câu 34: Hoà tan hoàn toàn FeO vào dung dịch H2SO4 loãng dư thu được dung dịch X. Phát biểu sai khi nói về dung dịch X là
A. tác dụng được với dung dịch NaNO3. B. làm mất màu thuốc tím.
C. tạo kết tủa với dung dịch NaOH dư. D. có thể hòa tan Cu.
Câu 35: Cho hình vẽ mô tả thí nghiệm điều chế kim loại bằng phương pháp nhiệt luyện:
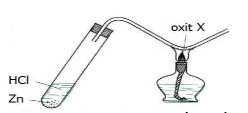
Trong hình vẽ trên, oxit X là
A. CuO. B. Na2O. C. MgO. D. Al2O3.
Câu 36: Cho hỗn hợp gồm Mg và Al (tỉ lệ mol 1:1) tan vừa đủ trong dung dịch gồm HCl; 0,05 mol NaNO3 và 0,1 mol KNO3. Sau khi kết thúc các phản ứng thu được dung dịch X chứa m gam muối; 0,125 mol hỗn hợp khí Y gồm hai khí không màu, trong đó có một khí hóa nâu trong không khí. Tỉ khối của Y so với H2 là 12,2. Giá trị của m gần nhất với giá trị nào sau đây?
A. 50,0. B. 48,6. C. 35,4. D. 47,3.
Câu 37: Khi nhỏ từ từ đến dư dung dịch HCl vào dung dịch hỗn hợp gồm a mol NaOH và b mol NaAlO2, kết quả thí nghiệm được biểu diễn bằng đồ thị sau:
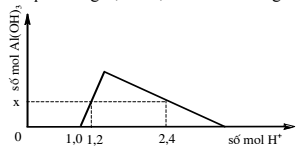
Tổng giá trị a + b là
A. 1,5. B. 0,5. C. 0,7. D. 1,7.
Câu 38: Cho H2 dư qua m gam hỗn hợp chất rắn X gồm Fe, CuO, Fe3O4 nung nóng, phản ứng kết thúc thấy khối lượng chất rắn giảm 0,48 gam. Nếu hòa tan hoàn toàn m gam X vào V(ml) dung dịch HNO3 0,5M vừa đủ thì thu được tối đa 1,344 lít NO (đktc, sản phẩm khử duy nhất). Giá trị của V là
A. 480. B. 720. C. 600. D. 500.
Câu 39: Cho các phát biểu về ứng dụng hóa học và giải pháp thực tế sau:
(a) Khi nhiệt kế bị vỡ có thể dùng bột lưu huỳnh gom thủy ngân bị rơi vãi.
(b) Bảo quản kim loại kiềm cần ngâm chúng trong dầu hỏa.
(c) Dùng hỗn hợp tecmit (Al và Fe2O3) điều chế một lượng nhỏ sắt để hàn đường ray.
(d) Ở điều kiện thường có thể dùng bình bằng sắt chuyên chở axit H2SO4 đặc.
(e) Ngâm đinh sắt vào dung dịch muối Fe2+ để dung dịch không chuyển thành Fe3+. Số phát biểu đúng là
A. 2. B. 5. C. 4. D. 3.
Câu 40: Cho 30 gam hỗn hợp X gồm Fe3O4 và Cu vào dung dịch HCl, sau phản ứng hoàn toàn thu được dung dịch Y chứa hai chất tan và còn lại 6,32 gam chất rắn. Cho dung dịch AgNO3 dư vào dung dịch Y thu được m gam chất rắn. Giá trị của m gần nhất với giá trị nào sau đây?
A. 25,9. B. 91,8. C. 86,2. D. 117,8.
Đáp án đề thi học kì 2 môn Hóa học lớp 12
|
1. A 2. D 3. B 4. A 5. C 6. C 7. C 8. D 9. B 10. D |
11. A 12. D 13. A 14. D 15. B 16. D 17. C 18. B 19. B 20. C |
21. C 22. A 23. A 24. B 25. B 26. C 27. D 28. C 28. C 30. C |
31. A 32. B 33. D 34. D 35. A 36. D 37. A 38. C 39. B 40. D |
