Oxi hóa ethylene bằng dung dịch KMnO4 thu được sản phẩm là
C2H4 KMnO4: Sản phẩm phản ứng ôxi hóa etilen bằng dung dịch thuốc tím là
Oxi hóa etilen bằng dung dịch KMnO4 thu được sản phẩm là gì... Để giúp các bạn học sinh trả lời được câu hỏi này cũng như hiểu hơn về phản ứng Oxi hóa etilen bằng dung dịch KMnO4, VnDoc biên soạn hướng dẫn các bạn viết và xác định được sản phẩm oxi hóa etilen bằng dung dịch thuốc tím ra gì. Thông qua tài liệu này, các em sẽ nắm được Tính chất hóa học của Etilen , phương trình phản ứng C2H4 cộng KMnO4, bên cạnh đó là các dạng câu hỏi bài tập liên quan đến đến etilen, giúp bạn đọc củng cố, rèn luyện kĩ năng thao tác giải bài tập một cách nhanh và chính xác nhất. Mời các bạn tham khảo.
>> Mời các bạn tham khảo thêm một số nội dung liên quan
- Trong phòng thí nghiệm etilen được điều chế bằng cách
- Để làm sạch Etilen có lẫn Axetilen ta cho hỗn hợp đi qua dung dịch nào sau đây
- Trùng hợp etilen sản phẩm thu được có cấu tạo là
- Chất nào sau đây làm mất màu dung dịch KMnO4 ở điều kiện thường
Oxi hoá etilen bằng dung dịch KMnO4 thu được sản phẩm là
A. MnO2, C2H4(OH)2, KOH.
B. K2CO3, H2O, MnO2.
C. C2H5OH, MnO2, KOH.
D. C2H4(OH)2, K2CO3, MnO2.
Đáp án hướng dẫn giải
Đáp án A
Phương trình phản ứng C2H4 cộng KMnO4
3C2H4 + 2KMnO4 + 4H2O → 3C2H4(OH)2 + 2KOH + 2MnO2
Điều kiện phản ứng xảy ra
Điều kiện nhiệt độ, xúc tác Ni
Tính chất hóa học của Etilen
CTCT:
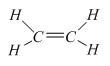
1. Phản ứng cộng
1.1. Phản ứng cộng halogen (phản ứng halogen hóa)
Tác dụng với dung dịch brom (làm đổi màu dung dịch Br, mất màu)
Ở phản ứng này, một liên kết kém bền trong liên kết đôi bị đứt ra và phân tử etilen kết hợp thêm một phân tử brom.
C2H4 + Br2 → C2H4Br2
Phản ứng với clo
CH2 = CH2 + Cl2 → CH2=CH2Cl – HCl
1.2. Phản ứng cộng hidro
C2H4 + H2 → C2H6
1.3. Phản ứng cộng nước (có điều kiện nhiệt độ và sự xúc tác của axit)
C2H4 + H2O → C2H5OH
1.4. Phản ứng cộng axit
- Hiđro halogenua (HCl, HBr, HI), axit sunfuric đậm đặc ,... có thể cộng vào etilen.
CH2=CH2 + HCl (khí) → CH3CH2Cl: (etyl clorua)
CH2=CH2 + H-OSO3H → CH3CH2OSO3H: (etyl hiđrosunfat )
2. Phản ứng cháy
Tác dụng với oxi: Khi đốt trong oxi, etilen cháy tạo thành khí CO2 và H2O, tỏa nhiều nhiệt.
2.1. Phản ứng oxi hóa hoàn toàn
Etilen cháy hoàn toàn tạo ra CO2, H2O và tỏa nhiều nhiệt:
C2H4 + 3O2 → 2CO2 + 2H2O
Khi etilen bị đốt với oxi, etilen và các đồng đẳng đều cháy và tỏa nhiều nhiệt
CnH2n + 3n/2O2 → nCO2 + nH2O
2.2. Phản ứng oxi không hoàn toàn
Etilen làm mất màu dung dịch KMnO4:
Phản ứng làm mất màu dung dịch thuốc tím kali pemanganat được dùng để nhận ra sự có mặt của liên kết đôi của anken.
CH2=CH2 + 4H2O + 2KMnO4 → 3HO-CH2-CH2-OH (etylen glicol)+ 2MnO2 + 2KOH
3. Phản ứng trùng hợp
Khi có xúc tác và nhiệt độ thích hợp, liên kết kém bền trong phân tử etilen bị đứt ra làm cho các phân tử etilen kết hợp với nhau, tạo thành chất có phân tử lượng rất lớn gọi là polietilen. Phản ứng đó gọi là phản ứng trùng hợp.
…+ CH2 = CH2 + CH2 = CH2 +… → … – CH2 – CH2 – CH2 – CH2 – …
Bài tập vận dụng liên quan
Câu 1. Nhận định nào sau đây không đúng với anken?
A. Nhiệt độ sôi giảm dần theo chiều tăng của phân tử khối.
B. Là nguyên liệu cho nhiều quá trình sản xuất hóa học.
C. Từ C2H4 đến C4H8 là chất khí ở điều kiện thường.
D. Nhẹ hơn nước và không tan trong nước.
Câu 2. Nếu chỉ dùng AgNO3 trong dung dịch NH3 dư làm thuốc thử thì phân biệt được
A. but-1-in, etan.
B. but-2-in, etilen.
C. but-1-in, propin.
D. etan, propilen
A đúng vì chỉ có but-1-in tham gia phản ứng tráng bạc, còn etan không tham gia
CH≡C−CH2−CH3 + AgNO3 + NH3 → CAg≡C−CH2−CH3 + NH4NO3
Loại B vì cả but-2-in, etilen đều không phản ứng AgNO3 trong dung dịch NH3 dư
Loại C vì cả but-1-in, propin đều tham gia phản ứng AgNO3 trong dung dịch NH3 dư
CH≡C−CH2−CH3 + AgNO3 + NH3 → CAg≡C−CH2−CH3 + NH4NO3
CH≡C–CH3 + AgNO3 + NH3 → AgC≡C–CH3 + NH4NO3
Loại D vì etan, propilen đều không phản ứng AgNO3 trong dung dịch NH3 dư
Câu 3: Tính chất hóa học nào sau đây không phải của etilen?
A. Etilen cháy tạo thành khí CO2 và H2O, tỏa nhiều nhiệt.
B. Làm mất màu dung dịch brom
C. Tham gia phản ứng thế với halogen
D. Tham gia phản ứng trùng hợp
Câu 4: Khí etilen dễ hóa lỏng hơn metan vì phân tử etilen:
A. Có liên kết π kém bền
B. Phân cực lớn hơn phân tử metan
C. Có cấu tạo phẳng
D. Có khối lượng lớn hơn
Câu 5: Để làm sạch metan có lần etilen người ta cho hỗn hợp đi qua:
A. Khí hidro có Ni, to
B. Dung dịch Brom
C. Dung dịch AgNO3/NH3
D. Khí hidroclorua
Câu 6: Ứng dụng nào sau đây không phải của anken?
A. Sản xuất rượu, các dẫn xuất halogen và các chất khác.
B. Nguyên liệu trùng hợp polime: PE, PVC,…
C. Ứng dụng trong công nghiệp thực phẩm kích thích quả mau chín.
D. Nguyên liệu sản xuất vật liệu silicat, thủy tinh, gốm sứ
Ứng dụng không phải của anken là: Nguyên liệu sản xuất vật liệu silicat, thủy tinh, gốm sứ
Câu 7: Trong công nghiệp, andehit axetic thường được điều chế từ:
A. Axetilen
B. Etilen
C. Ancol etylic
D. Metan
Sử dụng C2H4 ra CH3CHO theo phản ứng sau:
2C2H4 + O2 → 2CH3CHO ( Điều kiện phản ứng: nhiệt độ 450ºC; xúc tác PdCl2/CuCl2/HCl)
Câu 8. Khi dẫn khí etilen vào dung dịch Brom dư đựng trong ống nghiệm có quan sát thấy
A. màu của dung dịch brom nhạt dần, có chất kết tủa
B. màu của dung dịch brom nhạt dần, có chất lỏng không tan chìm xuống đáy ống nghiệm
C. màu của dung dịch brom nhạt dần, có khí thoát ra
D. màu của dung dịch brom không thay đổi
Khi dẫn khí etilen vào dung dịch Brom dư đựng trong ống nghiệm có quan sát thấy màu của dung dịch brom nhạt dần, có chất lỏng không tan chìm xuống đáy ống nghiệm
CH2 = CH2 + Br2 → Br - CH2 - CH2 - Br
.....................................
