Bài tập Khoa học tự nhiên 7 Chương 1
Đây là tài liệu Cao cấp - Chỉ dành cho Thành viên VnDoc ProPlus.
- Tải tất cả tài liệu lớp 7 (Trừ Giáo án, bài giảng)
- Trắc nghiệm không giới hạn
Tổng hợp bài tập Chương 1 Khoa học tự nhiên 7
Bài tập khoa học tự nhiên 7: Nguyên tử- Sơ lược về bảng tuần hoàn các nguyên tố hóa học được VnDoc biên soạn tổng hợp là chuyên đề 1 phân môn Hóa học khoa học tự nhiên 7. Gồm 3 phần:
- Nội dung lý thuyết trọng tâm
- Câu hỏi trắc nghiệm khách quan
- Câu hỏi bài tâp tự luận
Hy vọng thông qua nội dung chuyên đề bạn đọc nắm được các nội dung kiến thức, vận dụng tốt vào giải bài tập, từ đó học tốt môn Khoa học tự nhiên 7 hơn. Sau đây mời các bạn tham khảo chi tiết.
Chuyên đề 1: Nguyên tử Sơ lược về bảng tuần hoàn các nguyên tố hóa học
A. Nội dung lý thuyết trọng tâm
I. Nguyên tử
Nguyên tử là những hạt cực kì nhỏ bé, không mang điện, cấu tạo nên chất.
Ví dụ:
Nước được tạo nên từ các nguyên tử hydrogen và oxygen.
1. Cấu tạo nguyên tử
Nguyên tử được coi như một quả cầu, gồm hạt nhân nguyên tử và vỏ nguyên tử.
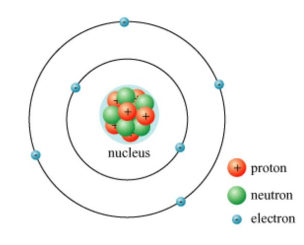
1.1. Vỏ nguyên tử
- Vỏ nguyên tử được tạo bởi một hay nhiểu electron chuyển động xung quanh hạt nhân.
- Electron: kí hiệu: e; mỗi hạt electron mang điện tích -1.
1. 2. Hạt nhân nguyên tử
Vị trí: nằm ở tâm của nguyên tử.
- Kích thước: rất nhỏ so với nguyên tử.
- Thành phần: gồm proton và neutron.
+ Proton: kí hiệu: p; mỗi proton mang điện tích +1.
+ Neutron: kí hiệu: n; không mang điện.
- Điện tích hạt nhân nguyên tử = tổng điện tích các proton.
- Số đơn vị điện tích hạt nhân = số proton.
Ví dụ: Nguyên tử helium gồm hạt nhân có 2 proton, 2 neutron và vỏ nguyên tử có 2 electron.
Điện tích hạt nhân = tổng điện tích các proton = 2.(+1) = +2
Số đơn vị điện tích hạt nhân = số proton = 2
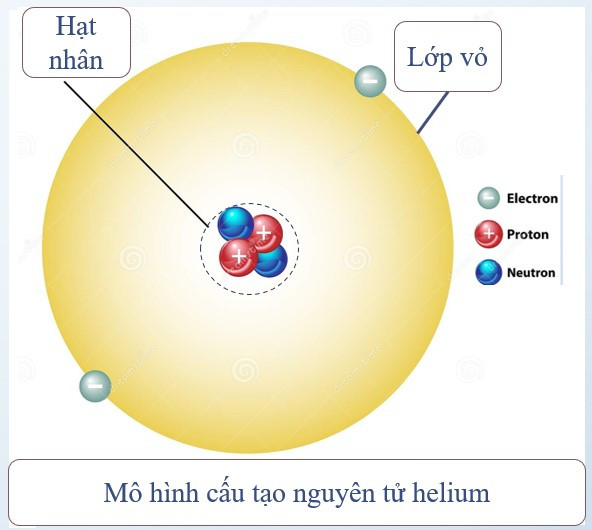
Chú ý:
Số proton = số electron ⇒ Nguyên tử trung hòa về điện
2.2. Sự chuyển động của electron trong nguyên tử
- Mô hình nguyên tử của Rơ-dơ-pho – Bo:
+ Electron chuyển động trên những quỹ đạo xác định xung quanh hạt nhân.
+ Electron phân bố trên các lớp electron theo chiều từ gần hạt nhân ra ngoài.
+ Số electron tối đa trên mỗi lớp được xác định, như lớp thứ nhất có tối đa 2 electron, lớp thứ hai có tối đa 8 electron,…
Ví dụ : Nguyên tử carbon có 6 electron, được phân bố thành hai lớp:
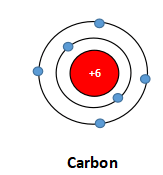
+ Lớp thứ nhất (lớp gần hạt nhân nhất) có 2 electron.
+ Lớp thứ hai có 4 electron.
Ta nói carbon có 4 electron ở lớp ngoài cùng.
3.3. Khối lượng của nguyên tử
- Nguyên tử có khối lượng rất nhỏ. Một gam của bất kì chất nào cũng chứa tới hàng tỉ tỉ nguyên tử.
- Đơn vị đo khối lượng nguyên tử: amu (atomic mass unit)
1 amu = 1,6605. 10-24 g.
- Khối lượng của một nguyên tử = khối lượng của proton + khối lượng của neutron + khối lượng của electron.
Tuy nhiên , do khối lượng của electron (0,00055 amu) rất nhỏ so với khối lượng của proton (1 amu) hay neutron (1 amu).
Nên có thể coi khối lượng của một nguyên tử bằng khối lượng hạt nhân (hay bằng tổng khối lượng của proton và neutron).
Ví dụ:
Nguyên tử sulfur có 16 proton và 16 neutron, nên khối lượng của một nguyên tử sulfur là:
16.1 + 16.1 = 32 (amu)
II. Nguyên tố hóa học
III. Sơ lược bảng tuần hoàn các nguyên tố hóa học
>> Xem tiếp nội dung lý thuyết trong FILE tải về <<
B. Câu hỏi trắc nghiệm khách quan
Bài 1. Nguyên tử
Câu 1. Các hạt cấu tạo nên hạt nhân của hầu hết các nguyên tử là:
| A. electron và neutron | B. electron, proton và neutron |
| C. electron và proton | D. proton và neutron |
Câu 2. Các hạt tạo nên hầu hết nguyên tử là:
| A. electron và neutron | B. proton và neutron |
| C. electron và proton | D. electron, proton và neutron |
Câu 3. Hạt cấu tạo nên vỏ nguyên tử là
| A. electron | B. proton và neutron |
| C. Proton | D. neutron |
Câu 4. Trong hạt nhân nguyên tử, hạt mang điện là
| A. electron | B. proton |
| C. neutron và proton | D. proton và electron |
Câu 5. Hạt mang điện âm trong nguyên tử là:
| A. electron | B. proton |
| C. neutron | D. proton và electron |
Câu 6 . Hạt mang điện dương trong nguyên tử là:
| A. electron | B. proton |
| C. neutron | D. proton và electron |
Câu 7. Nguyên tử luôn trung hòa về điện nên:
A. số hạt proton = số hạt neutron
B. số hạt proton = số hạt electron
C. số hạt electron = số hạt neutron
D. số hạt proton = số hạt electron = số hạt neutron
Câu 8. Khối lượng của nguyên tử bằng
A. tổng khối lượng các hạt proton, hạt neutron và hạt electron
B. tổng khối lượng các hạt proton và hạt neutron
C. tổng khối lượng các hạt proton và hạt electron
D. tổng khối lượng các hạt neutron và hạt electron
Bài 2: Nguyên tố hóa học
Câu 1. Nguyên tố hóa học nào dưới đây được kí hiệu bằng 2 chữ cái
|
A. Neon |
B. Nitrogen |
C. Iodine |
D. Phosphorus |
Câu 2. Kí hiệu nào sau đúng nguyên tố hóa học Aluminium
|
A. Ar |
B. Al |
C. A |
D. Au |
Câu 3. Nguyên tố hoá học là những nguyên tử có cùng
|
A. số khối. |
B. số neutron |
|
C. số proton. |
D. số neutron và số proton. |
Câu 4. Nguyên tố hóa học có nhiều nhất trong vũ trụ là
|
A. Nitrogen |
B. Oxygen |
C. Helium |
D. Hydrogen |
Câu 5. Nguyên tố phổ biến nhất trong vỏ Trái Đất là
|
A. Nitrogen |
B. Oxygen |
C. Silicon |
D. Iron |
Câu 6. Điền từ phù hợp vào chỗ trống: " Số ..... là số đặc trưng của một nguyên tố hóa học"
|
A. electron |
B. Proton |
C. Neutron |
D. Neutro và electron |
Bài 3: Sơ lược về bảng tuần hoàn các nguyên tố hóa học
Câu 1. Nguyên tố X có số thứ tự 15 trong bảng tuần hoàn. Nguyên tố đó ở chu kì
A. 1
B. 2
C. 3
D. 4
Câu 2. Nguyên tố X tạo nên chất khí duy trì sự hô hấp của con người và có nhiều trong không khí. Tên của nguyên tố X
A. Oxygen
B. Nitrogen
C. Helium
D. Hydrogen
Câu 3. Nguyên tố X nằm ở chu kì 2, nhóm VA trong bảng tuần hoàn. X là nguyên tố
A. Phosphorus
B. Sulfur
C. Nitrogen
D. Chlorine
Câu 4. Nguyên tử của nguyên tố X có 3 lớp electron, lớp electron ngoài cùng có 2 electron. Vị trí của nguyên tố X là
A. Thuộc chu kỳ 3, nhóm VIA
B. Thuộc chu kỳ 3, nhóm IIA
C. Thuộc chu kỳ 2, nhóm IIIA
D. Thuộc chu kỳ 2, nhóm VIA
Câu 5. Tính chất của nguyên tố bromine gần giống với tính chất của nguyên tố nào trong các nguyên tố sau đây?
A. Chlorine
B. Phosphorus
C. Nitrogen
D. Oxygen
Câu 6. Biết vị trí của nguyên tố X như sau: chu kì 2, nhóm VIA. Số lớp electron lớp ngoài cùng của nguyên tử X lần lượt là
A. 4 và 2
B. 2 và 6
C. 6 và 2
D. 2 và 4
C. Câu hỏi bài tập tự luận
Câu 1. Tổng số hạt proton, neutron, electron của nguyên tố X là 40, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 12. Xác định số p, n, e của X và vẽ sơ đồ cấu tạo của nguyên tử nguyên tố X
Câu 2.
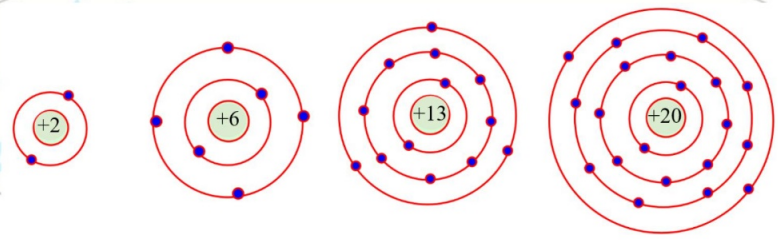
Dựa vào sơ đồ trên hãy hoàn thành bảng sau:
|
|
Số proton |
Số electron |
Số lớp electron |
Số e lớp ngoài cùng |
|
Helium |
|
|
|
|
|
Carbon |
|
|
|
|
|
Aluminium |
|
|
|
|
|
Calcium |
|
|
|
>> Chi tiết chuyên đề mời bạn đọc ấn vào FILE TẢI VỀ miễn phí bên dưới <<
----------------------------------

