Dung dịch nào sau đây có pH >7
Dung dịch nào sau đây có pH lớn hơn 7
Dung dịch nào sau đây có pH >7 được VnDoc biên soạn hướng dẫn bạn đọc trả lời câu hỏi liên quan đến độ pH của dung dịch các chất cũng như hiểu pH là gì, pH > 7 là gì, và ở mỗi giá trị pH là môi trường gì?. Mời các bạn cùng theo dõi bài viết dưới đây.
Dung dịch nào sau đây có pH > 7?
A. KOH.
B. H2SO4.
C. BaCl2.
D. HCl.
Đáp án hướng dẫn giải chi tiết
A. KOH là dung dịch bazo nên có pH >7
B, D. H2SO4 và HCl là axit nên có pH < 7
C. BaCl2 là muối trung tính nên có pH = 7
pH là gì?
Để đánh giá độ axitv và độ kiềm của dung dịch bằng nồng độ H+. Nhưng dung dịch thường dùng có nồng độ H+ nhỏ. Để tránh ghi nồng độ H+ với số mũ âm, người ta dùng giá trị pH với quy ước như sau:
[H+] = 10-pH M.
Nếu [H+] = 10-a M => pH = a
Ví dụ:
[H+] = 1,0.10-2M => pH = 2: môi trường axit
[H+] = 1,0.10-7M => pH = 7: môi trường trung tính
[H+] = 1,0.10-10M => pH = 10: môi trường kiềm
Thang pH thường có giá trị từ 1 đến 14
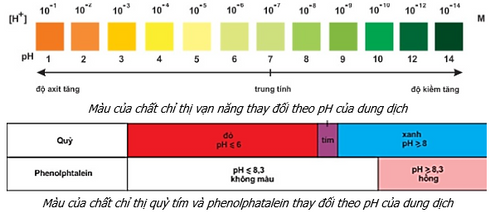
Lưu ý:
Cách xác định môi trường của một muối:
+ Muối được tạo bởi axit mạnh và bazơ yếu thì có môi trường axit, pH < 7
+ Muối được tạo bởi axit yếu và bazơ mạnh thì có môi trường bazo, pH > 7
+ Muối được tạo bởi axit mạnh và bazơ mạnh thì có môi trường trung tính, pH = 7
Bài tập vận dụng liên quan
Câu 1. Dãy nào sau đây gồm các muối axit?
A. NaHSO4, NaHSO3, K2HPO3, KHCO3.
B. KHS, NaHS, KH2PO3, NaH2PO4.
C. NaHS, KHS, Na2HPO3, Na2HPO4.
D. NaHCO3, KHSO3, K3PO4, NaH2PO4.
Muối axit là muối mà H trong anion gốc axit có khả năng phân li ra ion H+.
A. Sai vì K2HPO3 là muối trung hòa, dù còn H trong muối nhưng H này không thể phân li ra H+ được.
C. Sai vì Na2HPO3 là muối trung hòa.
D. Sai vì K3PO4 là muối trung hòa
Câu 2. Dãy chất nào sau đây chỉ gồm các muối trung hòa?
A. NaCl, MgSO4, Fe(NO3)3.
B. NaHCO3, MgCO3, BaCO3.
C. NaOH, ZnCl2, FeCl2.
D. NaCl, HNO3, BaSO4.
Muối trung hoà: Là muối mà gốc axit không có nguyên tử hiđro có thể thay thế bằng nguyên tử kim loại.
=> Dãy gồm các muối trung hòa là: NaCl, MgSO4, Fe(NO3)3.
Loại B vì NaHCO3 là muối axit
Loại C vì NaOH là bazơ, không phải muối
Loại D vì HNO3 là axit, không phải muối
Câu 3. Dãy gồm toàn muối trung hòa là?
A. NaOH, NaCl, Na2SO4
B. Zn(NO3)2, FeS, CuSO3
C. NaHS, K3PO4, KCl
D. H2SO4, NaCl, BaCO3
Muối trung hoà: Là muối mà gốc axit không có nguyên tử hiđro có thể thay thế bằng nguyên tử kim loại.
Nên dãy các chất thỏa mãn: Zn(NO3)2, FeS, CuSO3
Loại các đáp án khác vì:
+) NaHS: muối axit
+) H2SO4: axit
+) NaOH: bazơ
Câu 4. Dung dịch nào sau đây có pH < 7?
A. KOH
B. Na2SO4
C. HNO3
D. Ba(OH)2
Dung dịch nào sau đây có pH < 7?
Loại A vì KOH là bazo do đó pH >7
Loại B vì Na2SO4 được ra từ bazo mạnh NaOH và axit mạnh H2SO4 do đó có môi trường trung hòa => pH = 7
Đúng C vì HNO3 là axit mạnh => pH < 7
Loại D vì Ba(OH)2 là bazo mạnh => pH > 7
Câu 5. Dung dịch muối nào sau đây có pH = 7?
A. Al2(SO4)3
B. NH4Cl
C. KNO3
D. Tất cả 3 dung dịch trên
Dung dịch muối nào sau đây có pH = 7?
Loại A vì Al2(SO4)3 được tạo ra từ bazo yếu Al(OH)3 và axit mạnh H2SO4 => có môi trường axit => pH < 7
Loại B NH4Cl vifcos môi trường axit pH < 7
Đúng C vì KNO3 được ra từ bazo mạnh KOH và axit mạnh HNO3 do đó có môi trường trung hòa => pH = 7
Câu 6. Muối nào sau đây khi thuỷ phân tạo dung dịch có pH < 7?
A. BaCl2.
B. CH3COOK.
C. NaCl.
D. NH4NO3.
Cách xác định MT của một dung dịch muối:
+ Muối tạo bởi axit mạnh và bazo yếu => MT axit (pH < 7)
+ Muối tạo bởi axit yếu và bazo mạnh => MT kiềm (pH > 7)
+ Muối tạo bởi axit mạnh và bazo mạnh => MT trung tính (pH = 7)
NH4NO3 là muối tạo bởi bazo yếu (NH3) và axit mạnh (HNO3)
=> Thủy phân trong nước tạo môi trường axit (pH < 7)
Câu 7. Dung dịch muối nào sau đây có pH > 7 ?
A. NaNO3.
B. Na2CO3.
C. Ba(NO3)2.
D. NH4Cl.
Câu 8. Chất nào sau đây khi cho vào nước không làm thay đổi độ pH của dung dịch?
A. Na2CO3.
B. Na2SO4.
C. HCl.
D. NH4Cl.
A. Na2CO3 được tạo bởi bazơ mạnh NaOH và axit yếu H2CO3 => môi trường bazơ => làm pH tăng
B. Na2SO4 được tạo bởi bazơ mạnh NaOH và axit mạnh H2SO4 => môi trường trung tính => không làm thay đổi pH
C. HCl có môi trường axit => làm pH giảm
D. NH4Cl được tạo bởi bazơ yếu NH3 và axit mạnh HCl => môi trường axit => làm pH giảm
Câu 9. Chọn phát biểu đúng trong số các phát biểu sau đây?
A. Giá trị pH tăng thì độ axit giảm
B. Giá trị pH tăng thì độ axit tăng
C. Dung dịch có pH < 7 làm quỳ tím hoá xanh
D. Dung dịch có pH > 7 làm quỳ tím hoá đỏ
A đúng vì pH tăng thì nồng độ OH- trong dung dịch tăng => độ axit giảm
C. pH < 7 là môi trường axit => quỳ hóa đỏ
D. pH > 7 là môi trường bazơ => quỳ hóa xanh
Câu 10. Cho các dung dịch sau: NaHSO4, AlCl3, Na2SO4, K2S, Ca(NO3)2. Số dung dịch có pH < 7 là
A. 1.
B. 2.
C. 3.
D. 4
NaHSO4 có khả năng phân li H+ ⟹ Môi trường axit ⟹ pH < 7.
+ AlCl3 là muối của bazơ yếu Al(OH)3 và axit mạnh HCl ⟹ Môi trường axit ⟹ pH < 7.
+ Na2SO4 là muối của bazơ mạnh NaOH và axit mạnh H2SO4 ⟹ Môi trường trung tính ⟹ pH = 7.
+ K2S là muối của bazo mạnh KOH và axit yếu H2S ⟹ Môi trường kiềm ⟹ pH > 7.
+ Ca(NO3)2 là muối của bazo mạnh Ca(OH)2 và axit mạnh HNO3 ⟹ Môi trường trung tính ⟹ pH = 7.
Câu 11. Có các lọ đựng hóa chất riêng rẽ: Na2S, NaCl, AgNO3, Na2CO3. Hóa chất nào sau đây có thể sử dụng để phân biệt các dung dịch đó?
A. dung dịch NaOH.
B. dung dịch H2SO4.
C. dung dịch HCl.
D. phenolphtalein.
Sử dụng dung dịch HCl để nhận biết 4 hóa chất trên
Trích mẫu thử và đánh số thứ tự
CHo dung dịch HCl vào 4 ống nghiệm đựng sẵn hóa chất
Mẫu ống nghiệm nào xuất hiện kết tủa trắng thì hóa chất ban đầu là AgNO3
AgNO3 + HCl → AgCl↓ + HNO3
Mẫu thử nào xuất hiện khí mùi trứng thối thì hóa chất ban đầu là Na2S
Na2S + 2HCl → 2NaCl + H2S
Mẫu thử nào xuất hiện khí không màu bay ra là Na2CO3
Na2CO3 + 2HCl → 2NaCl + CO2 + H2O
Mẫu thử còn lại không có hiện tượng gì
Câu 12. Cho sơ đồ sau: muối A + HCl → muối B + H2S. Dãy các chất nào sau đây có thể là A?
A. BaS, FeS, PbS, K2S.
B. KHS, Ag2S, FeS, Na2S.
C. Na2S, CuS, FeS, MgS.
D. NaHS, ZnS, FeS, MgS.
+ Loại A: Tan trong nước và tan trong axit mạnh sinh ra khí H2S gồm Na2S, K2S, CaS và BaS, (NH4)2S.
Na2S + 2HCl → 2NaCl + H2S↑
+ Loại B: Không tan trong nước nhưng tan trong axit mạnh gồm FeS, ZnS...
ZnS + 2H2SO4 → ZnSO4 + H2S↑
+ Loại C: Không tan trong nước và không tan trong axit gồm CuS, PbS, HgS, Ag2S...
Câu 13. Cho ba dung dịch có cùng giá trị pH, các dung dịch được sắp xếp theo thứ tự nồng độ mol tăng dần là:
A. NH3, NaOH, Ba(OH)2
B. NH3, Ba(OH)2, NaOH
C. NaOH, NH3, Ba(OH)2
D. Ba(OH)2, NaOH, NH3
pH bằng nhau => nồng độ mol ion OH- trong các dung dịch bằng nhau
Phương trình phân li:
Ba(OH)2 → 2OH-
NaOH → OH-
NH3 +H2O ⇔ NH4+ + OH-
Mà [OH-] bằng nhau => [Ba(OH)2]< [NaOH] < [NH3]
Câu 14. Dãy chất nào sau đây có môi trường bazơ (pH > 7)?
A. Na2CO3, NaOH, NH4NO3, Na2S.
B. Na2CO3, NH4NO3, KOH, Ba(OH)2.
C. Na2CO3, Na2S, NaClO, NaOH.
D. LiOH, NaOH, Ba(OH)2, HNO3.
A, B loại NH4NO3 vì được tạo bởi bazo yếu (NH3) và axit mạnh (HNO3) nên có MT axit
D loại HNO3
Câu 15. Chất nào dưới đây vừa phản ứng được với dung dịch HCl vừa phản ứng được với dung dịch NaOH?
A. Na2CO3
B. NH4Cl
C. NH3
D. NaHCO3
Chất vừa phản ứng được với dung dịch HCl vừa phản ứng được với dung dịch NaOH là NaHCO3
Câu 16. Trộn 10g dung dịch HCl 7,3% với 20g dung dịch H2SO4 4,9% rồi thêm nước để được 100ml dung dịch A. Tính pH của dung dịch A.
A. 0,4
B. 1
C. 2
D. 3
Số mol HCl là nHCl = (10.7,3)/(100.36,5) = 0,02 mol
Số mol H2SO4 là nH2SO4 = (20.4,9)/(100.98) = 0,01 mol
Phương trình điện ly: HCl → H+ + Cl-
0,02 → 0,02 mol
H2SO4 → 2H+ + SO42-
0,01 → 0,02 mol
Tổng số mol H+ là nH+ = 0,02 + 0,02 = 0,04 mol
CM(H+) = 0,04/0,1 = 0,4 M ⇒ pH = 0,4
.............................
