Đề thi Hóa học kì 2 lớp 10 năm 2020 - Đề số 3
Trắc nghiệm hóa học kì 2 lớp 10 có đáp án - Đề số 3
Đề thi Hóa học kì 2 lớp 10 năm 2020 - Đề số 3 được VnDoc biên soạn gửi tới các bạn là đề thi học kì 2 Hóa học 10 nội dung câu hỏi bám sát nội dung ôn tập Hóa học 10. Gồm các mức độ câu hỏi khác nhau, giúp đánh giá năng lực học tập cũng như củng cố, luyện tập các câu hỏi lý thuyết, dạng bài tập để chuẩn bị tốt cho kì thi tới.
- Đề thi Hóa học kì 2 lớp 10 năm 2020 - Đề số 4
- Đề thi lớp 10 cuối kì 2 năm 2020 môn Hóa học (số 1)
- Đề thi lớp 10 cuối kì 2 năm 2020 môn Hóa học (số 2)
- Ôn tập Hóa học 10 kì 2 năm 2019 - 2020
ĐỀ KIỂM TRA CUỐI KÌ 2 MÔN HÓA HỌC LỚP 10
Bản quyền thuộc về VnDoc nghiêm cấm mọi hành vi sao chép vì mục đích thương mại
(Cho Fe = 56; Na = 23; Ca = 40; Mg = 24; Mn = 55; Cu = 64; Al = 27, Zn = 65, S = 32, O = 16; Cl = 35,5; Ag = 108; H = 1)
Câu 1. Trong các nhóm chất nào dưới đây, số oxi hóa của Lưu huỳnh đều là +6
A. H2S, H2SO3, H2SO4
B. K2S, Na2SO3, Na2SO4
C. SO2, SO3, Ba2SO3
D. H2SO4, H2S2O7, CuSO4
Câu 2. Kim loại nào dưới đây bị thụ động với axit H2SO4 đặc nguội
A. Cu, Fe
B. Cr, Zn
C. Fe, Cr
D. Cu, Al
Câu 3. Dãy nào được xếp đúng thứ tự tính axit và tính khử tăng dần?
A. HCl, HBr, HI, HF.
B. HI, HBr, HCl, HF.
C. HCl, HI, HBr, HF.
D. HF, HCl, HBr, HI.
Câu 4. Khi phản ứng thuận nghịch ở trạng thái cân bằng thì nó:
A. Không xảy ra nữa
B. Vẫn tiếp tục xảy ra
C. Chỉ xảy ra theo chiều thuận
D. Chỉ xảy ra theo chiều nghịch
Câu 5. Sục 6,72 lít khí SO2 (đktc) vào dung dịch Br2 dư rồi cho dung dịch thu được phản ứng với dung dịch BaCl2 dư thu được kết tủa có khối lượng
A. 66,9 gam
B. 23,3 gam
C. 34,95 gam
D. 46,6 gam
Câu 6. Sục khí ozon vào dung dịch KI có nhỏ sẵn vài giọt hồ tinh bột, hiện tượng quan sát thấy được là:
A. Dung dịch có màu tím
B. Dung dịch có màu vàng nhạt
C. Dung dịch trong suốt
D. Dung dịch có màu xanh
Câu 7. Dùng loại bình nào sau đây để đựng dung dịch HF?
A. Bình thuỷ tinh màu xanh.
B. Bình thuỷ tinh mầu nâu.
C. Bình thuỷ tinh không màu.
D. Bình nhựa teflon (chất dẻo).
Câu 8. Cho sơ đồ chuyển hóa:
Fe3O4 + dung dịch HI (dư) ![]() \(\overset{}{\rightarrow}\) X + Y + H2O
\(\overset{}{\rightarrow}\) X + Y + H2O
Biết X và Y là sản phẩm cuối cùng của quá trình chuyển hóa. Các chất X và Y là:
A. Fe và I2.
B. FeI3 và FeI2.
C. FeI2 và I2.
D. FeI3 và I2.
Câu 9. Hòa tan 5,6 lít SO2 (đktc) vào 100 ml dung dịch KOH 3,5M. Dung dịch tạo thành có chứa:
A. K2SO3
B. K2SO3, KHSO3
C. KHSO3
D. K2SO3, KOH dư
Câu 10. Cho 11 gam hỗn Al, Fe tác dụng với dung dịch H2SO4 đậm đặc nóng dư thì được 10,08 lít khí SO2 (đktc). Phần trăm khối lượng Al trong hỗn hợp ban đầu là:
A. 38%
B. 49,1 %
C. 50,9%
D. 62%
Câu 11. Cho phản ứng: 2NH3 + 3Cl2 ![]() \(\rightarrow\) N2 + 6HCl. Trong đó Cl2 đóng vai trò là:
\(\rightarrow\) N2 + 6HCl. Trong đó Cl2 đóng vai trò là:
A. Chất khử.
B. Vừa là chất oxi hoá vừa là chất khử.
C. Chất oxi hoá.
D. Không phải là chất khử hoặc chất oxi hoá.
Câu 12. Trong các phản ứng sau đây, hãy chỉ ra phản ứng không đúng?
A. H2S + 2NaCl ![]() \(\rightarrow\) Na2S + 2HCl.
\(\rightarrow\) Na2S + 2HCl.
B. 2H2S + 3O2 ![]() \(\overset{}{\rightarrow}\) 2SO2 + 2H2O.
\(\overset{}{\rightarrow}\) 2SO2 + 2H2O.
C. H2S + Pb(NO3)2 ![]() \(\rightarrow\) PbS + 2HNO3.
\(\rightarrow\) PbS + 2HNO3.
D. H2S + 4H2O + 4Br2 ![]() \(\rightarrow\) H2SO4 + 8HBr.
\(\rightarrow\) H2SO4 + 8HBr.
Câu 13. Cho FeS tác dụng với dung dịch H2SO4 loãng, thu được khí A; nếu dùng dung dịch H2SO4 đặc, nóng thì thu được khí B. Dẫn khí B vào dung dịch A thu được rắn C. Các chất A, B, C lần lượt là:
A. H2, H2S, S.
B. H2S, SO2, S.
C. H2, SO2, S.
D. O2, SO2, SO3.
Câu 14. Thể tích khí thu được sau phản ứng khi cho 4,8 gam đồng tác dụng với axit H2SO4 đặc nóng
A. 1,68 lít
B. 2,24 lít
C. 3,36 lít
D. 1,12 lít
Câu 15. 14,5 gam hỗn hơp Mg, Fe, Zn tác dụng vừa đủ với dung dịch H2SO4 loãng thấy thoát ra 6,72 lít khí H2 (đktc). Sau phản ứng cô cạn thu được khối lượng muối khan là:
A. 34,3 gam
B. 43,3 gam
C. 33,4 gam
A. 33,8 gam
Câu 16. Cho 10 gam dung dịch HCl tác dụng với dung dịch AgNO3 dư thu dược 14,35 gam kết tủa. Tính nồng độ % dung dịch HCl phản ứng là:
A. 50%
B. 15%
C. 35%
D. 36,5%
Câu 17. Đối với các phản ứng có chất khí tham gia, khi tăng áp suất, tốc độ phản ứng tăng là do
A. Nồng độ của các chất khí tăng lên.
B. Nồng độ của các chất khí giảm xuống.
C. Chuyển động của các chất khí tăng lên.
D. Nồng độ của các chất khí không thay đổi.
Câu 18. Hòa tan hoàn toàn 13 gam kim loại A có hóa trị II vào H2SO4 loãng thu được 4,48 lít H2 (đktc). Kim loại A là:
A. Mg
B. Zn
C. Cu
D. Fe
Câu 19. Khi tăng thêm 10oC, tốc độ phản ứng hóa học tăng lên 3 lần. Để tốc độ phản ứng đó (đang tiến hành ở 30oC) tăng 81 lần thì cần phải tăng nhiệt độ lên đến
A. 70oC
B. 80oC
C. 50oC
D. 60oC
Câu 20. Tổng hệ số cân bằng trong phản ứng hóa học sau:
FeO + H2SO4 → Fe2(SO4)3 + SO2 + H2SO4
A. 11
B. 12
C. 13
D. 14
Câu 21. Những phản ứng nào sau đây chứng minh tính oxi hóa của ozon mạnh hơn oxi?
(1) O3 + Ag
(2) O3 + KI + H2O
(3) O3 + Fe
(4) O3 + CH4
A. 1, 2.
B. 2, 3.
C. 2, 4.
D. 3, 4.
Câu 22. Để a gam bột sắt ngoài không khí,sau một thời gian sẽ chuyển thành hỗn hợp A có khối lượng 37,6 gam gồm Fe, FeO, Fe2O3, Fe3O4. Cho hỗn hợp A phản ứng hết với dung dịch H2SO4 đặc nóng thu được 3,36 lít khí SO2 (đktc). Giá trị a là:
A. 11,2 gam
B. 8,4 gam
C. 56 gam
D. 28 gam
Câu 23. Để loại bỏ SO2 ra khỏi CO2 có thể:
A. Cho hỗn hợp khí qua dung dịch nước vôi trong
B. Cho hỗn hợp khí qua dung dịch Na2CO3
C. Cho hỗn hợp khí qua dung dịch nước Br2 dư
D. Cho hỗn hợp qua dung dịch NaOH
Câu 24. Khi cho cùng một lượng nhôm vào cốc đựng dung dịch axit HCl 0,1M, tốc độ phản ứng sẽ lớn nhất khi dùng nhôm ở dạng nào sau đây?
A. Dạng viên nhỏ.
B. Dạng bột mịn, khuấy đều.
C. Dạng tấm mỏng.
D. Dạng nhôm dây.
Câu 25. Trộn 3,42 muối sunfat của kim loại hóa III với 8 gam Fe2(SO4)3. Cho hỗn hợp tác dụng vừa đủ với 100ml dung dịch BaCl2 tạo thành 20,97 g kết tủa trắng. Nồng độ mol/l của dung dịch BaCl2 và tên kim loại đó là
A. 0,54M; Cr
B. 0,65M; Al
C. 0,9M; Al
D. 0,4M; Cr
ĐÁP ÁN ĐỀ KIỂM TRA CUỐI KÌ 2 MÔN HÓA HỌC LỚP 10
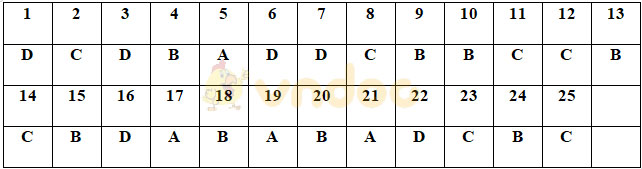
Đây là Đề thi Hóa học kì 2 lớp 10 năm 2020 - Đề số 3 được biên tập theo cấu trúc giống với đề thi hóa 10 học kì 2, bao gồm 25 câu hỏi trắc nghiệm, tóm tắt toàn bộ kiến thức đã được học trong chương trình Hóa học 10 kì 2, kèm theo đáp án. Qua đó sẽ giúp các bạn học sinh củng cố và ôn tập, để chuẩn bị cho kì thi học kì 2 Hóa học.
Trên đây VnDoc đã giới thiệu Đề thi Hóa học kì 2 lớp 10 năm 2020 - Đề số 3 tới các bạn. Để có kết quả học tập tốt và hiệu quả hơn, VnDoc xin giới thiệu tới các bạn học sinh tài liệu Giải bài tập Hóa học 10, Chuyên đề Vật Lí 10, Giải sách bài tập Sinh học 10. Tài liệu học tập lớp 10 mà VnDoc tổng hợp biên soạn và đăng tải.
Ngoài ra, VnDoc.com đã thành lập group chia sẻ tài liệu học tập THPT miễn phí trên Facebook, mời bạn đọc tham gia nhóm Tài liệu học tập lớp 10 để có thể cập nhật thêm nhiều tài liệu mới nhất.
