Giải SBT Khoa học tự nhiên 9 Bài 24: Alkene
Giải SBT KHTN 9 Bài 24: Alkene
Giải SBT KHTN 9 Bài 24: Alkene hướng dẫn trả lời câu hỏi trong sách bài tập Khoa học tự nhiên 9 Kết nối tri thức, giúp các em học sinh củng cố kiến thức được học môn KHTN Bài 24. Sau đây mời các bạn tham khảo.
24.1
CTCT nào sau đây biểu diễn chất thuộc alkene?
A. CH2 = CH – CH3 B. CH ≡ C – CH3
C. CH3 – CH2 – CH3 D. CH2 = CH – CH = CH2.
Hướng dẫn giải:
CH2 = CH – CH3 thuộc loại alkene.
24.2
Phát biểu nào sau đây đúng?
A. Chất có CTPT dạng CnH2n là alkene.
B. Alkene là hydrocarbon mạch hở có một liên kết C = C.
C. Alkene không làm mất màu dung dịch KMnO4.
D. Alkene tác dụng với Br2 trong dung dịch theo tỉ lệ mol 1:2.
Hướng dẫn giải:
A sai, CTPT dạng CnH2n (n≥2).
B đúng
C sai, alkene làm mất màu dung dịch KMnO4.
D sai, alkene tác dụng với Br2 theo tỉ lệ mol 1:2.
Đáp án B
24.3
Khi đốt cháy hoàn toàn một lượng alkene, các sản phẩm cháy có mỗi liên hệ với nhau như thế nào?
A. Số mol CO2 lớn hơn số mol H2O.
B. Số mol CO2 nhỏ hơn số mol H2O.
C. Số mol CO2 bằng số mol H2O.
D. Không có mối liên kết giữa số mol hai sản phẩm.
Hướng dẫn giải:
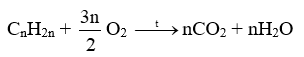
Ta thấy: n CO2 = n H2O.
Đáp án C
24.4
Ethylene không có phản ứng nào sau đây?
A. Tác dụng với NaOH
B. Tác dụng với H2 (xúc tác Ni, đun nóng)
C. Làm nhạt màu dung dịch Br2
D. Cháy trong không khí.
Hướng dẫn giải:
Ethylene không tác dụng với NaOH.
Đáp án A
24.5
Đốt cháy hoàn toàn 1 mol alkene X, thu được CO2 và H2O với tổng khối lượng 310g. CTPT của X là
A. C2H4
B. C4H8
C. C5H10
D. C3H6
Hướng dẫn giải:
Gọi n CO2 = n H2O = a mol
Ta có: m CO2 + m H2O = a.44 + a.18 = 310g
=> a = 5 mol
Số nguyên tử C là: 5 : 1 = 5
Số nguyên tử H là: 5.2 : 1 = 10.
Công thức phân tử là C5H10.
Đáp án C
24.6
Viết PTHH dưới dạng phân tử minh họa tính chất hóa học của alkene C4H8.
Hướng dẫn giải:
C4H8 + 6O2 ![]() \(\to\)4CO2 + 4H2O
\(\to\)4CO2 + 4H2O
C4H8 + Br2 ![]() \(\to\) C4H8Br2
\(\to\) C4H8Br2
24.7
Có hai bình giống nhau, một bình chứa khí methane, một bình chứa khí ethylene. Hãy nêu cách nhận biết mỗi bình bằng phương pháp hóa học.
Hướng dẫn giải:
Dẫn khí của 2 bình chứa khí vào dung dịch nước bromine.
Bình chứa khí ethylene làm mất màu nước bromine, bình chứa khí methane không có hiện tượng.
24.8
Một hỗn hợp khí Y gồm methane và ethylene, biết Y có tỉ khối so với hydrogen bằng 10. Đốt cháy hoàn toàn 6g Y, hấp thụ toàn bộ sản phẩm cháy vào nước vôi trong dư, thu được m gam kết tủa.
a) Xác định thành phần hỗn hợp Y.
b) Tính giá trị của m.
Hướng dẫn giải:
Y có tỉ khối so với hydrogen bằng 10 ![]() \(\to\)M Y = 10.2 = 20
\(\to\)M Y = 10.2 = 20
n Y = 6 : 20 = 0,3 mol
Gọi số mol của methane và ethylene lần lượt là a và b mol:
Ta có: a + b = 0,3 mol (1)
16a + 28b = 6g (2)
Từ (1) và (2) ta có: a = 0,2 mol; b = 0,1 mol
a) %n CH4 = ![]() \(\frac{{0,2}}{{0,3}}.100\%\) =
\(\frac{{0,2}}{{0,3}}.100\%\) = ![]() \(66,67\%\)
\(66,67\%\)
%n C2H4 = 33,33%
PTHH:
CH4 + 2O2 ![]() \(\to\)CO2 + 2H2O
\(\to\)CO2 + 2H2O
0,2 ![]() \(\to\)0,2
\(\to\)0,2
C2H4 + O2 ![]() \(\to\)2CO2 + 2H2O
\(\to\)2CO2 + 2H2O
0,1 ![]() \(\to\)0,2
\(\to\)0,2
Số mol CO2 thu được là: 0,2 + 0,2 = 0,4 mol
Khi dẫn sản phẩm cháy vào nước vôi trong thu được kết tủa:
CO2 + Ca(OH)2 ![]() \(\to\)CaCO3 + H2O
\(\to\)CaCO3 + H2O
0,4 0,4
m CaCO3 = 0,4.100 = 40g

