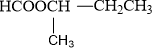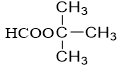Tổng hợp kiến thức hóa 12 học kì 1 Đầy đủ Chi tiết


Lý thuyết hóa 12 học kì 1
Tổng hợp kiến thức hóa 12 học kì 1 Đầy đủ Chi tiết được VnDoc biên soạn tổng hợp là toàn bộ nội dung ôn tập hóa 12 học kì 1, kèm theo các câu hỏi trắc nghiệm sau mỗi chương giúp các bạn củng cố luyện tập, chuẩn bị tốt cho các kì thi quạn trọng.
Tổng hợp kiến thức hóa 12 học kì 1
Một số kiến thức ôn tập trước khi vào bài este
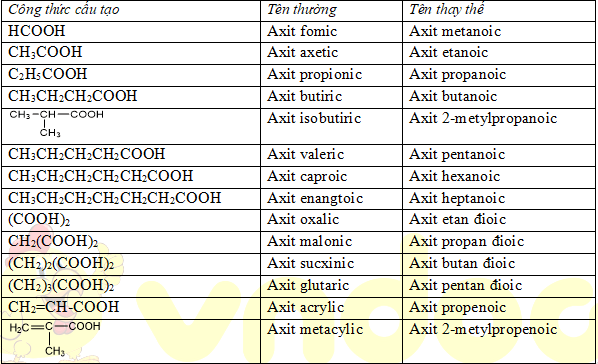
Bảng 1: Tên gọi của 1 số axit thường gặp
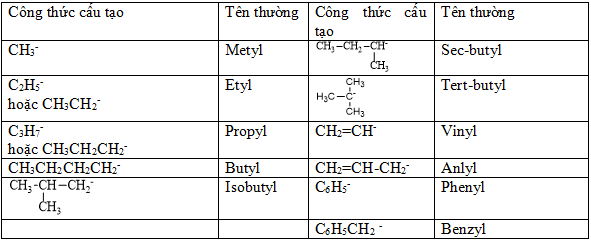
 Bảng 2: Tên gọi của 1 số gốc thường gặp
Bảng 2: Tên gọi của 1 số gốc thường gặp
 CHƯƠNG I : ESTE – LIPIT
CHƯƠNG I : ESTE – LIPIT
BÀI 1 : ESTE
I/ Khái niệm: Khi thay thế nhóm OH- trong phân tử axit cacboxylic bằng nhóm OR’ của phân tử ancol, ta thu được este.
Ví dụ: CH3COOH + C2H5OH CH3COOC2H5 + H2O
Tổng quát RCOOH + R’OH RCOOR’ + H2O
II/ Đồng phân, danh pháp:
RCOOR’ (R là H hoặc gốc hiđrocacbon , R’ là gốc hiđrocacbon )
Cách gọi: “Tên gốc hiđrocacbon R’ + tên anion gốc axit (gọi theo tên thường của axit, đuôi ic => at )”
1/ Este no, đơn chức, mạch hở:
CnH2nO2 (n ≥ 2) hoặc CnH2n+1COOCmH2m+1 (n ≥ 0 , m ≥ 1)
- n = 2: C2H4O2 (1 este) HCOOCH3: metyl fomiat (metyl fomat)
- n = 3: C3H6O2 (2 este) HCOOC2H5: etyl fomat và CH3COOCH3: metyl axetat
- n = 4: C4H8O2 (4 este)
| HCOOCH2CH2CH3 propyl fomat |
isopropyl fomat |
CH3COOC2H5 etyl axetat |
C2H5COOCH3 metyl propionat |
n = 5 : C5H10O2 (9 este)
|
HCOOCH2CH2CH2CH3 butyl fomat |
sec-butyl fomat |
isobutyl fomat |
|
tert-butyl fomat |
CH3COOCH2CH2CH3 propyl axetat |
ispropyl axetat |
|
C2H5COOCH2CH3 metyl propionat |
CH3CH2CH2COOCH3 metyl butirat |
metyl isobutirat |
2/ Este không no, đơn chức, mạch hở, 1 nối đôi C=C: CnH2n-2O2 (n ≥ 3)
+ n = 3: C3H4O2 (1 este) HCOOCH=CH2: vinyl fomat
+ n = 4: C4H6O2 (5 este)
Ngoài ra, este C4H6O4 còn đồng phân 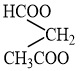
và este C5H8O4 còn đồng phân 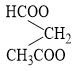 không thuộc hai dạng phân loại ở trên.
không thuộc hai dạng phân loại ở trên.
III/ Tính chất vật lí:
Các este là chất lỏng hoặc rắn ở điều kiện thường.
Các este có mùi thơm đặc trưng: isoamyl axetat CH3COOCH2CH2CH(CH3)2 có mùi chuối chín, etyl butirat CH3CH2CH2COOC2H5 và etyl propionat CH3CH2COOC2H5 có mùi dứa, geranyl axetat có mùi hoa hồng, benzyl axetat CH3COOCH2C6H5 có mùi hoa nhài....
Không tan trong nước, nhẹ hơn nước. Thường có t0 sôi và độ tan trong nước thấp hơn hẳn các axit và ancol cùng số cacbon hoặc cùng phân tử khối (nguyên nhân: không tạo được liên kết hiđrô giữa este với nước và este với nhau).
IV/ Tính chất hóa học:
1/ Phản ứng thủy phân: (phản ứng đặc trưng của este)
a/ Thủy phân trong môi trường axit:
Ví dụ: CH3COOC2H5 + H2O CH3COOH + C2H5OH
Tổng quát: RCOOR’ + H2O RCOOH + R’OH
Đặc điểm: phản ứng thuận nghịch (2 chiều), cần xúc tác là H2SO4 và nhiệt độ cao.
(vì phản ứng thuận nghịch nên este vẫn còn dư và tạo thành hai chất lỏng → tách lớp )
b/ Thủy phân trong môi trường kiềm: (phản ứng xà phòng hóa)
Ví dụ: CH3COOC2H5 + NaOH CH3COONa + C2H5OH
Tổng quát: RCOOR’ + NaOH RCOONa + R’OH
Đặc điểm: phản ứng 1 chiều (không thuận nghịch) , xảy ra ở nhiệt độ cao.
(vì phản ứng 1 chiều nên este hết → sản phẩm đồng nhất )
(**) Một số phản ứng đặc biệt:
c/ Este có dạng anđêhit: RCOOCH=CH-R’ (R và R’ là H hoặc các gốc hiđrôcacbon)
- Khi thủy phân trong môi trường axit: sinh ra axit và anđêhit
Ví dụ: CH3COOCH=CH2 + H2O CH3COOH + CH3CHO
- Khi thủy phân trong môi trường bazơ: sinh ra muối và anđêhit
Ví dụ: HCOOCH=CH-CH3 + NaOH HCOONa + CH3CH2CHO
d/ Este đơn chức của phenol: cộng NaOH hoặc KOH tỉ lệ 1:2, sản phẩm tạo 2 muối và nước.
RCOOC6H4R’ + 2NaOH → RCOONa + R’C6H4ONa + H2O
Ví dụ: CH3COOC6H5 + 2NaOH → CH3COONa + C6H5ONa + H2O
HCOOC6H4CH3 + 2NaOH → HCOONa + CH3C6H4ONa + H2O
e/ Este tráng bạc: có dạng HCOOR (R bất kì)
f/ Phản ứng ở gốc hiđrôcacbon: các este không no có phản ứng ở gốc hiđrôcacbon (phản ứng cộng dung dịch Br2, phản ứng trùng hợp ...)
g/ Phản ứng cháy: este no đơn hở CnH2nO2 + O2 nCO2 + nH2O
V/ Điều chế:
- Các este thường được điều chế bằng cách đun sôi hỗn hợp ancol và axit cacboxylic, có mặt H2SO4 đặc làm xúc tác (phản ứng este hóa)
RCOOH + R’OH RCOOR’ + H2O
- Một số este có phương pháp điều chế riêng:
Vinyl axetat: CH3COOH + CH≡CH CH3COOCH=CH2
Este của phenol: C6H5OH + (CH3CO)2O → CH3COOC6H5 + CH3COOH
Anhidrit axetic phenyl axetat
VI/ Ứng dụng:
Do có khả năng hòa tan tốt nhiều chất nên một số este được dùng làm dung môi để tách, chiết chất hữu cơ (etyl axetat), pha sơn (butyl axetat).
Một số polime của este được dùng làm chất dẻo: poli (vinyl axetat), poli (metyl metacrylat)...
Một số este có mùi thơm, không độc, được dùng làm chất tạo hương trong công nghiệp thực phẩm (benzyl fomat, etyl fomat,... ), mĩ phẩm (linalyl axetat, geranyl axetat,...)
...........
BÀI TẬP
Câu 1: Chất thuộc loại đisaccarit là
A. glucozơ.
B. saccarozơ.
C. xenlulozơ.
D. fructozơ.
Câu 2: Hai chất đồng phân của nhau là
A. glucozơ và mantozơ.
B. fructozơ và glucozơ.
C. fructozơ và mantozơ.
D. saccarozơ và glucozơ
Câu 3: Trong điều kiện thích hợp glucozơ lên men tạo thành khí CO2 và
A. C2H5OH.
B. CH3COOH.
C. HCOOH.
D. CH3CHO.
Câu 4: Saccarozơ và glucozơ đều có
A. phản ứng với AgNO3 trong dung dịch NH3, đun nóng.
B. phản ứng với dung dịch NaCl.
C. phản ứng với Cu(OH)2 ở nhiệt độ thường tạo thành dung dịch xanh lam.
D. phản ứng thuỷ phân trong môi trường axit.
Câu 5: Cho sơ đồ chuyển hoá:
Glucozơ → X → Y → CH3COOH. Hai chất X, Y lần lượt là
A. CH3CHO và CH3CH2OH.
B. CH3CH2OH và CH3CHO.
C. CH3CH(OH)COOH và CH3CHO.
D. CH3CH2OH và CH2=CH2.
Câu 6: Chất tham gia phản ứng tráng gương là
A. xenlulozơ.
B. tinh bột.
C. fructozơ.
D. saccarozơ.
Câu 7: Để chứng minh trong phân tử của glucozơ có nhiều nhóm hiđroxyl, người ta cho dung dịch glucozơ phản ứng với
A. Cu(OH)2 trong NaOH, đun nóng.
B. AgNO3 trong dung dịch NH3, đun nóng.
C. Cu(OH)2 ở nhiệt độ thường.
D. kim loại Na.
Câu 8: Khi lên men 360 gam glucozơ với hiệu suất 100%, khối lượng ancol etylic thu được là
A. 184 gam.
B. 276 gam.
C. 92 gam.
D. 138 gam.
Câu 9: Đun nóng dung dịch chứa 27 gam glucozơ với AgNO3 trong dung dịch NH3 (dư) thì khối lượng Ag tối đa thu được là
A. 16,2 gam.
B. 10,8 gam.
C. 21,6 gam.
D. 32,4 gam.
Câu 10: Lượng glucozơ cần dùng để tạo ra 1,82 gam sobitol với hiệu suất 80% là
A. 2,25 gam.
B. 1,80 gam.
C. 1,82 gam.
D. 1,44 gam.
Câu 11: Cho sơ đồ chuyển hóa sau: Tinh bột → X → Y → axit axetic. X và Y lần lượt là
A. ancol etylic, anđehit axetic.
B. glucozơ, ancol etylic.
C. glucozơ, etyl axetat.
D. glucozơ, anđehit axetic.
Câu 12: Cho dãy các chất: glucozơ, xenlulozơ, saccarozơ, tinh bột, fructozơ. Số chất trong dãy tham gia phản ứng tráng gương là
A. 3.
B. 4.
C. 2.
D. 5.
Câu 13: Thuốc thử để phân biệt glucozơ và fructozơ là
A. Cu(OH)2
B. dung dịch brom.
C. [Ag(NH3)2] NO3
D. Na
Câu 14: Đun nóng 37,5 gam dung dịch glucozơ với lượng AgNO3/dung dịch NH3 dư, thu được 6,48 gam bạc. Nồng độ % của dung dịch glucozơ là
A. 11,4 %
B. 14,4 %
C. 13,4 %
D. 12,4 %
Câu 15: Phân tử khối trung bình của xenlulozơ là 1620 000. Giá trị n trong công thức (C6H10O5)n là
A. 10000
B. 8000
C. 9000
D. 7000
...................................
Để xem và tải toàn bộ tài liệu Tổng hợp kiến thức hóa 12 học kì 1 Đầy đủ Chi tiết mời các bạn ấn link TẢI VỀ phía dưới.
Trên đây VnDoc đã gửi tới bạn đọc Tổng hợp kiến thức hóa 12 học kì 1 Đầy đủ Chi tiết. Nội dung tài liệu bám sát lý thuyết hóa 12 hữu cơ, kèm theo các ví dụ minh họa giúp bạn đọc dễ dàng theo dõi. Các bạn có thể các em cùng tham khảo thêm một số tài liệu liên quan hữu ích trong quá trình học tập như: Giải bài tập Hóa 12, Giải bài tập Toán lớp 12, Giải bài tập Vật Lí 12 ,....
Ngoài ra, VnDoc.com đã thành lập group chia sẻ tài liệu ôn tập THPT Quốc gia miễn phí trên Facebook: Quyết tâm đỗ Đại Học Mời các bạn học sinh tham gia nhóm, để có thể nhận được những tài liệu, đề thi mới nhất.