Lý thuyết hóa 12 chương 2: Carbohydrate đầy đủ nhất
Đây là tài liệu Cao cấp - Chỉ dành cho Thành viên VnDoc ProPlus.
- Tải tất cả tài liệu lớp 12 (Trừ Giáo án, bài giảng)
- Trắc nghiệm không giới hạn
Lí thuyết bài tập Carbohydrate
Lý thuyết hóa 12 chương 2: Carbohydrate đầy đủ nhất được VnDoc biên soạn là tổng hợp Tóm tắt chương 2 hóa 12. Mời các bạn cùng theo dõi bài viết dưới đây.
Một số nội dung ôn thi THPT Quốc gia năm 2025
- Tổng ôn Polymer Hóa 12: Lý thuyết, Bài tập
- Tổng ôn Đại cương về hóa học hữu cơ
- Sổ tay Hóa học 12: Tài liệu ôn thi THPT Quốc gia ngắn gọn, dễ hiểu
- Những kiến thức trọng tâm môn Hóa trong đề thi THPT Quốc gia
A. KHÁI NIỆM, CÁCH PHÂN LOẠI CARBOHYDRATE
Các chất tinh bột, đường saccharose, glucose, fructose, cellulose có công thức chung là Cn(H2O)m nên có tên gọi là carbohydrate. Trong phân tử của chúng có nhiểu loại nhóm chức (tạp chức). Carbohydrate được chia làm 3 nhóm chủ yếu sau đây:
|
CARBOHYDRATE |
||
|
Monosaccharide |
Disaccharide |
Polysaccharide |
|
Là nhóm carbohydrate đơn giản nhất, không bị thuỷ phân. Ví dụ: glucose, fructose. |
Là nhóm carbohydrate phức tạp hơn, khi bị thuỷ phân hoàn toàn, mỗi phân tử tạo thành hai phân tử monosaccharide. Ví dụ: saccharose, maltose. |
Là nhóm carbohydrate phức tap nhất, khi bị thuỷ phân hoàn toàn, mỗi phân tử tạo thành nhiều phân tử monosaccharide. Ví dụ: tinh bột, cellulose. |
B. GLUCOSE VÀ FRUCTOSE
I. TRẠNG THÁI TỰ NHIÊN GLUCOSE VÀ FRUCTOSE
- Glucose là chất rắn, vị ngọt, dễ tan trong nước. Trong tự nhiên, glucose có trong nhiều loại trái cây chín. Ở người trưởng thành, khoẻ mạnh lượng glucose trong máu trước hơn khi ăn khoảng 4,4 - 7,2 mmol/L (hay 80 - 130 mg/dL).
Fructose là chất rắn, dễ tan trong nước, có vị ngọt hơn glucose. Fructose cũng có trong một số trái cây chín. Mật ong chứa trung bình 40% fructose và 30% glucose theo khối lượng.
II. CÔNG THỨC CẤU TẠO MẠCH HỞ VÀ MẠCH
Glucose có công thức phân tử C6H12O6. Phân tử glucose ở dạng mạch hở có năm nhóm hydroxy và một nhóm aldehyde, với công thức cấu tạo là CH2OH[CHOH]4CH=O.
- Các nghiên cứu sâu hơn về cấu tạo cho biết glucose có một dạng mạch hở và hai dạng mạch vòng (α và β) chuyển hoá qua lại lẫn nhau.
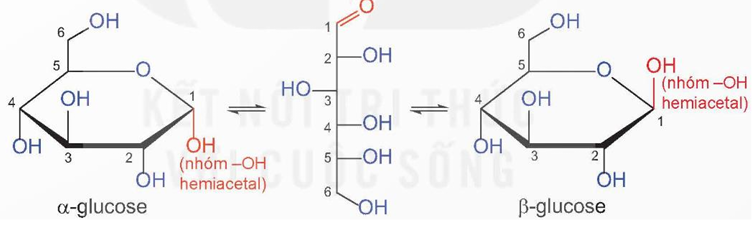
- Fructose có công thức phân tử C6H12O6, ở dạng mạch hở chứa năm nhóm hydroxy và một nhóm ketone. Tương tự glucose, fructose tồn tại đồng thời ở dạng mạch hở và mạch vòng.
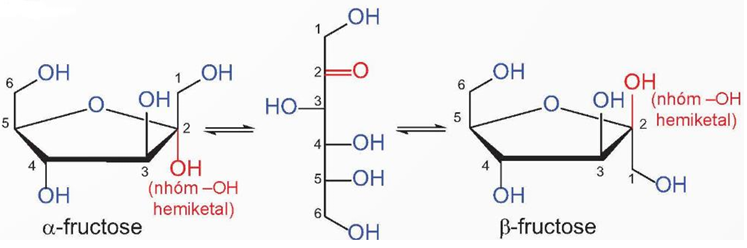
- Trong môi trường kiềm, glucose và fructose có thể chuyển hoá qua lại:
Glucose ![]() Fructose
Fructose
Chú ý: Cấu tạo vòng của các monosaccharide hình thành do phản ứng thuận nghịch giữa nhóm –OH với –CH=O (hoặc >C=O) hình thành cấu tạo hemiacetal (hoặc hemiketal). Ví dụ: sự hình thành cấu tạo vòng của glucose là do nhóm –OH trên carbon số 5 với nhóm –CH=O (hình bên dưới):
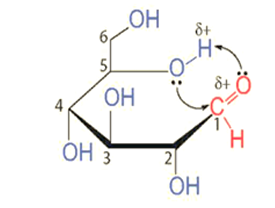
II. TÍNH CHẤT HÓA HỌC
Glucose có tính chất của polyalcohol và của aldehyde. Fructose có tính chất của polyalcohol và của ketone.
1. Tính chất của polyalcohol
Phân tử glucose và fructose có nhiều nhóm hydroxy liền kề nên dung dịch glucose và dung dịch fructose có thể hoà tan copper(II)hydroxide trong môi trường kiềm, tạo thành dung dịch có màu xanh lam.
2C6H12O6 + Cu(OH)2 → (C6H11O6)2Cu + 2H2O
2. Tính chất của aldehyde
Nhóm aldehyde của glucose có thể bị oxi hoá bởi Cu(OH)2 trong môi trường kiềm khi đun nóng, bởi thuốc thử Tollens và bởi nước bromine.
CH2OH[CHOH]4CH=O + 2Cu((OH)2 + NaOH ![]() CH2OH[CHOH]4COONa + Cu2O + 3H2O
CH2OH[CHOH]4COONa + Cu2O + 3H2O
CH2OH[CHOH]4CH=O + 2[Ag(NH3)2]OH ![]() CH2OH[CHOH]4COONH4 +2Ag + 3NH3 + H2O
CH2OH[CHOH]4COONH4 +2Ag + 3NH3 + H2O
CH2OH[CHOH]4CH=O + Br2 + H2O → CH2OH[CHOH]4COOH + 2HBr
Tương tự glucose, fructose cũng bị oxi hoá bởi thuốc thử Tollens và bởi Cu(OH)2 trong môi trường kiềm
3. Tính chất của nhóm –OH hemiacetal
Ở dạng cấu tạo mạch vòng, nhóm –OH hemicetal của glucose tác dụng với methanol khi có mặt của HCl khan, tạo thành methyl glucoside.
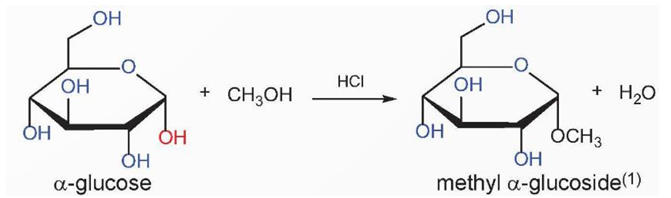
4. Phản ứng lên men của glucose
Dưới tác dụng của enzyme từ các vi sinh vật khác nhau, glucose được lên men tạo thành các hợp chất có nhiều ứng dụng trong đời sống như ethanol, lactic acid…
Ví dụ:
C6H12O6 ![]() 2C2H5OH + 2CO2
2C2H5OH + 2CO2
C6H12O6 ![]() 2CH3CH(OH)COOH
2CH3CH(OH)COOH
III. TRẠNG THÁI TỰ NHIÊN VÀ ỨNG DỤNG
1. Glucose
- Glucose là chất rắn, dễ tan trong nước, có vị ngọt.
- Glucose hình thành trong thực vật nhờ quá trình quang hợp. Glucose có trong hầu hết các bộ phận của cây như hoá, lá…. và nhất là trong quả chín. Glucose có trong cơ thể người và động vật. Trong máu người trưởng thành, khoẻ mạnh vào lúc đói có một lượng nhỏ glucose với nồng độ khoảng 4,4 -7,2 mmol/l (hay 80 -130mg/dL).
- Glucose đóng vai trò cung cấp năng lượng cho tế bào. Trong cuộc sống, glucose có các ứng dụng phổ biến sau:
+ Tráng gương, tráng ruột phích;
+ Nguyên liệu sản xuất ethanol;
+ Dùng trong công nghiệp chế biến thực phẩm và đồ uống;
+ Trong y học, glucose 5% được dùng làm dung dịch truyền tĩnh mạch.
2. Fructose
- Fructose là chất rắn, dễ tan trong nước, có vị ngọt.
- Fructose có trong nhiều trái cây (táo, lựu, nho, lê…), trong một số loại củ (cà rốt, củ cải đường…) và fructose có nhiều trong mật ong.
- Tương tự glucose, fructose chủ yếu đóng vài trò cung cấp năng lượng cho tế bào.
B. SACCHAROSE VÀ MALTOSE
I. CẤU TẠO PHÂN TỬ
- Saccharose có công thức phân tử C12H22O11, cấu tạo từ một đơn vị α-glucose và một đơn vị β-fructose qua liên kết α -1,2-glycoside.
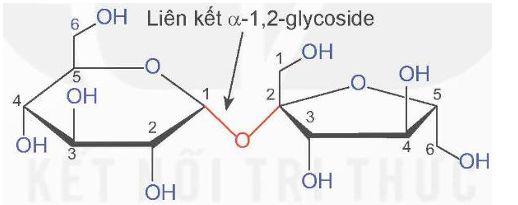
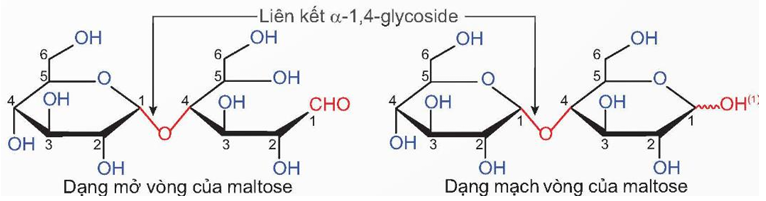
- Maltose có công thức phân tử C12H22O11, cấu tạo từ hai đơn vị glucose qua liên kết α -1,4-glycoside.
II. TÍNH CHẤT HÓA HỌC CỦA SACCHAROSE
1. Tính chất của polyalcohol
Phân tử saccharose có nhiều nhóm hydroxy kề nhau nên dung dịch chất này có thể hoà tan Cu(OH)2 trong môi trường kiềm, tạo thành dung dịch có màu xanh lam.
2C12H22O11 + Cu(OH)2 → (C12H21O11)2Cu + 2H2O
2. Phản ứng thuỷ phân
Saccharose bị thuỷ phân trong môi trường acid hoặc dưới tác dụng của enzyme, tạo thành glucose và fructose.
C12H22O11 +H2O C6H12O6 (glucose) + C6H12O6 (fructose)
III. TRẠNG THÁI TỰ NHIÊN VÀ ỨNG DỤNG
1. Saccharose
- Saccharose là chát rắn có vị ngọt, dễ tan trong nước.
- Saccharose được tổng hợp trong thực vật từ glucose và fructose. Saccharose có trong nhiều loài thực vật, có nhiều nhất trong cây mía, củ cải đường và hoa thốt nốt.
- Saccharose được sử dụng như một chất làm ngọt phổ biến trong sản xuất thực phẩm như bánh, kẹo, nước giải khát và đồ uống có gas,…
2. Maltose
- Maltose là chất rắn, có vị ngọt, dễ tan trong nước.
- Maltose có trong một số hạt nảy mầm. Maltose chủ yếu được tạo ra trong quá trình thuỷ phân tinh bột.
- Maltose được sử dụng làm nguyên liệu sản xuất bia và chất tạo ngọt cho một số loại bánh kẹo.
D. TINH BỘT VÀ CELLULOSE
I. CẤU TẠO PHÂN TỬ
1. Tinh bột
- Tinh bột là polymer thiên nhiên, gồm amylose và amylopectin. Tinh bột có công thức phân tử là (C6H10O5)n.
+ Phân tử amylose cấu tạo từ nhiều đơn vị α-glucose liên kết với nhau qua các liên kết α-1,4-glycoside và hình thành chuỗi xoắn.
+ Phân tử amylopectin có cấu tạo phân nhánh, gồm các chuỗi chứa nhiều đơn vị α-glucose liên kết với nhau qua các liên kết α-1,4-glycoside. Các chuỗi này liên kết với nhau tạo cấu tạo mạch nhánh qua liên kết α-1,6-glycoside.
2. Cellulose
Cellulose là polymer thiên nhiên, có công thức phân tử là (C6H10O5)n. Phân tử cellulose cấu tạo từ nhiều đơn vị β-glucose qua liên kết β-1,4-glycoside và hình thành chuỗi không nhánh.
II. TÍNH CHẤT HOÁ HỌC
1. Tính chất của tinh bột
a) Phản ứng thuỷ phân
Tinh bột bị thuỷ phân dưới tác dụng của enzyme hoặc acid. Khi tinh bột bị thuỷ phân không hoàn toàn tạo thành dextrin, maltose và glucose. Tinh bột bị thuỷ phân hoàn toàn tạo thành glucose.
(C6H10O5)n + nH2O ![]() nC6H12O6 (glucose)
nC6H12O6 (glucose)
(Dextrin là các hợp chất carbohydrate có phân từ khối thấp hơn tinh bột)
b) Phản ứng màu với dung dịch lodine
Trong tinh bột, các phân tử amylose có dạng xoắn, khi tương tác với iodine tạo ra màu xanh tím. Phản ứng này được dùng để nhận biết tinh bột.
2. Tính chất của cellulose
a) Phản ứng thủy phân
Tương tự tinh bột, cellulose bị thủy phân bởi enzyme hoặc acid (HCl hoặc H2SO4).
Phản ứng thủy phân hoàn toàn tạo thành glucose.
(C6H10O5)n + nH2O![]() nC6H12O6 (glucose)
nC6H12O6 (glucose)
b) Phản ứng với nitric acid
Trong mỗi đơn vị glucose cấu thành phân tử cellulose có ba nhóm hydroxy. Khi đun nóng cellulose với hỗn hợp HNO3 đặc và H2SO4 đặc, tuỳ theo điều kiện phản ứng mà một, hai hay cả ba nhóm hydroxy này có thể phản ứng với nitric acid tạo thành cellulose nitrate.
Ví dụ:
![]()
c) Cellulose phản ứng với nước Schweizer
Cellulose tan được trong nước Schweizer (dung dịch thu được khi hòa tan Cu(OH)2 trong ammonia).
III. TRẠNG THÁI TỰ NHIÊN VÀ ỨNG DỤNG
1. Tinh bột
- Tinh bột là chất rắn màu trắng, hầu như không tan trong nước lạnh. Trong nước nóng, tinh bột tan tạo dịch keo nhớt, gọi là hồ tinh bột.
- Sự tạo thành tinh bột trong cây xanh: Trong thực vật, tinh bột có chủ yếu trong củ, quả hay hạt. Sự hình thành tinh bột trong thực vật diễn ra qua nhiều giai đoạn, bao gồm hai quá trình chính là quá trình quang hợp thành thành glucose và quá trình kết hợp của các đơn vị glucose tạo thành tinh bột.
6nCO2 + 5nH2O ![\xrightarrow[ánh\: sáng]{chất\: diệp\: lục}](/data/image/holder.png) (C6H10O5)n + 6nO2
(C6H10O5)n + 6nO2
- Sự chuyển hóa tinh bột trong cơ thể: Khi con người sử dụng thức ăn chứa tinh bột, enzyme α-amylase có trong nước bọt thúc đẩy quá trình thủy phân tinh bột thành các phân tử nhỏ hơn bao gồm maltose và dextrin. Quá trình này tiếp tục ở ruột non, nơi phần lớn tinh bột bị thủy phân thành glucose. Glucose được hấp thụ vào máu và di chuyển đến các tế bào trong khắp cơ thể. Glucose có thể được sử dụng cho nhu cầu năng lượng hoặc có thể chuyển đổi thành glycogen lưu trữ trong gan và cơ.
- Tinh bột là nguồn lương thực chính của con người và một số động vật, đồng thời cũng được dùng nhiều trong công nghiệp thực phẩm (chất làm đặc, chất kết dính, sản xuất ethanol,...). Ngoài ra, tinh bột cũng được sử dụng làm chất kết dính trong công nghiệp giấy và công nghiệp dệt may.
2. Cellulose
- Cellulose là chất rắn, dạng sợi, màu trắng, không tan trong nước ngay cả khi đun nóng, không tan trong các dung môi hữu cơ thông thường như ether, benzene,....
- Cellulose được tổng hợp bởi thực vật, chiếm khoảng 50% khối lượng của gỗ khô và khoảng 90% khối lượng sợi bông.
- Cellulose được sử dụng để làm vật liệu xây dựng (các loại đồ gỗ), sản xuất giấy, sợi tự nhiên và sợi nhân tạo. Cellulose cũng được sử dụng làm nguyên liệu để điều chế ethanol và cellulose trinitrate (dùng chế tạo thuốc súng không khói).
Để tham khảo toàn bộ tài liệu mới nhất mời các bạn ấn link TẢI VỀ phía dưới.
..........................

