Dạng bài tập xác định chỉ số xà phòng hóa của chất béo
Chuyên đề Hóa học 12 Dạng bài tập xác định chỉ số xà phòng hóa của chất béo được VnDoc biên soạn tổng hợp đưa ra phương pháp công thức xác định chỉ số xà phòng hóa của chất béo, từ đó đưa ra các dạng bài tập ví dụ, giúp các bạn học sinh có thể vận dụng, luyện tập làm các dạng bài tập dựa theo hướng dẫn. Nội dung tài liệu sẽ giúp các bạn giải bài tập Hóa học lớp 12 hiệu quả hơn. Mời các bạn tham khảo.
Hóa học 12: Dạng bài tập xác định chỉ số xà phòng hóa của chất béo
A. Phương pháp xác định chỉ số xà phòng hóa của chất béo
Chất béo gồm 2 thành phần chính là: Triglyceride và acid béo tự do.
RCOOH + KOH → RCOOK + H2O (1)
(RCOO)3C3H5 + KOH → 3RCOOK + C3H5(OH)3 (2)
- Chỉ số acid của chất béo: Số mg KOH dùng để trung hòa lượng axit tự do trong 1 gam chất béo.
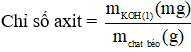
- Chỉ số este hóa: Số mg KOH cần dùng để xà phòng hóa hoàn toàn các glixerit trong 1 g chất béo
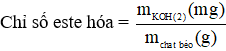
- Chỉ số xà phòng của chất béo: Số mg KOH cần để xà phòng hóa Triglyceride (tức chất béo) và trung hòa axit béo tự do trong gam chất béo.
Chỉ số xà phòng hóa = 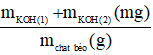
Chỉ số xà phòng hóa = chỉ số acid + chỉ số este hóa
- Chỉ số iot: là số gam iot có thể cộng vào liên kết bội trong mạch C của 100 gam lipid. Chỉ số này dùng để đánh giá mức độ không no của lipit.
B. Ví dụ minh họa xác định chỉ số xà phòng hóa của chất béo
Ví dụ 1: Để trung hòa lượng acid béo tự do có trong 14gam một mẩu chất béo cần 15ml dung dịch KOH 0,1M. Chỉ số axit của mẩu chất béo trên là:
A. 6,0
B. 7,2
C. 4,8
D. 5,5
Đáp án hướng dẫn giải chi tiết
Theo định nghĩa: chỉ số axit của chất béo là số miligam KOH cần dùng để trung hòa hết các acid béo tự do có trong 1 gam chất béo.
Ta có: mKOH = 0,015 . 0,1 . 56000 = 84 (mg)
⇒ Chỉ số axit là: 84/14 = 6
Ví dụ 2: Để tác dụng hết với 100 gam lipid có chỉ số axit bằng 7 phải dùng 17,92 gam KOH. Khối lượng muối thu được là:
A. 108,265 g
B. 170g
C. 82,265g
D. 107,57g
Đáp án hướng dẫn giải chi tiết
Ta có: mKOH cần dùng = 7. 100 = 700 mg = 0,7 (gam)
⇒ nKOH = 0,7/56 = 0,0125 (mol)
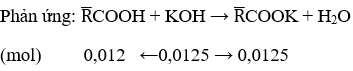
nKOH phản ứng với lipid = 17,92/56 – 0,0125 = 0,3075 (mol)
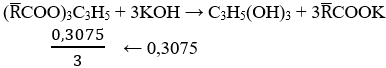
Vậy mmuối = 100 + mKOH - mH2O - mglixerol = 100 + 17,92 – 0,0125 . 18 – 0,3075/3 . 92 = 108, 265 (gam)
Ví dụ 3: Hãy tính khối lượng NaOH cần dùng để trung hòa axit tự do có trong 5 gam chất béo với chỉ số acid bằng 7.
Đáp án hướng dẫn giải chi tiết
Theo định nghĩa, chỉ số axit của chất béo bằng 7 nghĩa là muốn trung hòa lượng acid béo tự do trong 1 gam chất béo phải dùng 7 mg KOH. Vậy muốn trung hòa acid béo tự do trong 5 gam chất béo có chỉ số 7 thì phải dùng 5 .7 = 35 mg KOH, hay ![]() mol KOH
mol KOH
⇒ nNaOH = nOH- = ![]() mol
mol
⇒ mNaOH = ![]() .40 = 25 mg = 0,025 g/5g chất béo
.40 = 25 mg = 0,025 g/5g chất béo
Ví dụ 4. Khi thủy phân a gam ester X thu được 0,92 gam glycerol, 3,02 gam Sodium linoleate C17H31COONa và m gam muối của Sodium oleate C17H33COONa. Giá trị a, m lần lượt là:
A. 6,08 gam và 8,82 gam
B. 8,06 gam và 8,28 gam
C. 8,82 gam và 6,08 gam
D. 8,16 gam và 8,86 gam
Đáp án hướng dẫn giải
PTHH tổng quát: (RCOO)3C3H5 + 3NaOH → 3RCOONa + C3H5(OH)3
Theo tỉ lệ phản ứng ⇒ nmuối = nNaOH = 3. nglycerol = 3. 0,01 = 0,03 mol
⇒n(C17H33COONa) = 0,03 – 0,01 = 0,02 mol
⇒ m = m(C17H33COONa) = 0,02. 304 = 6,08(g)
mNaOH = 0,03. 40 = 1,2 g
BTKL ⇒ a = mester = mMuối + mglycerol - mNaOH = 6,08 + 3,02 + 0,92 - 1,2 = 8,82g
C. Bài tập vận dụng xác định chỉ số xà phòng hóa của chất béo
Câu 1. Để xà phòng hóa hoàn toàn 2,52 gam một lipid cần dùng 90ml dung dịch NaOH 0,1M. Chỉ số xà phòng của lipid là:
A. 210
B. 150
C. 187
D. 200
Ta có: nKOH = nNaOH = 0,09 . 0,1 = 0,009 (mol)
⇒ mKOH = 0,009 . 56 = 0,504 (gam) = 504 (mg)
1 gam lipid cần: ![]() = 200 (mg) KOH
= 200 (mg) KOH
Vậy chỉ số xà phòng là 200
Câu 2. Khi trung hòa 2,8 gam chất béo cần 3 ml dung dịch KOH 0,1M. Tính chỉ số axit chủa chất béo đó.
A. 6
B. 5
C. 7
D. 8
Ta có: nKOH = 0,1. 0,003 = 0,0003 mol
⇒ mKOH = 0,0003 . 56 = 0,0168 g = 16,8 mg
Vậy chỉ số axit = ![]() = 6
= 6
Câu 3. Muốn trung hòa 5,6 gam một chất béo X đó cần 6ml dung dịch KOH 0,1M. Hãy tính chỉ số acid của chất béo X và tính lượng KOH cần trung hòa 4 gam chất béo có Y chỉ số acid bằng 7.
A. 5 và 14mg KOH
B. 4 và 26mg KOH
C. 3 và 56mg KOH
D. 6 và 28mg KOH
Chỉ số axit = ![]() = 6
= 6
Trung hòa 4g chất béo cần mKOH = 4.7 = 28 (mg)
Câu 4. Chỉ số iot của triolein có giá trị bằng bao nhiêu?
A. 26,0
B. 86,2
C. 82,3
D. 102,0
Phản ứng: (C17H33COO)3C3H5 + 3I2 → (C17H33COOI2)3C3H5
⇒Chỉ số iot là: ![]() . 100 = 86,2
. 100 = 86,2
Câu 5. Số miligam KOH trung hòa hết lượng acid tự do và xà phòng của chất béo. Tính chỉ số xà phòng hóa của mẫu chất béo có chỉ số acid bằng 7 chứa tristearoyl glycerol còn lẫn một lượng Acid stearic.
A. 175
B. 168
C. 184
D. 158
Khối lượng KOH trung hòa acid: 0,007 (gam)
nKOH = 0,007 : 56 = 0,125.10-3 (mol)
Khối lượng C17H35COOH trong 1 gam chất béo là:
0,125 . 10-3. 890 = 0,11125 g
Khối lượng tristearoyl glycerol trong 1 gam chất béo là: 0,8875 (gam)
⇒ n ≈ 0,001 mol ⇒ nKOH = 0,003 mol ⇒ mKOH = 0,168 g
⇒ Chỉ số xà phòng hóa là: 168 + 7 = 175.
