Các dạng bài tập về dãy điện hóa kim loại và pin điện hóa
Chuyên đề Hóa học 12 Các dạng bài tập về dãy điện hóa kim loại và pin điện hóa. Nội dung tài liệu sẽ giúp các bạn học sinh giải bài tập Hóa học lớp 12 hiệu quả hơn. Mời các bạn tham khảo.
Hóa học 12: Các dạng bài tập về dãy điện hóa kim loại và pin điện hóa
A. Phương pháp và ví dụ về dãy điện hóa kim loại và pin điện hóa
Lý thuyết và Phương pháp giải
Xác định thế điện cực chuẩn, suất điện động chuẩn của pin điện hóa
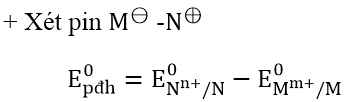
+ Chiều phản ứng: Viết cặp oxi hóa - khử có thế điện cực nhỏ ở bên trái, cặp oxi hóa - khử có thế điện cực chuẩn lớn hơn ở bên phải rồi viết phương trình phản ứng oxi hóa - khử theo quy tắc α.
Ví dụ minh họa
Bài 1: Tính thế điện cực chuẩn E0 của những cặp oxi hóa khử sau:
a. E0 (Cr3+/Cr), biết suất điện động chuẩn của pin điện hóa Cr -Ni là +0,51V và E0 (Ni2+/Ni) = -0,23V.
b. E0 (Mn2+/Mn), biết suất điện động chuẩn của pin điện hóa Cd -Mn là +0,79V và E0(Cd2+/Cd) = -0,40V.
Hướng dẫn:
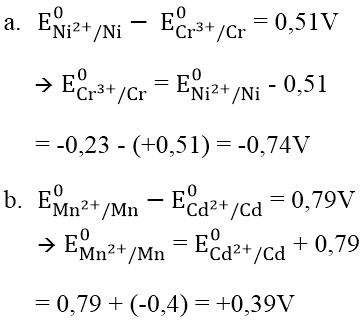
Bài 2: Biết phản ứng oxi hóa khử xảy ra trong một pin điện hóa là:
Fe + Ni2+ → Fe2+ + Ni
a. Hãy xác định các điện cực âm và dương của pin điện hóa.
b. Viết các phản ứng oxi hóa và phản ứng khử xảy ra trên mỗi điện cực.
c. Tính suất điện động chuẩn pin điện hóa.
Hướng dẫn:
a. Ni (+); Fe (-)
b. Phản ứng trên các điện cực:
Cực (-): Fe → Fe2+ + 2e
Cực (+): Ni2+ + 2e → Ni
c. E0pin = -0,23 - (-0,44) = 0,21 V
Bài 3: Tính thế điện cực chuẩn E0 của các cặp oxi hóa khử sau:
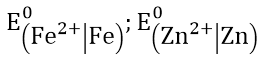 . Biết suất điện động chuẩn của pin điện hóa Fe – Ni là 0,18V và của pin Zn – Ag là 1,56V, thế điện cực chuẩn
. Biết suất điện động chuẩn của pin điện hóa Fe – Ni là 0,18V và của pin Zn – Ag là 1,56V, thế điện cực chuẩn 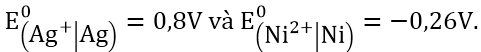
Hướng dẫn:
+) Pin điện hóa Fe – Ni: cực (-) là Fe; cực dương (+) là Ni
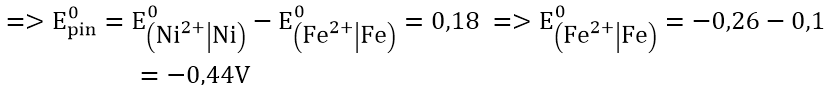
+) Pin điện hóa Zn – Ag : cực (-) là Zn; cực (+) là Ag.
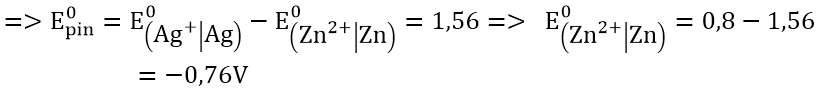
B. Bài tập trắc nghiệm về dãy điện hóa kim loại và pin điện hóa
Bài 1: Cho pin điện hóa ![]() , biết
, biết ![]() . Vậy suất điện động của pin có giá trị là:
. Vậy suất điện động của pin có giá trị là:
A. 0,78V B. - 0,78V C. - 0,1V D. 0,2V
Đáp án: A
Ta có: E0pđh = E0Cu2+/Cu - E0Fe2+/Fe = 0,34 - (-0,44) = 0,78V
Bài 2: Cho E0pđh của pin được tạo bởi giữa Sn2+/Sn và Ag+/Ag là 0,94V. Biết E0Ag+/Ag = 0,8V. Vậy E0Sn2+/Sn có giá trị là:
A. -1,74V B. 1,74V C. -0,14V D. 0,14V
Đáp án: C
Ta có:
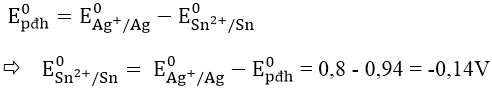
Bài 3: Cho suất điện động chuẩn của các pin điện hóa : Zn - Cu là 1,1V; Cu - Ag là 0,46V. Biết thể tích điện cực chuẩn E0Ag+/Ag = + 0,8V. Thế điện cực chuẩn E0Zn2+/Zn và E0Cu2+/Cu có giá trị lần lượt là:
A. -0,76V và +0,34V B. -1,46V và -0,34V
C. +1,56V và +0,64V D. -1,56V và +0,64V
Đáp án: A
Ta có:
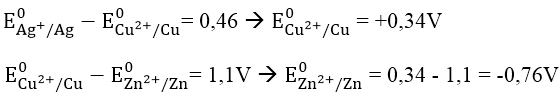
Bài 4: Biết E0Ag+/Ag = + 0,8V, E0Fe3+/Fe2+ =0,77V
Vậy nhận định nào sau đây đúng?
A. Ion Fe3+ oxi hóa được Ag. B. Ion Fe2+ bị oxi hóa bởi Ag+.
C. Ion Ag+ bị khử bởi ion Fe3+. D. Ion Fe2+ oxi hóa được Ag.
Đáp án: B
Dựa vào E0 ta có thể viết phương trình phản ứng:
Ag+ + Fe2+ → Fe3+ + Ag↓
Bài 5: Tính thế điện cực chuẩn của cặp oxi hóa - khử sau:
E0Zn2+/Zn, biết rằng E0pin(Zn-Cu) = 1,10V và E0Cu2+/Cu = +0,34V.
A. -0,76V B. 0,42 V C. -0,38 V D. 0,24V
Đáp án: A
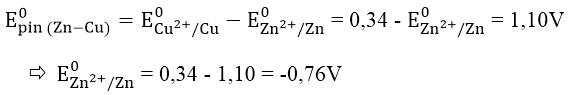
Bài 6: Có pin điện hóa được tạo thành từ những cặp oxi hóa - khử sau:
Fe2+/Fe và Ag+/Ag
Hãy tính suất điện động của mỗi pin điện hóa, biết rằng:
E0Ag+/Ag = + 0,8V; E0Fe2+/Fe = -0,44V.
A. 0,36V B. -1,24V C. 1,24V D. -0,36V
Đáp án: C
Bài 7: Cho suất điện động chuẩn E0 của các pin điện hóa: E0 (Cu - X) = 0,46V; E0 (Y - Cu) = 1,1V; E0 (Z - Cu) = 0,47V (X, Y, Z là ba kim loại). Dãy các kim loại xếp theo chiều tăng dần tính khử từ trái sang phải là:
A. Z, Y, Cu, X B. X, Cu, Z, y C. Y, Z, Cu, X D. X, Cu, Y, Z
Đáp án: B
E0 (Cu - X) = 0,46V > 0 → Tính khử của X < Cu
E0 (Y - Cu) = 1,1V > E0 (Z - Cu) = 0,47V > 0 → Tính khử của Y > Z > Cu.
Tóm lại: tính khử tăng dần theo chiều X, Cu, Z, Y.
Bài 8: Cho suất điện động chuẩn của các pin điện hóa: Zn-Cu là 1,1V; Cu-Ag là 0,46V. Biết thế điện cực chuẩn E0Ag+/Ag = +0,8V. Thế điện cực chuẩn E0Zn2+/Zn và E0Cu2+/Cu lần lượt là:
A. -0,76V và +0,34V.
B. -1,46V và -0,34V.
C. +1,56V và +0,64V.
D. -1,56V và +0,64V.
Đáp án: A
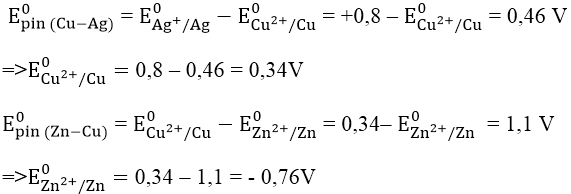
Mời các bạn tham khảo thêm các bài viết dưới đây của chúng tôi:
- Lý thuyết: Sự điện phân - Sự ăn mòn
- Lý thuyết: Kim loại và hợp kim
- Lý thuyết: Luyện tập tính chất của kim loại
- Lý thuyết: Điều chế kim loại
- Lý thuyết: Luyện tập sự điện phân - Sự ăn mòn kim loại - Điều chế kim loại
- Tính chất chung của kim loại
- Chuỗi phản ứng hóa học của kim loại
Trên đây VnDoc đã giới thiệu tới các bạn Các dạng bài tập về dãy điện hóa kim loại và pin điện hóa. Để có kết quả cao hơn trong học tập, VnDoc xin giới thiệu tới các bạn học sinh tài liệu Giải bài tập Toán lớp 12, Giải bài tập Hóa học lớp 12, Giải bài tập Vật Lí 12, Tài liệu học tập lớp 12 mà VnDoc tổng hợp và đăng tải.
