Dạng bài tập phản ứng thủy phân Lipit
Chuyên đề Hóa học 12 Dạng bài tập phản ứng thủy phân Lipit. Chắc chắn tài liệu sẽ giúp các bạn giải bài tập Hóa học lớp 12 hiệu quả hơn. Mời các bạn tham khảo.
Hóa học 12: Dạng bài tập phản ứng thủy phân Lipit
Phương pháp giải bài tập phản ứng thủy phân Lipit
a. Phản ứng thủy phân trong môi trường axit
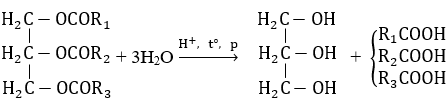
Trong công nghiệp, phản ứng trên được tiến hành trong nồi hấp ở 220℃ và 25 atm.
b. Phản ứng xà phòng hóa
Khi đun nóng với dung dịch kiềm (NaOH hoặc KOH) thì tạo ra glixerol và hỗn hợp muối của các axit béo. Muối natri hoặc kali của các axit béo chính là xà phòng
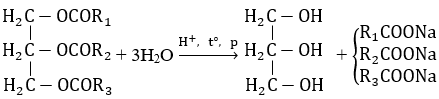
Phản ứng của chất béo với dung dịch kiềm được gọi là phản ứng xà phòng hóa. Phản ứng xà phòng hóa xảy ra nhanh hơn phản ứng thủy phân trong môi trường axit và không thuận nghịch.
- Chỉ số xà phòng hóa: là số mg KOH dùng để xà phòng hóa hoàn toàn 1 gam lipit (tức là để trung hòa axit sinh ra từ sự thủy phân 1 gam lipit).
- Chỉ số axit: số mg KOH dùng để trung hòa axit tự do có trong 1 mg lipit.
Ví dụ minh họa bài tập phản ứng thủy phân Lipit
Ví dụ 1: Khi xà phòng hóa tristearin ta thu được sản phẩm là
A. C15H31COONa và etanol.
B. C17H35COOH và glixerol.
C. C15H31COOH và glixerol.
D. C17H35COONa và glixerol.
Giải
Đáp án D
PTHH: (C17H35COO)3C3H5 + 3NaOH → 3C17H35COONa + C3H5(OH)3
⇒ sản phẩm thu được là: C17H35COONa và glixerol.
Ví dụ 2: Cần bao nhiêu kg chất béo chứa 89% khối lượng tristearin (còn 11% tạp chất trơ bị loại bỏ trong quá trình nấu xà phòng) để sản xuất được 1 tấn xà phòng chứa 72% khối lượng natri stearate.
Giải
Trong 1 tấn xà phòng có72% khối lượng natri stearate.
⇒ ![]() \(m_{C_{17}H_{35}COONa}\) = 720kg
\(m_{C_{17}H_{35}COONa}\) = 720kg
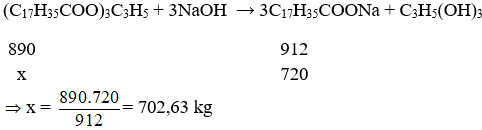
Khối lượng chất béo là : ![]()
Ví dụ 3: Xà phòng hóa hoàn toàn 17,24g chất béo cần vừa đủ 0,06mol NaOH. Cô cạn dung dịch sau phản ứng thu được khối lượng xà phòng là
A. 17,80g
B. 18,24g
C. 16,68g
D. 18,38g
Giải
Đáp án A
Phản ứng: (RCOO)3C3H5 + 3NaOH → 3RCOONa + C3H5(OH)3
![]()
BTKL: mxà phòng = 17,24 + 0,06.40 – 0,02.92 = 17,8g
Bài tập vận dụng phản ứng thủy phân Lipit
Câu 1. Phát biểu nào sau đây không đúng?
A. Chất béo là trieste của glixerol với các axit monocacboxylic có mạch cacbon dài, không phân nhánh
B. Chất béo chứa chủ yếu các gốc no của axit thường là chất rắn ở nhiệt độ phòng
C. Chất béo chứa chủ yếu các gốc không no của axit thường là chất lỏng ở nhiệt độ phòng và được gọi là dầu
D. Phản ứng thủy phân chất béo trong môi trường kiềm là phản ứng thuận nghịch
Đáp án D
Phản ứng thủy phân chất béo trong môi trường kiềm là phản ứng xà phòng hóa, xảy ra nhanh hơn phản ứng thủy phân trong môi trường axit và không thuận nghịch.
Câu 2. Khi đun nóng chất béo với dung dịch H2SO4 loãng thu được
A. Glixerol và axit cacboxylic.
B. Glixerol và muối của axit béo.
C. Glixerol và muối của axit cacboxylic.
D. Glixerol và axit béo
Đáp án D
Đun nóng chất béo với dung dịch H2SO4 loãng thu được glixerol và axit béo: phản ứng thủy phân trong môi trường axit.
Câu 3. Thủy phân chất béo glixerol tristearat (C17H35COO)3C3H5 cần dùng 1,2 kg NaOH. Biết hiệu suất phản ứng là 80%. Khối lượng glixerol thu được là:
A. 8,100kg
B. 0.750 kg
C. 0,736 kg
D. 6,900 kg
(C17H35COO)3C3H5 + 3NaOH → 3C17H35COONa + C3H5(OH)3 (1)
Ta có: nNaOH = 1,2/40 = 0,03 (kmol)
Từ (1) ⇒ ![]() \(n_{C_3H_5(OH)_3}\) = 1/3 nNaOH = 0,01 (kmol)
\(n_{C_3H_5(OH)_3}\) = 1/3 nNaOH = 0,01 (kmol)
⇒![]() \(m_{C_3H_5(OH)_3}\) = 0,01 . 92 = 0,92 (kg)
\(m_{C_3H_5(OH)_3}\) = 0,01 . 92 = 0,92 (kg)
Vì H = 80% ⇒ ![]() \(m_{C_3H_5(OH)}\)(3 thực tế) = 0,92 . 80/100 = 0,736 (kg)
\(m_{C_3H_5(OH)}\)(3 thực tế) = 0,92 . 80/100 = 0,736 (kg)
Đáp án C
Câu 4. Phản ứng nào sau đây dùng để điều chế xà phòng?
A. Đun nóng axit béo với dung dịch kiềm.
B. Đun nóng chất béo với dung dịch kiềm.
C. Đun nóng glixerol với các axit béo.
D. Cả A, B đều đúng.
Xà phòng là muối của natri của các axit béo (RCOONa).
Khi đun axit béo với kiềm: RCOOH + NaOH → RCOONa + H2O.
Khi đun chất béo với kiềm: C3H5(OOCR)3 + 3NaOH → C3H5(OH)3 + 3RCOONa.
Câu 5. Khi xà phòng hóa tripanmitin ta thu được sản phẩm là
A. C15H31COONa và etanol.
B. C17H35COOH và glixerol.
C. C15H31COONa và glixerol.
D. C17H35COONa và glixerol.
Tripanmitin: (C15H31COO)3C3H5 + 3NaOH → 3C15H31COONa + C3H5(OH)3
Câu 6. Xà phòng hoá hoàn toàn m gam lipit X bằng 200 gam dung dịch NaOH 8% sau phản ứng thu được 9,2 gam glixerol và 94,6 gam chất rắn khan. Công thức cấu tạo của X là:
A. (C17H35COO)3C3H5.
B. (C15H31COO)3C3H5.
C. (C17H33COO)3C3H5.
D. (C17H31COO)3C3H5.
Đặt công thức trung bình của lipit X là C3H5(OOCR)3.
C3H5(OOCR)3 + 3NaOH → C3H5(OH)3 + 3RCOONa (1)
Theo giả thiết ta có
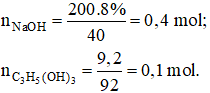
⇒ nNaOH = 0,3 mol
Do đó trong 94,6 gam chất rắn có 0,1 mol NaOH dư và 0,3 mol RCOONa.
⇒ 0,1.40 + (R+67).0,3 = 94,6 ⇒ R = 235 ⇒ R là: C17H31–
- Phương pháp điều chế và ứng dụng của Este
- Bài tập về Este đa chức
- Tìm công thức phân tử của Este dựa vào phản ứng đốt cháy
- Tìm công thức phân tử của Este dựa vào phản ứng xà phòng hóa
- Tìm công thức phân tử của Este dựa vào phản ứng thủy phân
- Bài tập hỗn hợp Este đơn chức tham gia phản ứng xà phòng hóa
- Bài tập về hỗn hợp Este hay có đáp án
Trên đây VnDoc đã giới thiệu tới các bạn Dạng bài tập phản ứng thủy phân Lipit. Để có kết quả cao hơn trong học tập, VnDoc xin giới thiệu tới các bạn học sinh tài liệu Giải bài tập Toán lớp 12, Giải bài tập Hóa học lớp 12, Giải bài tập Vật Lí 12, Tài liệu học tập lớp 12 mà VnDoc tổng hợp và đăng tải.
