150 câu trắc nghiệm Este Lipit có lời giải chi tiết (Cơ bản - phần 4)
Hóa học 12: Trắc nghiệm Este Lipit có lời giải chi tiết
Chuyên đề Hóa học 12 150 câu trắc nghiệm Este Lipit có lời giải chi tiết (Cơ bản - phần 4). Tài liệu chắc chắn sẽ là nguồn thông tin hữu ích để giúp các bạn giải bài tập Hóa học lớp 12 hiệu quả hơn. Mời các bạn tham khảo chi tiết và tải về tại đây nhé.
- 200 câu hỏi trắc nghiệm có đáp án Hóa học lớp 12: Este - Lipit
- Trắc nghiệm Hóa học lớp 12: Chương 1 - Este và Lipit
- Giải bài tập Hóa học 12 bài 8: Thực hành Điều chế, tính chất hóa học của este và cacbohiđrat
VnDoc.com xin gửi tới bạn đọc bài viết Chuyên đề Hóa học 12 150 câu trắc nghiệm Este Lipit có lời giải chi tiết (Cơ bản - phần 4) để bạn đọc cùng tham khảo. Bài viết được tổng hợp gồm có 30 câu hỏi trắc nghiệm về môn Hóa học lớp 12 phần Este lipit. Bài tập có đáp án và lời giải chi tiết kèm theo. Qua phần bài tập này bạn đọc có thể luyện tập được cách viết công thức cấu tạo thu gọn của este, cách tính khối lượng chất tham gia phản ứng... Mời các bạn cùng tham khảo chi tiết và tải về tại đây nhé.
Câu 121: Cho 20 gam một este X (có phân tử khối là 100đvc) tác dụng với 300 ml dung dịch NaOH 1M. Sau phản ứng, cô cạn dung dịch thu được 23,2g chất rắn khan. Công thức cấu tạo thu gọn của X là
A. CH2=CHCH2COOCH3.
B. CH3COOCH=CHCH3.
C. C2H5COOCH=CH2.
D. CH2=CHCOOC2H5.
nX = 0,2 mol; nNaOH = 1.0,3 = 0,3 mol → nNaOH dư = 0,3 – 0,2 = 0,1 mol.
→ mchất rắn sau phản ứng = mmuối + mNaOH dư → mmuối = 23,2 – 0,1.40 = 19,2 gam
→ Mmuối = 96 → Muối là C2H5COONa → X: C2H5COOCH=CH2
→ Đáp án C
Câu 122: Thuỷ phân hoàn toàn 444 gam một lipit X thu được 46 gam glixerol và hai loại axit béo. Hai loại axit béo đó là
A. C17H31COOH và C17H33COOH.
B. C15H31COOH và C17H35COOH.
C. C17H33COOH và C17H35COOH.
D. C17H33COOH và C15H31COOH.
nglixerol = 0,5 mol → nX = 0,5 mol → MX = 888
X: C3H5(OCOR)3 → MR = 238,33
→ Hai loại axit béo đó là: C17H33COOH và C17H35COOH
→ Đáp án C
Câu 123: Hóa hơi 27,2 gam một este X thu được 4,48 lít khí (quy về đktc). Xà phòng hóa X bằng dung dịch NaOH (vừa đủ) thu được hỗn hợp hai muối của natri. Công thức cấu tạo thu gọn của este X là
A. CH3COOC6H5.
B. C6H5COOCH3.
C. CH3COOC6H4CH3.
D. HCOOC6H5.
nkhí = 0,2 mol → MX = 136
Xà phòng hóa X bằng dung dịch NaOH (vừa đủ) thu được hỗn hợp hai muối của natri
→ X có dạng RCOOC6H5
Mà MX = 136 → MR + 121 = 136 → MR = 15 → R là CH3
→ Công thức cấu tạo thu gọn của este X là CH3COOC6H5
→ Đáp án A
Câu 124: Xà phòng hoá hoàn toàn 17,6 gam hỗn hợp 2 este là etyl axetat và metyl propionat bằng một lượng vừa đủ V ml dung dịch NaOH 0,5M. Giá trị V đã dùng là
A. 400 ml.
B. 500 ml.
C. 200 ml.
D. 600 ml.
Etyl axetat: CH3COOC2H5, metyl propionat: CH3CH2COOCH3
→ Etyl axetat và metyl propionat có cùng công thức phân tử là C4H8O2
→ neste = 0,2 mol
Gọi công thức chung của hỗn hợp este là RCOOR’
RCOOR’ + NaOH -to→ RCOONa + R’OH
→ nNaOH = neste = 0,2 mol → 0,5.V.10-3 = 0,2 → V = 400ml.
→ Đáp án A
Câu 125: Xà phòng hoá 8,8 gam etyl axetat bằng 200 ml dung dịch NaOH 0,2M. Sau khi phản ứng xảy ra hoàn toàn, cô cạn dung dịch thu được chất rắn khan có khối lượng là
A. 3,28 gam.
B. 8,56 gam.
C. 8,2 gam.
D. 10,4 gam.
![]() \(n_{CH_3COOCH_2CH_3}\) = 0,1 mol;
\(n_{CH_3COOCH_2CH_3}\) = 0,1 mol;
nNaOH = 0,2. 0,2 = 0,04 mol
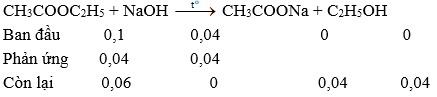
→ Chất rắn thu được sau khi cô cạn là CH3COONa
→ ![]() \(m_{CH_3COONa}\) = 0,04.82 = 3,28 gam
\(m_{CH_3COONa}\) = 0,04.82 = 3,28 gam
→ Đáp án A
Câu 126: Cho 20,8 gam hỗn hợp gồm metyl fomat và metyl axetat tác dụng với NaOH thì hết 150 ml dung dịch NaOH 2M. Khối lượng metyl fomat trong hỗn hợp là
A. 3,7 gam.
B. 3 gam.
C. 6 gam.
D. 3,4 gam.
nNaOH = 2.0,15 = 0,3 mol → neste = 0,3 mol
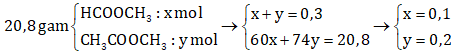
→ Khối lượng metyl fomat trong hỗn hợp là: ![]() \(m_{HCOOCH_3}\)= 0,1.60 = 6 g.
\(m_{HCOOCH_3}\)= 0,1.60 = 6 g.
→ Đáp án C
Câu 127: Muốn thuỷ phân 5,6 gam hỗn hợp etyl axetat và etyl fomiat cần 25,93 ml NaOH 10%, (D = 1,08 g/ml). Thành phần % khối lượng của etyl axetat trong hỗn hợp là
A. 47,14%.
B. 52,16%.
C. 36,18%.
D. 50,20%.
mdung dịch NaOH = D.V = 1,08. 25,93 = 28 gam
→ nNaOH = 28. 10% = 2,8 gam → nNaOH = 0,07 → neste = nNaOH = 0,07 mol
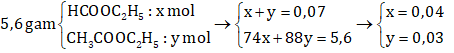
→ Thành phần % khối lượng của etyl axetat trong hỗn hợp là:
%![]() \(m_{CH_3COOC_2H_5}\) = 47,14%
\(m_{CH_3COOC_2H_5}\) = 47,14%
→ Đáp án A
Câu 128: Cho 13,6 gam phenyl axetat tác dụng với 200 ml dung dịch NaOH 1,5M đun nóng. Sau khi phản ứng xảy ra hoàn toàn thu được dung dịch X. Cô cạn X thu được a gam chất rắn khan. Giá trị của a là
A. 12,2 gam.
B. 16,2 gam.
C. 19,8 gam.
D. 23,8 gam.
![]() \(n_{CH_3COOC_6H_5}\) = 13,6/136 = 0,1 mol
\(n_{CH_3COOC_6H_5}\) = 13,6/136 = 0,1 mol
nNaOH = 1,5. 0,2 = 0,3 mol
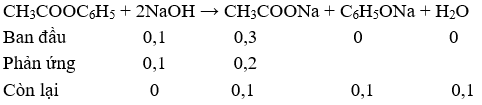
→ Chất rắn khan sau khi cô cạn dung dịch X là: NaOH dư (0,1 mol); CH3COONa (0,1 mol); C6H5ONa (0,1 mol)
→ a = mNaOH(dư) + ![]() \(m_{CH_3COONa}\) +
\(m_{CH_3COONa}\) + ![]() \(m_{C_6H_5ONa}\) = 0,1.40 + 0,1.82 + 0,1.116 = 23,8 gam
\(m_{C_6H_5ONa}\) = 0,1.40 + 0,1.82 + 0,1.116 = 23,8 gam
→ Đáp án D
Câu 129: Cho 6 gam một este X của axit cacboxylic no, đơn chức, mạch hở và ancol no, đơn chức, mạch hở phản ứng vừa hết với 100 ml dung dịch NaOH 1M. Tên gọi của este đó là
A. etyl axetat.
B. propyl fomat.
C. metyl axetat.
D. metyl fomat.
X là este của axit cacboxylic no, đơn chức, mạch hở và ancol no, đơn chức, mạch hở
→ X là este, no đơn chức, mạch hở có công thức phân tử là CnH2nO2
→ neste = nNaOH = 1.0,1 = 0,1 mol → Meste = 6/0,1 = 60 → 14n + 32 = 60 → n = 2
→ Công thức phân tử của X là C2H4O2 → este X là HCOOCH3: metyl fomat
→ Đáp án D
Câu 130: Cho 4,2 g este no, đơn chức, mạch hở E tác dụng hết với dung dịch NaOH ta thu được 4,76 g muối natri. Vậy công thức cấu tạo của E có thể là
A. CH3COOCH3.
B. HCOOCH3.
C. CH3COOC2H5.
D. HCOOC2H5.
Gọi công thức chung của este là RCOOR’ (R’ là gốc hiđrocacbon)
Ta có: RCOOR’ + NaOH → RCOONa + R’OH
Khi thủy phân este mà mmuối > meste, vậy gốc R’ là CH3 → loại đáp án C và D
Theo phương pháp tăng giảm khối lượng:
1 mol este phản ứng → khối lượng muối tăng so với khối lượng este: 23 - 15 = 8 gam
Khối lượng tăng thực tế là: 4,76 – 4,2 = 0,56 gam
→ ![]() \(n_{RCOOCH_3}\) = nRCOONa = 0,07 mol → MRCOONa = 68 gam
\(n_{RCOOCH_3}\) = nRCOONa = 0,07 mol → MRCOONa = 68 gam
→ RCOONa là HCOONa
→ Công thức cấu tạo của E là HCOOCH3
→ Đáp án B
Câu 131: X là một este no đơn chức có tỉ khối hơi đối với CH4 là 5,5. Nếu đem đun 2,2 gam este X với dung dịch NaOH (dư), thu được 2,05 gam muối. Công thức cấu tạo thu gọn của X là
A. C2H5COOCH3.
B. HCOOCH2CH2CH3.
C. CH3COOC2H5.
D. HCOOCH(CH3)2.
Ta có: RCOOR’ + NaOH → RCOONa + R’OH
Meste = 5,5.16 = 88 → neste = 2,2/88 = 0,025 mol
→ neste = nmuối = 0,025 mol → Mmuối = 82 gam
→ R là CH3 → X là CH3COOR’ → → MR’ = 29 → R’ là C2H5
→ Công thức cấu tạo thu gọn của X là CH3COOC2H5
→ Đáp án C
Câu 132: Trong cơ thể chất béo bị oxi hóa thành các chất nào sau đây?
A. NH3 và CO2.
B. H2O và CO2.
C. CO và H2O.
D. NH3, CO2 và H2O.
Ta có: RCOOR’ + NaOH → RCOONa + R’OH
Meste = 5,5.16 = 88 → neste = 0,025 mol
→ neste = nmuối = 0,025 mol → Mmuối = MRCOONa = 82 gam
→ R là CH3 → X là CH3COOR’ → ![]() \(M_{CH_3COOR'}\)→ MR’ = 29 → R’ là C2H5
\(M_{CH_3COOR'}\)→ MR’ = 29 → R’ là C2H5
→ Công thức cấu tạo thu gọn của X là CH3COOC2H5
→ Đáp án B
Câu 133: Đốt cháy hoàn toàn 0,1 mol X chỉ chứa nhóm chức este ta thu được 4.48 lít CO2(đktc) và 3,6 gam H2O. CTPT của este X có thể là:
A. C6H8O2
B. C4H8O4
C. C3H6O2
D. C2H4O2
Ta có: ![]() \(n_{CO_2}\) = 0, 2 (mol);
\(n_{CO_2}\) = 0, 2 (mol); ![]() \(n_{H_2O}\) = 0,2 (mol)
\(n_{H_2O}\) = 0,2 (mol)
0,1 mol este khi cháy tạo ra 0,2 mol CO2 và 0,2mol H2O nên este là C2H4O2.
→ Đáp án D
Câu 134: X là một este no đơn chức, có tỉ khối so với CH4 là 5,5. Nếu đem đun 2,2 gam este X với dung dịch NaOH dư, thu được 2,05 gam muối. Công thức cấu tạo thu gọn của X là:
A. C2H5COOCH3
B. CH3HCOOCH2CH2CH3
C. CH3COOC2H5
D. HCOOCH(CH3)2.
Gọi công thức tổng quát của este no đơn chức có dạng CnH2nO2.
Mà ![]() \(d_{X/CH_4}\) = 5,5 → MX = 5,5.16 = 88
\(d_{X/CH_4}\) = 5,5 → MX = 5,5.16 = 88
→ 14n + 32 = 88 → n = 4 → Công thức phân tử của X là C4H8O2.
nX = 2,2/88 = 0,025 mol
Phản ứng: RCOOR’ (0,025 mol) + NaOH → RCOONa (0,025 mol) + R’OH
Theo đề bài, ta có: 0,025(R + 67) = 2,05 → R = 15 : CH3–
Vậy công thức cấu tạo là CH3COOCH2CH3
→ Đáp án C
Câu 135: Khi đốt cháy hoàn toàn hỗn hợp các este no, đơn chức, mạch hở thì sản phẩm thu được có
A. số mol CO2 = số mol H2O.
B. số mol CO2 > số mol H2O.
C. số mol CO2 < số mol H2O.
D. không xác định được.
Gọi công thức phân tử của este no, đơn chức, mạch hở CnH2nO2 (n ≥ 2)
Phản ứng đốt cháy:
→ Sản phẩm cháy thu được có: ![]() \(n_{H_2O}\) =
\(n_{H_2O}\) = ![]() \(n_{CO_2}\)
\(n_{CO_2}\)
→ Đáp án A
Câu 136: Khi thủy phân một triglixerit X, thu được các axit béo gồm axit oleic, axit panmitic, axit stearic. Thể tích khí O2 (đktc) cần để đốt cháy hoàn toàn 8,6 gam X là
A. 15,680 lít.
B. 20,160 lít.
C. 17,472 lít.
D. 16,128 lít.
X là este của glixerol với các axit béo: axit oleic (C17H33COOH), axit panmitic (C15H31COOH) và axit stearic (C17H35COOH)
→ Công thức phân tử của X là: C55H104O6
PTHH: C55H104O6 + 78O2 → 55CO2 + 52H2O
![]() \(n_{O_2}\) = 0,01. 78 = 0,78
\(n_{O_2}\) = 0,01. 78 = 0,78
→ ![]() \(V_{O_2}\) = 0,78.22,4 = 17,4721
\(V_{O_2}\) = 0,78.22,4 = 17,4721
→ Đáp án C
Câu 137: Đốt cháy hết a mol este A được 2a mol CO2. A là
A. metyl fomat.
B. este 2 lần este.
C. este vòng.
D. este không no.
Số mol C có trong 1 mol este A: nC(1 mol A) = ![]() \(n_{CO_2}/nA\)= 2 mol
\(n_{CO_2}/nA\)= 2 mol
→ este A là HCOOCH3 (metyl fomat) là este no, đơn chức, mạch hở → Loại đáp án B, C, D
→ Đáp án A
Câu 138: Đốt cháy một lượng este no, đơn chức, mạch hở E cần 0,35 mol oxi thu được 0,3 mol CO2. Công thức phân tử của este này là
A. C2H4O2.
B. C4H8O2.
C. C3H6O2.
D. C5H10O2.
E là este no, đơn chức, mạch hở khi đốt cháy cho: = = 0,3 mol
Bảo toàn nguyên tố oxi ta có: nO(E) = ![]() \(2n_{O_2}\)= 2 +
\(2n_{O_2}\)= 2 +
→ nO(E) + 2. 0,35 = 2.0,3 + 0,3 → nO(E) = 0,2
→ nC : nH : nO = 0,3 : (2.0,3) : 0,2 = 3:6:2
→ E có dạng (C3H6O2)n
Vì E là este đơn chức → n = 1 → Công thức phân tử của este E là C3H6O2
→ Đáp án C
Câu 139: Đốt cháy 2,58 gam một este đơn chức thu được 2,688 lít CO2 (đktc) và 1,62 gam H2O. Công thức phân tử của este đó là
A. C4H8O2.
B. C4H6O2.
C. C3H6O2.
D. C5H8O2.
= 0,12 mol; = 0,09 mol
Theo định luật bảo toàn khối lượng ta có:
mO(este) = 2,58 – mC – mH = 2,58 – 0,12.12 – 0,09.2 = 0,96 g
→ nO(este) = 0,96/16 = 0,06 mol → nC : nH : nO = 0,12 : (0,09.2) : 0,06 = 2:3:1
→ este có dạng (C2H3O)n
Vì este đơn chức → n = 2 → Công thức phân tử của este đó là C4H6O2
→ Đáp án B
Câu 140: Đốt cháy 6 gam este Y ta thu được 4,48 lít CO2 (đktc) và 3,6 gam H2O. Công thức cấu tạo của Y là
A. CH3COOCH3.
B. HCOOCH3.
C. CH3COOC2H5.
D. HCOOC2H5.
Y no, đơn chức, mạch hở nên ta có sơ đồ phản ứng:
CnH2nO2 →
14n+32 18n
6 3,6
→ Công thức phân tử của Y là C2H4O2
→ Công thức cấu tạo của Y là HCOOCH3
→ Đáp án B
Câu 141: Đốt cháy hoàn toàn một lượng este X no, đơn chức, mạch hở thì thể tích khí CO2 sinh ra luôn bằng thể tích khí O2 cần dùng cho phản ứng ở cùng điều kiện nhiệt độ và áp suất. Công thức cấu tạo của este X đem đốt là
A. HCOOCH3.
B. CH3COOCH3.
C. CH3COOC2H5.
D. HCOOC3H7.
Tỉ lệ về thể tích (cùng điều kiện nhiệt độ, áp suất) chính là tỉ lệ về số mol
→ Đốt cháy este X thu được số mol khí CO2 bằng số mol khí O2 cần dùng cho phản ứng
Este X no, đơn chức mạch hở (CnH2nO2) có phản ứng đốt cháy:
→ ![]() \(n_{CO_2}\) =
\(n_{CO_2}\) = ![]() \(n_{O_2}\)→ n = (3n-2)/2 → n = 2 → Công thức phân tử của X là C2H4O2
\(n_{O_2}\)→ n = (3n-2)/2 → n = 2 → Công thức phân tử của X là C2H4O2
→ Công thức cấu tạo của este X là HCOOCH3
→ Đáp án A
Câu 142: Đốt cháy hoàn toàn m gam hỗn hợp các este no, đơn chức, mạch hở. Sản phẩm cháy được dẫn vào bình đựng dung dịch nước vôi trong dư thấy khối lượng bình tăng 6,2 gam. Số mol H2O sinh ra và khối lượng kết tủa tạo ra là
A. 0,1 mol; 12 gam.
B. 0,1 mol; 10 gam.
C. 0,01 mol; 10 gam.
D. 0,01 mol; 1,2 gam.
Este no, đơn chức, mạch hở có công thức phân tử là CnH2nO2 khi đốt cháy hoàn toàn cho:
Khối lượng bình tăng là tổng khối lượng của H2O và CO2
→![]() \(m_{CO_2}\) +
\(m_{CO_2}\) + ![]() \(m_{H_2O}\) = 6,2 → 44x + 18x = 6,2 → x = 0,1 mol
\(m_{H_2O}\) = 6,2 → 44x + 18x = 6,2 → x = 0,1 mol
CO2 + Ca(OH)2 → CaCO3↓ + H2O
→ ![]() \(n_{CaCO_3}\) =
\(n_{CaCO_3}\) = ![]() \(n_{CO_2}\)= 0,1 mol →
\(n_{CO_2}\)= 0,1 mol → ![]() \(m_{CaCO_3}\)= 0,1.100 = 10 gam
\(m_{CaCO_3}\)= 0,1.100 = 10 gam
→ Có 0,1 mol H2O sinh ra và 10 gam kết tủa tạo thành
→ Đáp án B
Câu 143: Đốt cháy 7,4 gam este E thu được 6,72 lít CO2 (đktc) và 5,4 gam H2O. Biết E có phản ứng tráng gương với dung dịch AgNO3/NH3. Vậy công thức cấu tạo của E là
A. CH3COOCH2CH2CH3.
B. HCOOCH2CH2CH3.
C. HCOOC2H5.
D. HCOOCH3.
E no, đơn chức, mạch hở nên ta có sơ đồ phản ứng:
CnH2nO2 → ![]() \(n_{H_2O}\)
\(n_{H_2O}\)
14n+32 18n
7,4 5,4
→ Công thức phân tử của E là C3H6O2
E có phản ứng tráng gương với dung dịch AgNO3/NH3 → E là este của axit fomic
→ Công thức cấu tạo của E là HCOOC2H5
→ Đáp án C
Câu 144: Đốt cháy hoàn toàn 0,11 gam một este X (tạo nên từ một axit cacboxylic đơn chức và một ancol đơn chức) thu được 0,22 gam CO2 và 0,09 gam H2O. Số este đồng phân của X là
A. 2.
B. 5.
C. 6.
D. 4.
![]() \(n_{CO_2}\) = 0,22/44 = 0,005 mol;
\(n_{CO_2}\) = 0,22/44 = 0,005 mol;
![]() \(n_{H_2O}\) = 0,09/18 = 0,005 mol;
\(n_{H_2O}\) = 0,09/18 = 0,005 mol;
→ ![]() \(n_{CO_2}\) =
\(n_{CO_2}\) = ![]() \(n_{H_2O}\) → este X no, đơn chức, mạch hở
\(n_{H_2O}\) → este X no, đơn chức, mạch hở
Gọi công thức phân tử X là CnH2nO2 ta có sơ đồ:
CnH2nO2 → ![]() \(n_{H_2O}\)
\(n_{H_2O}\)
14n+32 18n
0,11 0,09
→ Công thức phân tử của E là C4H8O2
→ Các đồng phân este của X là
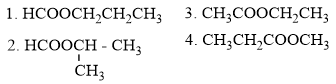
→ Có 4 đồng phân
→ Đáp án D
Câu 145: Đốt cháy 3 gam chất hữu cơ A được 4,4 gam CO2 và 1,8 gam nước. Công thức đơn giản nhất của A là
A. CH2O.
B. C3H6O.
C. C2H6O.
D. C2H4O.
![]() \(n_{H_2O}\) = 1,8/18 = 0,1 mol;
\(n_{H_2O}\) = 1,8/18 = 0,1 mol;
![]() \(n_{CO_2}\) = 4,4/44 = 0,1 mol;
\(n_{CO_2}\) = 4,4/44 = 0,1 mol;
Bảo toàn khối lượng ta có:
3 = mC + mH + mO → 3 = 0,1.12 + 0,1.2 + mO → mO = 1,6g
→ nO = 1,6/16 = 0,1 mol
→ nC : nH : nO = 0,1: (0,1.2) : 0,1 = 1: 2: 1
→ Công thức đơn giản nhất của A là CH2O
→ Đáp án A
Câu 146: Nếu A là một este đơn chức thì số đồng phân của A là
A. 1.
B. 2.
C. 3.
D. 4.
Nếu A là este đơn chức → Công thức phân tử của A là C2H4O2
→ Đồng phân este duy nhất của A là HCOOCH3
→ Đáp án A
Câu 147: Este X tạo bởi ancol no, đơn chức, mạch hở và axit cacboxylic không no (có 1 liên kết đôi) đơn chức, mạch hở. Đốt cháy a mol X thu được 22,4 lít CO2 (đktc) và 9 gam H2O. Giá trị của a là
A. 1.
B. 2.
C. 3.
D. 0,5.
![]() \(n_{CO_2}\) = 22,4/22,4 = 1 mol;
\(n_{CO_2}\) = 22,4/22,4 = 1 mol;
![]() \(n_{H_2O}\) = 9/18 = 0,5 mol;
\(n_{H_2O}\) = 9/18 = 0,5 mol;
Este X tạo bởi ancol no, đơn chức, mạch hở và axit cacboxylic không no (có 1 liên kết đôi C = C) đơn chức, mạch hở → Gọi công thức tổng quát của X là CnH2n-2O2
Ta có: ![]()
→ ![]() \(n_{C_nH_{2n-2}O_2}\) =
\(n_{C_nH_{2n-2}O_2}\) = ![]() \(n_{CO_2}\) -
\(n_{CO_2}\) - ![]() \(n_{H_2O}\) = 1 - 0,5 = 0,5 mol
\(n_{H_2O}\) = 1 - 0,5 = 0,5 mol
→ Đáp án D
Câu 148: Đốt cháy hoàn toàn m gam este đơn chức, no, mạch hở X thu được (m+7) gam CO2 và (m-6) gam H2O. Công thức cấu tạo của X có thể là:
A. HCOOCH3
B. HCOOC2H5.
C. CH3COOCH3
D. HCOOC2H3.
Đốt hoàn toàn m gam este đơn chức, no, mạch hở X → ![]() \(n_{H_2O}\) =
\(n_{H_2O}\) = ![]() \(n_{CO_2}\)
\(n_{CO_2}\)
![]() →
→ ![]() \(n_{CO_2}\) =
\(n_{CO_2}\) = ![]() \(n_{H_2O}\) = 0,5 mol
\(n_{H_2O}\) = 0,5 mol
BTKL: mO(X) = mX – mC - mH = 15 – 0,5.12 – 0,5.2 = 8 → nO(X) = 0,5 mol
→ nC : nH : nO = 0,5 : 1 : 0,5 = 1: 2:1
X là este đơn chức → X có CTPT là C2H4O2
→ Đáp án A
Câu 149: Khi đốt cháy hoàn toàn một este no, đơn chức, mạch hở Y thì số mol CO2 sinh ra bằng số mol O2 đã phản ứng. Tên gọi của este Y là
A. propyl axetat.
B. metyl axetat.
C. etyl axetat.
D. metyl fomat.
Gọi CTPT của este là Y CnH2nO2
Ta có: ![]()
![]() \(n_{O_2}\) =
\(n_{O_2}\) = ![]() \(n_{CO_2}\) → n = 3
\(n_{CO_2}\) → n = 3
→ Y là metyl axetat
→ Đáp án B
Câu 150: Đốt cháy hoàn toàn 1 thể tích hơi este đơn chức E phải dùng 2 thể tích O2 (đo ở cùng điều kiện). E là
A. este 2 lần este.
B. este không no.
C. metyl fomat.
D. etyl axetat.
Tỉ lệ về thể tích (đo ở cùng điều kiện) cũng chính là tỉ lệ về số mol
→ Vậy đốt cháy hoàn toàn 1 mol este đơn chức E phải dùng 2 mol O2
Gọi công thức phân tử của E là CxHyO2 (x ≥ 2) (1)
Ta có: ![]()
→ Bảo toàn nguyên tố O: ![]() \(2nC_xH_yO_2\) +
\(2nC_xH_yO_2\) + ![]() \(2n_{O_2}\) =
\(2n_{O_2}\) = ![]() \(2n_{CO_2}\) +
\(2n_{CO_2}\) + ![]() \(n_{H_2O}\)
\(n_{H_2O}\)
→ 2.1 + 2.2 = 2x + y/2 → 4x + y = 12 → 4x ≤ 12 → x ≤ 3 (2)
Từ (1) và (2) ![]()
→ Công thức phân tử của E là C2H4O2
→ E là HCOOCH3 (metyl fomat) là este no, đơn chức, mạch hở → Loại đáp án A, B, D
→ Đáp án C
- Xác định công thức phân tử Este dựa vào tỉ khối hơi
- Dạng bài tập phản ứng xà phòng hóa
- Bài tập tính khối lượng xà phòng
- Câu hỏi trắc nghiệm lý thuyết vai trò và ứng dụng của chất béo
- Câu hỏi trắc nghiệm lý thuyết về chất giặt rửa
- Dạng bài tập xác định chỉ số xà phòng hóa của chất béo
- Cách làm bài tập về chất béo
- Dạng bài tập về hiệu suất phản ứng Este hóa
- 150 câu trắc nghiệm Este Lipit có lời giải chi tiết (Cơ bản - phần 1)
- 150 câu trắc nghiệm Este Lipit có lời giải chi tiết (Cơ bản - phần 2)
- 150 câu trắc nghiệm Este Lipit có lời giải chi tiết (Cơ bản - phần 3)
Trên đây VnDoc đã giới thiệu tới các bạn 150 câu trắc nghiệm Este Lipit có lời giải chi tiết (Cơ bản - phần 4). Để có kết quả cao hơn trong học tập, VnDoc xin giới thiệu tới các bạn học sinh tài liệu Giải bài tập Toán lớp 12, Giải bài tập Hóa học lớp 12, Giải bài tập Vật Lí 12, Tài liệu học tập lớp 12 mà VnDoc tổng hợp và đăng tải. Mời các bạn cùng tham khảo thêm các môn Toán 12, Ngữ văn 12, tiếng Anh 12, đề thi học kì 1 lớp 12, đề thi học kì 2 lớp 12...
Mời bạn đọc cùng tham gia nhóm Tài liệu học tập lớp 12 của VnDoc.com để có thêm tài liệu học tập nhé.
