80 câu trắc nghiệm Đại cương về kim loại có lời giải chi tiết (Cơ bản - phần 1)
Câu hỏi trắc nghiệm Đại cương về kim loại có đáp án
Chuyên đề Hóa học 12 80 câu trắc nghiệm Đại cương về kim loại có lời giải chi tiết (Cơ bản - phần 1). Hy vọng tài liệu sẽ giúp các bạn học sinh giải bài tập Hóa học lớp 12 hiệu quả hơn. Mời các bạn tham khảo.
Câu 1: Công thức chung của oxit kim loại thuộc nhóm IIA là
A. R2O3.
B. RO2.
C. R2O.
D. RO.
Kim loại nhóm IIA có hóa trị II → Công thức chung của oxit kim loại thuộc nhóm IIA là RO.
→ Đáp án D
Câu 2: Nguyên tử Fe có cấu hình e là
A. [Ar]3d64s2.
B. [Ar]4s13d7.
C. [Ar]3d74s1.
D. [Ar]4s23d6.
Nguyên tử Fe có Z = 26 → Cấu hình e của Fe là 1s22s22p63s23p63d64s2 hay [Ar]3d64s2.
→ Đáp án A
Câu 3: Cấu hình e của Cr là
A. [Ar]3d44s2.
B. [Ar]4s23d4.
C. [Ar]3d54s1.
D. [Ar]4s13d5.
Nguyên tử Cr có Z = 24 (Có cấu hình bán bão hòa) → Cấu hình e của Cr là 1s22s22p63s23p63d54s1 hay [Ar]3d54s1.
→ Đáp án C
Câu 4: Kim loại Ni phản ứng được với tất cả các muối trong dung dịch ở dãy nào sau đây?
A. NaCl, AlCl3, ZnCl2
B. MgSO4, CuSO4, AgNO3
C. Pb(NO3)2, AgNO3, NaCl
D. AgNO3, CuSO4, Pb(NO3)2
Kim loại hoạt động có thể khử được ion kim loại kém hoạt động hơn trong dung dịch muối thành kim loại tự do.
Ni đứng trước Ag, Cu, Pb trong dãy điện hóa → Ni có thể khử được các ion kim loại trên.
Ni + 2AgNO3 → Ni(NO3)2 + 2Ag
Ni + CuSO4 → NiSO4 + Cu
Ni + Pb(NO3)2 → Ni(NO3)2 + Pb.
→ Đáp án D
Câu 5: Cho ba kim loại là Al, Fe, Cu và bốn dung dịch muối riêng biệt là ZnSO4, AgNO3, CuCl2, MgSO4. Kim loại nào tác dụng được với cả bốn dung dịch muối đã cho?
A. Al.
B. Fe.
C. Cu.
D. Không kim loại nào.
Không kim loại nào vì cả 3 kim loại đều đứng sau Mg trong dãy điện hóa → Cả 3 kim loại đều không khử được ion Mg2+ trong muối.
→ Đáp án D
Câu 6: Cho khí CO dư đi qua hỗn hợp gồm CuO, Al2O3 và MgO (nung nóng). Khi phản ứng xảy ra hoàn toàn thu được chất rắn gồm :
A. Cu, Al, Mg.
B. Cu, Al, MgO.
C. Cu, Al2O3, Mg.
D. Cu, Al2O3, MgO.
CO khử được các oxit kim loại của kim loại đứng sau Al trong dãy điện hóa thành kim loại và khí CO2.
→ CO chỉ khử được CuO thành Cu; Al2O3 và MgO không bị khử.
→ Đáp án D
Câu 7: Nguyên tử kim loại khi tham gia phản ứng hoá học có tính chất nào sau đây?
A. Nhường electron và tạo thành ion âm.
B. Nhường electron và tạo thành ion dương.
C. Nhận electron để trở thành ion âm.
D. Nhận electron để trở thành ion dương.
Nguyên tử kim loại khi tham gia phản ứng hóa học đóng vai trò chất khử → Nhường electron và tạo thành ion dương.
→ Đáp án B
Câu 8: Cặp chất không xảy ra phản ứng là
A. Fe + Cu(NO3)2.
B. Cu + AgNO3.
C. Zn + Fe(NO3)2.
D. Ag + Cu(NO3)2.
Ag đứng sau Cu trong dãy điện hóa → Ag không thể khử ion Cu2+.
→ Đáp án D
Câu 9: Dãy gồm các kim loại đều phản ứng với nước ở nhiệt độ thường tạo ra dung dịch có môi trường bazơ là:
A. Na, Ba, K.
B. Be, Na, Ca.
C. Na, Fe, K.
D. Na, Cr, K.
Các kim loại phản ứng với nước ở điều kiện thường tạo ra dung dịch có môi trường bazơ là: Li, Na, K, Ca, Ba. → Chỉ đáp án A thỏa mãn.
→ Đáp án A
Câu 10: Để loại bỏ kim loại Cu ra khỏi hỗn hợp bột gồm Ag và Cu, người ta ngâm hỗn hợp kim loại trên vào lượng dư dung dịch
A. AgNO3.
B. HNO3.
C. Cu(NO3)2.
D. Fe(NO3)2.
Ta ngâm vào lượng dư dung dịch AgNO3 vì Cu phản ứng với AgNO3 tạo thành dung dịch muối và đẩy kim loại Ag ra khỏi muối.
Cu + 2AgNO3 → Cu(NO3)2 + 2Ag.
→ Đáp án A
Câu 11: Những tính chất vật lí chung của kim loại (dẫn điện, dẫn nhiệt, dẻo, ánh kim) gây nên chủ yếu bởi
A. cấu tạo mạng tinh thể của kim loại.
B. khối lượng riêng của kim loại.
C. các electron độc thân trong tinh thể kim loại
D. các electron tự do trong tinh thể kim loại.
Những tính chất vật lí chung của kim loại (dẫn điện, dẫn nhiệt, dẻo, ánh kim) gây nên chủ yếu bởi các e tự do trong tinh thể kim loại.
→ Đáp án D
Câu 12: So với nguyên tử phi kim cùng chu kì, nguyên tử kim loại
A. thường có bán kính nguyên tử nhỏ hơn.
B. thường có năng lượng ion hoá nhỏ hơn.
C. thường dễ nhận electron trong các phản ứng hoá học.
D. thường có số electron ở các phân lớp ngoài cùng nhiều hơn.
So với nguyên tử phi kim cùng chu kì, nguyên tử kim loại thường có năng lượng ion hóa nhỏ hơn.
→ Đáp án B
Câu 13: Kim loại nào sau đây có tính dẫn điện tốt nhất trong tất cả các kim loại?
A. Vàng
B. Bạc
C. Đồng
D. Nhôm
Kim loại dẫn điện tốt nhất là bạc (Ag).
→ Đáp án B
Câu 14: Kim loại nào sau đây dẻo nhất trong tất cả các kim loại?
A. Vàng
B. Bạc
C. Đồng
D. Nhôm
Kim loại dẻo nhất trong tất cả các kim loại là vàng (Au).
→ Đáp án A
Câu 15: Kim loại nào sau đây có độ cứng lớn nhất trong tất cả các kim loại?
A. Vonfam
B. Crom
C. Sắt
D. Đồng
Kim loại có độ cứng lớn nhất trong tất cả các kim loại là crom (Cr).
→ Đáp án B
Câu 16: Kim loại nào sau đây là kim loại mềm nhất trong tất cả các kim loại?
A. Liti
B. Xesi
C. Natri
D. Kalim
Kim loại mềm nhất trong tất cả các kim loại là Xesi (Xe).
→ Đáp án B
Câu 17: Kim loại có nhiệt độ nóng chảy cao nhất trong tất cả các kim loại?
A. Vonfam
B. Đồng
C. Sắt
D. Kẽm
Kim loại có nhiệt độ nóng chảy cao nhất trong tất cả các kim loại Vonfam.
→ Đáp án A
Câu 18: Kim loại nào sau đây nhẹ nhất (có khối lượng riêng nhỏ nhất) trong tất cả các kim loại
A. Liti
B. Rubidi
C. Natri
D. Kali
Kim loại nhẹ nhất (khối lượng riêng nhỏ nhất) trong tất cả các kim loại là Li (D = 0,5g/cm3).
→ Đáp án A
Câu 19: Bao nhiêu gam clo tác dụng vừa đủ kim loại nhôm tạo ra 26,7 gam AlCl3?
A. 21,3 gam
B. 12,3 gam.
C. 13,2 gam.
D. 23,1 gam.
2Al + 3Cl2 → 2AlCl3
Theo bài ta có: nAlCl3 = 26,7/133,5 = 0,2 mol
Theo phương trình ta có: nCl2 = 3nAlCl3/2 = 0,3 mol
Khối lượng clo cần là: mCl2 = 0,3.71 = 21,3 g
→ Đáp án A
Câu 20: Một thanh kim loại M hóa trị 2 được nhúng vào trong 1 lít dung dịch CuSO4 0,5M. Sau khi lấy thanh M ra và cân lại, thấy khối lượng thanh tăng 1,6 gam, nồng độ CuSO4 còn 0,3M. Hãy xác định kim loại M?
A. Fe
B. Mg
C. Zn
D. Pb
M + Cu2+ → M2+ + Cu
Số mol Cu2+ phản ứng là: 1(0,5 – 0,3) = 0,2 mol
Độ tăng khối lượng của thanh kim loaị M:
M = mCu – mM tan = 0,2(64 – M) = 1,6
Suy ra: M = 56 là Fe
→ Đáp án A
Câu 21: Ngâm một lá kẽm trong 100ml dung dịch AgNO3 0,1 mol. Kết thúc phản ứng, khối lượng lá kẽm là bao nhiêu?
A. 0,655g
B. 0,75g
C. 0,65g
D. 0,755g
Ta có: nAgNO3 = 0,01 mol.
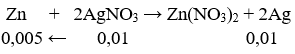
mAg = 0,01. 108 = 1,08g.
Đặt mZn = a ⇒ a = 1,08 – (0,005.65) = 0,755g.
→ Đáp án D
Câu 22: Cho 8,4 g Fe vào dung dịch có chứa 0,4mol AgNO3. Kết thúc phản ứng, khối lượng bạc là bao nhiêu?
A. 42,3g
B. 23,4g
C. 43,2g
D. 21,6g
Ta có: nFe = 0,15 mol, nAgNO3 = 0,4mol.
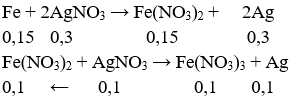
Suy ra: mAg = (0,1+ 0,3).108 = 43,2g.
→ Đáp án C
Câu 23: Cho biết các cặp oxi hoá - khử sau: Fe2+/Fe; Cu2+/Cu; Fe3+/Fe2+
Tính oxi hoá tăng dần theo thứ tự
A. Cu2+, Fe2+, Fe3+
B. Cu2+, Fe3+,Fe2+
C. Fe3+,Cu2+, Fe2+
D. Fe2+,Cu2+, Fe3+
Tính oxi hoá tăng dần từ trái sang phải: Fe2+,Cu2+, Fe3+.
→ Đáp án D
Câu 24: Muốn khử dd chứa Fe3+ thành dd có chứa Fe2+ cần dùng kim loại sau:
A. Cu
B. Na
C. Zn
D. Ag
2Fe3+ + Cu → Cu2+ + 2Fe2+
→ Đáp án A
Câu 25: Cho các kim loại: Fe, Al, Mg, Cu, Zn, Ag. Số kim loại tác dụng được với dd H2SO4 loãng là:
A. 5
B. 3
C. 6
D. 4
Kim loại đứng trước H trong dãy điện hoá tác dụng được với dung dịch axit H2SO4 loãng: Fe, Al, Mg, Zn.
→ Đáp án D
Câu 26: Ngâm Cu dư vào dd AgNO3 thu được dd X, sau đó ngâm Fe dư vào dung dịch X thu được dung dịch Y. dung dịch Y gồm:
A. Fe(NO3)2
B. Fe(NO3)2, Cu(NO3)2, AgNO3
C. Fe(NO3)2, Cu(NO3)2
D. Fe(NO3)3
Ngâm Cu dư vào dd AgNO3, Ag bị đẩy hết ra khỏi muối, muối mới là Cu(NO3)2 (dd X).
Cu + 2AgNO3 → Cu(NO3)2 + 2Ag
Ngâm Fe dư vào dung dịch X, Cu bị đẩy hết ra khỏi muối tạo muối mới là Fe(NO3)2.
Fe + Cu(NO3)2 → Fe(NO3)2 + Cu
→ Đáp án A
Câu 27: Ngâm đinh sắt sạch trong 200 ml dd CuSO4. Sau phản ứng kết thúc lấy đinh sắt ra rửa nhẹ và làm khô thấy khối lượng đinh sắt tăng 8 gam. Nồng độ CuSO4 ban đầu là:
A. 0,52 M
B. 0,5 M
C. 5 M
D. 0,25 M
Gọi số mol Fe phản ứng là x mol.
→ mtăng = 64x – 56x = 8 → x = 1 mol
→ nCuSO4 = x = 1 mol → CM(CuSO4) = 1/0,2 = 5M
→ Đáp án C
Câu 28: Cho 4 dung dịch muối: CuSO4, K2SO4, NaCl, KNO3. Dung dịch nào sau khi điện phân cho ra một dung dịch axit (điện cực trơ)
A. CuSO4
B. K2SO4
C. NaCl
D. KNO3
2NaCl + 2H2O -Dp→ 2NaOH + Cl2 + H2
CuSO4 + H2O -Dp→ Cu + H2SO4 + 0,5O2
Điện phân dung dịch KNO3 và K2SO4 thực chất là quá trình điện phân nước
2H2O -Dp→ 2H2 + O2.
→ Đáp án A
Câu 29: Cho các kim loại sau: K, Ba, Cu và Ag. Số kim loại điều chế được bằng phương pháp điện phân dung dịch (điện cực trơ) là:
A. 3
B. 1
C. 2
D. 4
Điện phân dung dịch dùng để điều chế những kim loại trung bình hoặc yếu như Cu, Ag.
→ Đáp án C
Bài 30: Trong công nghiệp, kim loại nào sau đây được điều chế bằng phương pháp điện phân nóng chảy?
A. Fe
B. Cu
C. Mg
D. Ag
Phương pháp điện phân nóng chảy dùng để điều chế các kim loại từ nhôm trở về trước.
VD: K, Na, Mg…
→ Đáp án C
Câu 31: Trong quá trình điện phân, các muối X- (X: Cl-, Br-) di chuyển về:
A. Cực dương và bị oxi hóa
B. Cực âm và bị oxi hóa
C. Cực dương và bị khử
D. Cực âm và bị khử
Ion âm bị hút về cực dương (hay di chuyển về cực dương) và bị khử: 2X- + 2e → X2
→ Đáp án C
Câu 32: Cho dung dịch chứa các ion: Na+, K+, Cu+, Cl-, SO42-, NO32-. Các ion nào không bị điện phân khi ở trạng thái dung dịch:
A. Na+, K+, Cl-, SO42-
B. K+, Cu+, Cl-, NO32-
C. Na+, Cu+, Cl-, SO42-
D. Na+, K+, SO42-, NO32-
Ion của kim loại mạnh như: K, Na, Li, Ca… và ion của các gốc muối có oxi như: SO42-, NO3- không bị điện phân. → Chọn D.
→ Đáp án D
Câu 33: Điện phân một lượng dư dung dịch MgCl2 (điện cực trơ, có màng ngăn xốp bao điện cực) với cường độ dòng điện 2,68A trong 2 giờ. Sau khi dừng điện phân khối lượng dung dịch giảm m gam, giả thiết nước không bay hơi, các chất tách ra đều khan. Giá trị của m là:
A. 8,7
B. 18,9
C. 7,3
D. 13,1.
Phản ứng: MgCl2 + 2H2O -đpdd Mg(OH)2 + H2 + Cl2
- Ta có: ne trao đổi = It/F = 0,2 mol
→ nMgCl2 = nCl2 = nH2 = ne/2 = 0,1 mol
→ mdd giảm = 58nMg(OH)2 + 2nH2 + 71nCl2 = 13,1 gam
→ Đáp án D
Câu 34: Điện phân nóng chảy hoàn toàn 1,9g muối clorua của kim loại M được 0,48g kim loại M ở catot. Kim loại M là:
A. Zn
B. Ca
C. Mg
D. Ba
Gọi muối cần tìm là MCln.
Bảo toàn khối lượng ta có:
mCl2 = mMCln - mM = 1,9 - 0,48 = 1,42 gam → nCl2 = 1,42/71 = 0,02 mol
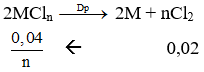
Theo bài ta có: ![]()
Vậy M là Mg.
→ Đáp án C
Câu 35: Điện phân một dd muối MCln với điện cực trơ. Khi ở catot thu được 16g kim loại M thì ở anot thu được 5,6 lít khí (đktc). Kim loại M là:
A. Mg
B. Fe
C. Cu
D. Ca
nM = 16/M mol; nCl2 = 5,6/22,4 = 0,25 mol
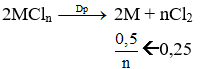
![]() ⇔ M = 32n ⇒ n = 2; M = 64
⇔ M = 32n ⇒ n = 2; M = 64
Kim loại M là Cu.
→ Đáp án C
Câu 36: Nếu muốn điện phân hoàn toàn (mất màu xanh) 400 ml dung dịch CuSO4 0,5M với cường độ dòng điện I = 1,34A (hiệu suất điện phân là 100%) thì cần bao nhiêu thời gian.
A. 6 giờ
B. 7 giờ
C. 8 giờ
D. 9 giờ
nCuSO4 = 0,5. 0,4 = 0,2 mol
ne trao đổi = 2.0,2 = 0,4 mol
→ Đáp án C
Câu 37: Điện phân dung dịch muối CuSO4 dư trong thời gian 1930 giây, thu được 1,92 gam Cu ở catot. Cường độ dòng điện trong quá trình điện phân là giá trị nào dưới đây:
A. 3A
B. 4,5A
C. 1,5A
D. 6A
Ta có: ![]()
Với F = 96500 C/mol ta có: ![]()
→ Đáp án A
Câu 38: Điện phân hòa toàn 2,22 gam muối clorua kim loại ở trạng thái nóng chảy thu được 448 ml khí (ở đktc) ở anot. Kim loại trong muối là:
A. Na
B. Ca
C. K
D. Mg
nCl2 = 0,02 mol
Tại catot: Mn+ + ne → M
Theo định luật bảo toàn khối lượng mM = m(muối) – mCl2 = 2,22 – 0,02.71 = 0,8 gam
Tại anot: 2Cl- → Cl2 + 2e
Theo định luật bảo toàn mol electron ta có: nM = 0,04/n → M = 20.n → n = 2 và M là Ca
→ Đáp án B
Câu 39: Điện phân 250g dd CuSO4 8% đến khi nồng độ CuSO4 trong dd thu được giảm đi và bằng một nửa so với trước phản ứng thì dừng lại. Khối lượng kim bám ở catot gần với giá trị nào?
A. 4,08g
B. 2,04g
C. 4,58g
D. 4,5g
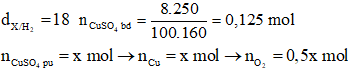
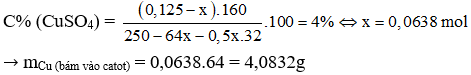
→ Đáp án A
Câu 40: Điện phân dung dịch CuCl2, điện cực trơ bằng dòng điện 5A trong 45 phút 20 giây. Tính khối lượng kim loại sinh ra ở Catot và V lít (đktc) khí sinh ra ở Anot.
A. 4,512g
B. 4,5g
C. 4,6g
D. 4,679g
Phương trình điện phân:
CuCl2 -đpdd→ Cu + Cl2↑
Áp dụng công thức Faraday:
→ Đáp án A
Mời các bạn tham khảo thêm các bài viết dưới đây của chúng tôi:
- Lý thuyết: Điều chế kim loại
- Lý thuyết: Luyện tập sự điện phân - Sự ăn mòn kim loại - Điều chế kim loại
- Tính chất chung của kim loại
- Chuỗi phản ứng hóa học của kim loại
- Các dạng bài tập về dãy điện hóa kim loại và pin điện hóa
- Phương pháp giải các bài toán về kim loại
- Kim loại tác dụng với dung dịch axit
- Kim loại tác dụng với dung dịch muối
Trên đây VnDoc đã giới thiệu tới các bạn 80 câu trắc nghiệm Đại cương về kim loại có lời giải chi tiết (Cơ bản - phần 1). Để có kết quả cao hơn trong học tập, VnDoc xin giới thiệu tới các bạn học sinh tài liệu Giải bài tập Toán lớp 12, Giải bài tập Hóa học lớp 12, Giải bài tập Vật Lí 12, Tài liệu học tập lớp 12 mà VnDoc tổng hợp và đăng tải.
