Lý thuyết Este: Tính chất hóa học, Tính chất vật lí, Cấu tạo, Điều chế, Ứng dụng
VnDoc xin giới thiệu tới bạn đọc Lý thuyết Este: Tính chất hóa học, Tính chất vật lí, Cấu tạo, Điều chế, Ứng dụng. Nội dung tài liệu sẽ giúp các bạn học sinh đạt kết quả Hóa học 12 cao hơn. Mời các bạn tham khảo.
Lý thuyết Este
I. Cấu tạo, phân loại Este
1. Cấu tạo
Khi thay nhóm –OH ở nhóm cacboxyl của axit cacboxylic bằng nhóm –OR thì được este.
Este đơn giản có công thức cấu tạo như sau:
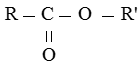 với R, R’ là gốc hiđrocacbon no, không no hoặc thơm (trừ trường hợp este của axit fomic)
với R, R’ là gốc hiđrocacbon no, không no hoặc thơm (trừ trường hợp este của axit fomic)
Este là dẫn xuất của axit cacboxylic. Một vài dẫn xuất khác của axit cacboxylic có công thức cấu tạo như sau:
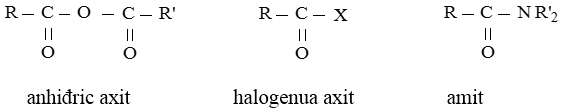
2. Phân loại:
a. Este no, đơn chức:
Công thức phân tử: CmH2mO2 hay CnH2n + 1COOCn'H2n' + 1
Với m ≥ 2; m = n + n’ + 1; n ≥ 0, n’ ≥ 1.
b. Este không no, đơn chức:
Este đơn chức, mạch hở, không no có 1 nối đôi: CmH2m - 2O2
+ Este tạo từ axit không no, ancol no: CnH2n - 1COOCn'H2n' + 1
Với n ≥ 2; n’ ≥ 1; m ≥ 4
+ Este tạo từ axit no, ancol không no: CnH2n + 1COOCn'H2n' - 1
Với n ≥ 0; n’ ≥ 2; m ≥ 3 (n = 0 ⇒ HCOOCn'H2n' + 1)
c. Este đa chức
+ Tạo bởi axit đơn chức và rượu đa chức có dạng: (RCOO)mR’ (nếu gốc R’ là gốc glixerol thì este có dạng lipit (RCOO)3C3H5 với R là gốc axit béo).
+ Tạo bởi axit đa chức và rượu đơn chức có dạng:
R(COOR’)n (n ≥ 2; R ≥ 0).
+) Tạo bởi axit đa chức R(COOH)n và rượu đa chức R’(OH) có dạng Rm(COO)nmR’n.
Nếu m = n thì tạo este vòng có dạng R(COO)nR’.
II. Danh pháp Este
Tên este = Tên gốc hiđrocacbon R’ + tên anion gốc axit (đuôi at)
- Tên 1 số gốc axit thường gặp:
HCOOH: Axit Fomic ⇒ HCOO-: Fomat
CH3COOH: Axit Axetic ⇒ CH3COO-: Axetat
CH2=CHCOOH: Axit Acrylic ⇒ CH2=CHCOO-: Acrylat
C6H5COOH: Axit Benzoic ⇒ C6H5COO-: Benzoat
- Tên gốc R’:
CH3-: metyl; C2H5-: etyl; CH2=CH-: Vinyl
Ví dụ

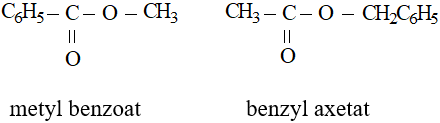
a. Với ancol đơn chức R’OH:
Tên este = tên gốc hidrocacbon R’+ tên gốc axit (đổi đuôi ic thành at)
Ví dụ:
CH3COOC2H5: etyl axetat
CH2=CH-COO-CH3: metyl acrylat
b. Với ancol đa chức:
Tên este = tên ancol + tên gốc axit
Ví dụ: (CH3COO)2C2H4: etylenglicol điaxetat
c. Với axit đa chức
Gọi theo tên riêng của từng este.
Ví dụ: C3H5(COOC17H33)3: triolein (C17H33COOH: axit oleic)
C3H5(COOC17H35)3: tristearin (C17H35COOH: axit stearic)
III. Tính chất vật lý Este
1. Trạng thái: Đa số ở trạng thái lỏng. Những este có KLPT rất lớn có thể ở trạng thái rắn (như mỡ động vật, sáp ong …).
2. Nhiệt độ sôi: Thấp, dễ bay hơi do không tạo liên kết hidro giữa các phân tử.
3. Tính tan: Ít tan hoặc không tan trong nước do không tạo liên kết hidro giữa các phân tử với nước.
* Đa số các este có mùi thơm đặc trưng:
+ isoamyl axetat (CH3COOCH2CH2(CH3)2): mùi thơm của chuối.
+ Etyl isovalerat ((CH3)2CHCH2COOC2H5): mùi táo.
+ Etyl butirat (CH3CH2CH2COOC4H9): mùi thơm của dứa.
+ Geranyl axetat (CH3COOC10H17): mùi hoa hồng …
+ Benzyl propionat: CH3CH2COO-CH2C6H5: mùi hoa nhài.
IV. Tính chất hóa học Este
1. Phản ứng ở nhóm chức
a. Phản ứng thủy phân
Este bị thủy phân cả trong môi trường axit và trong môi trường kiềm. Thủy phân este trong môi trường axit là phản ứng nghịch với phản ứng este hóa:
![]()
Ví dụ:
![]()
Phản ứng thủy phân trong môi trường kiềm là phản ứng một chiều và còn được gọi là phản ứng xà phòng hóa:
![]()
Ví dụ:
![]()
Chú ý: Nếu este dạng lipit (chất béo) khi xà phòng hóa, ta thu được glixerol C3H5(OH)3và xà phòng.
![]()
* Một số phản ứng thuỷ phân đặc biệt của este
Căn cứ vào sản phẩm của phản ứng thủy phân este ta có thể suy đoán cấu tạo của este ban đầu.
Dưới đây là một số trường hợp thuỷ phân đặc biệt của este (không chứa halogen) thường gặp trong bài toán định lượng là:
![]()
⇒ X là este của phenol, có công thức là C6H5OOC–R
![]()
⇒X là este đơn chức, có công thức là R–COO–CH=CH–R’
![]()
![]()
⇒ X là este - axit, có công thức là HOOC–R–COOR’
![]()
⇒ X hiđroxi - este, có công thức là RCOOCH(OH)–R’
![]()
⇒ X hiđroxi - este, có công thức là RCOOC(R)(OH)–R’
![]()
hoặc “mchất rắn = meste + mNaOH ” hoặc “msản phẩm = meste + mNaOH ”
⇒ X là este vòng (được tạo bởi hiđroxi axit, ví dụ:
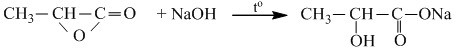
b. Phản ứng khử
Este bị khử bởi liti nhôm hiđrua (LiAlH4), khi đó nhóm RCO– (gọi là nhóm axyl) trở thành ancol bậc I:
![]()
2. Phản ứng ở gốc hiđrocacbon
Este có thể tham gia phản ứng thế, cộng, tách, trùng hợp,... Sau đây chỉ xét phản ứng cộng và phản ứng trùng hợp.
a. Phản ứng cộng vào gốc không no: Gốc hiđrocacbon không no ở este có phản ứng cộng với H2, Br2, Cl2, ... giống hiđrocacbon không no. Ví dụ:
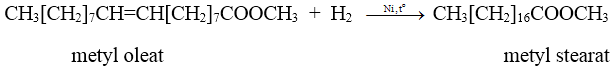
b. Phản ứng trùng hợp: Một số este đơn giản có liên kết C = C tham gia phản ứng trùng hợp giống như anken.
V. Điều chế - ứng dụng Este
1. Điều chế
a. Phản ứng giữa axit và rượu
- Từ axit đơn chức và rượu đơn chức:
![]()
Ví dụ:
![]()
- Từ axit đơn chức và rượu đa chức:
![]()
Ví dụ:
![]()
- Từ axit đa chức và rượu đơn chức:
![]()
Ví dụ:
![]()
- Từ axit đa chức và rượu đa chức:
![]()
Ví dụ:
![]()
b. Phản ứng giữa anhiđric axit và rượu
![]()
Ví dụ:
![]()
Đây là phản ứng để điều chế este của phenol do este của phenol không điều chế được bằng axit cacboxylic.
c. Phản ứng giữa axit và hiđrocacbon chưa no
![]()
Ví dụ:
![]()
d. Phản ứng giữa muối natri của axit và dẫn xuất halogen
![]()
Ví dụ:
![]()
2. Ứng dụng
Este có khả năng hòa tan tốt các chất hữu cơ, kể cả hợp chất cao phân tử, nên được dùng làm dung môi (ví dụ: butyl và amyl axetat được dùng để pha sơn tổng hợp).
Poli (metyl acrylat) và poli (metyl metacrylat) dùng làm thủy tinh hữu cơ. Poli (vinyl axetat) dùng làm chất dẻo, hoặc thủy phân thành poli (vinyl ancol) dùng làm keo dán. Một số este của axit phtalic được dùng làm chất hóa dẻo, làm dược phẩm.
Một số este có mùi thơm của hoa quả được dùng trong công nghiệp thực phẩm (bánh kẹo, nước giải khát) và mĩ phẩm (xà phòng, nước hoa,...).
VI. Nhận biết Este
- Este của axit fomic có khả năng tráng gương.
- Các este của ancol không bền bị thủy phân tạo anđehit có khả năng tráng gương.
- Este không no có phản ứng làm mất màu dung dịch Brom.
- Este của glixerol hoặc chất béo khi thủy phân cho sản phẩm hòa tan Cu(OH)2.
Trên đây VnDoc đã giới thiệu tới các bạn Lý thuyết Este: Tính chất hóa học, Tính chất vật lí, Cấu tạo, Điều chế, Ứng dụng. Để có kết quả cao hơn trong học tập, VnDoc xin giới thiệu tới các bạn học sinh tài liệu Giải bài tập Toán lớp 12, Giải bài tập Hóa học lớp 12, Giải bài tập Vật Lí 12, Tài liệu học tập lớp 12 mà VnDoc tổng hợp và đăng tải.
