Bài tập lý thuyết Amine
Lý thuyết amine
Lớp:
Lớp 12
Môn:
Hóa Học
Bộ sách:
Kết nối tri thức với cuộc sống
Loại File:
PDF
Phân loại:
Tài liệu Tính phí
Trang chủ: https://vndoc.com/ | Zalo: 0936.120.169
CHỦ ĐỀ 3
HỢP CHẤT NITROGEN
AMINE
A. TÓM TẮT LÝ THUYẾT
I. KHÁI NIỆM, PHÂN LOẠI, ĐỒNG PHÂN, DANH PHÁP
1. Khái niệm
Amine là dẫn xuất của ammonia, trong đó nguyên tử hydrogen của phân tử ammonia được
thay thế bằng gốc hydrocarbon.
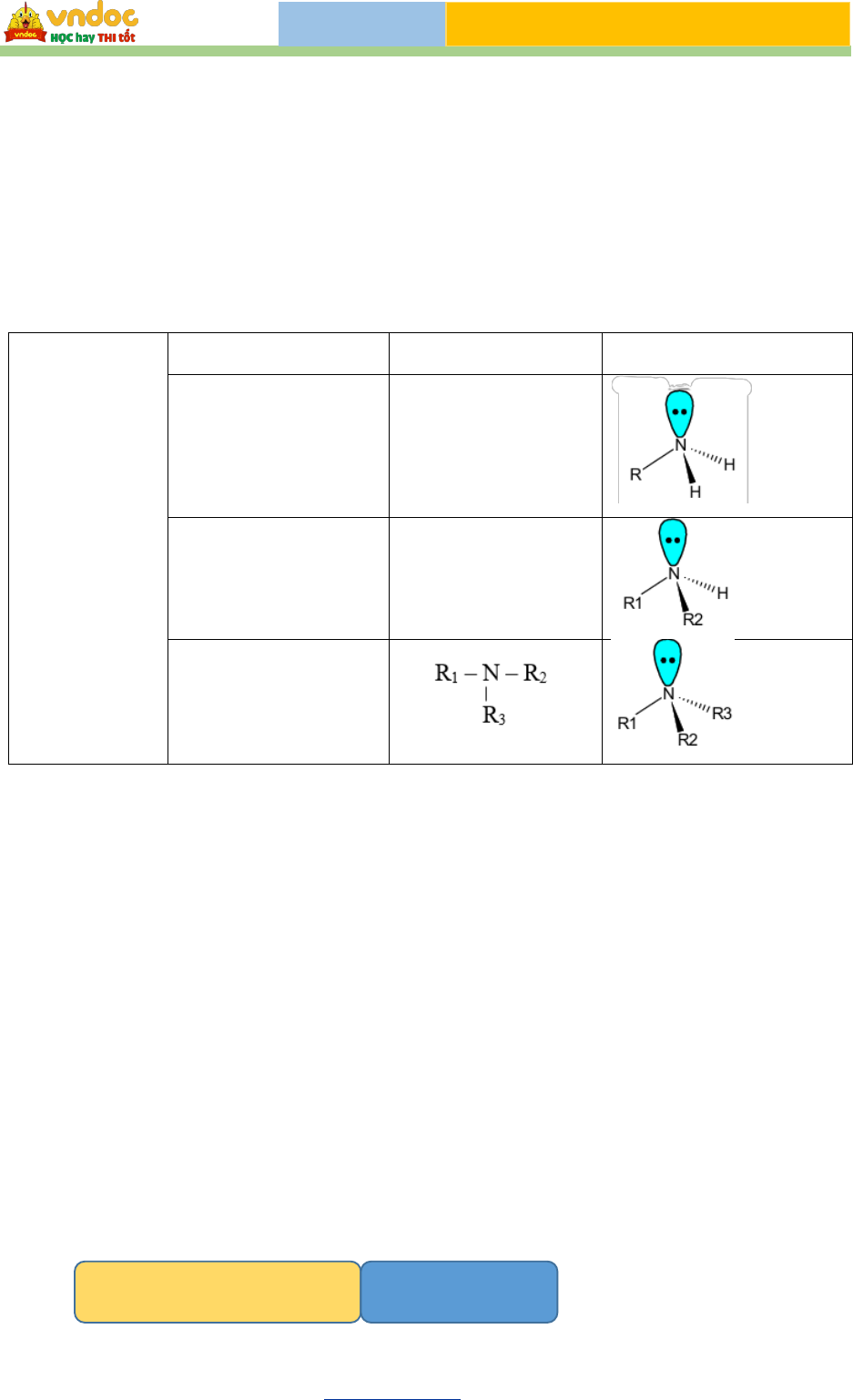
Phân tử NH
3
Số H bị thay thế
Công thức chung
Công thức phối cảnh
Thay 1H = R
R-NH
2
amine bậc 1
Thay 2H = R
1
, R
2
R
1
- NH- R
2
amine bậc 2
Thay 3H = R
1
, R
2
,
R
3
2. Phân loại
Amine thường được phân loại theo bậc của amine và bản chất gốc hydrocarbon.
Bậc amine được tính bằng số gốc hydrocarbon liên kết trực tiếp với nguyên tử nitrogen.
Theo đó, amine được phân loại thành amine bậc một, amine bậc hai và amine bậc ba.
Dựa trên đặc điểm cấu tạo của gốc hydrocarbon
+ alkylamine (N gắn với gốc alkyl): CH
3
NH
2
, C
2
H
5
NH
2
,…
+ arylamine (N liên kết trực tiếp C vòng benzene) : C
6
H
5
NH
2
,..
3. Đồng phân
Các amine có từ hai nguyên tử carbon trong phân tử bắt đầu xuất hiện hiện tượng đồng
phân. Amine có thể có các đồng phân: bậc amine, mạch carbon và vị trí nhóm amine.
4. Danh pháp
- Tên pháp gốc – chức:
+
Ví dụ: CH
3
NH
2
(Methylamine), C
2
H
5
–NH
2
(Ethylamine)…
Tên gốc hydrocarbon
Amine
Trang chủ: https://vndoc.com/ | Zalo: 0936.120.169
CHỦ ĐỀ 3
HỢP CHẤT NITROGEN
- Tên thay thế:
+ Tên amine bậc một:
Ví dụ: C
2
H
5
–NH
2
(Etanamine), CH
3
CH(NH
2
)CH
3
(Propan - 2- amine) ...
+ Tên amine bậc hai:
Ví dụ: CH
3
CH
2
NHCH
3
: N-methylethanamine.
+ Tên amine bậc ba
Ví dụ:
(CH
3
)
3
N: N,N-dimethylmethanamine.
Ngoài ra, một số amine có tên riêng, chẳng hạn C
6
H
5
– NH
2
có tên riêng là aniline.
II. TÍNH CHẤT VẬT LÍ
Giữa các phân tử amine bậc một hoặc amine bậc hai hình thành liên kết hydrogen liên
phân tử, ảnh hưởng đến nhiệt độ nóng chảy, nhiệt độ sôi của amine. Giữa phân tử amine
với phân tử nước hình thành liên kết hydrogen, ảnh hưởng đến độ tan trong nước của
amine.
+ Ở điều kiện thường, amine có thể ở thể khí, thể lỏng hoặc thể rắn.
+ Nhiệt độ nóng chảy, nhiệt độ sôi của các amine cùng bậc có xu hướng tăng khi phân tử
khối tăng.
+ Các amine có số nguyên tử carbon nhỏ thường tan nhiều trong nước.
IV. TÍNH CHẤT HÓA HỌC
- Trong phân tử amine:
N còn một cặp e chưa liên kết =>có thể tạo ra liên kết cho nhận
(giống NH
3
)
do đó các amine có tính chất hóa học tương tự ammonia.
1. Tính base của nhóm NH
2
Tên gốc hydrocarbon
Amine
– số chỉ vị trí nhóm amine
Tên gốc hydrocarbon
mạch nhanh (bỏ kí tự e)
N-Tên gốc
hydrocarbon
– số chỉ vị trí
nhóm amine
Amine
N-Tên gốc
Hydrocarbon thứ nhất –N-
tên hydrocabon thứ hai
Tên gốc
hydrocarbon mạch
nhanh (bỏ kí tự e)
– số chỉ vị trí
nhóm amine
Amine
Trang chủ: https://vndoc.com/ | Zalo: 0936.120.169
CHỦ ĐỀ 3
HỢP CHẤT NITROGEN
- Trong dung dịch, amine phản ứng với H
2
O tạo ra ion ammonium và ion hydroxide.
RNH
2
+ H
2
O ⇌ RNH
3
+
+ OH
-
- Phương trình hóa học của các phản ứng thể hiện tính base của amine:
CH
3
NH
2
+ HCl → CH
3
NH
3
Cl
3CH
3
NH
2
+ 3H
2
O + FeCl
3
→ 3CH
3
NH
3
Cl + Fe(OH)
3
↓
- Tính base của aniline yếu hơn methylamine và dung dịch aniline không làm đổi màu quỳ
tím.
2. Phản ứng với nitrous acid (H-O-N=O)
Amine phản ứng với nitrous acid, sản phẩm phụ thuộc vào bậc của amine, bản chất của
gốc hydrocarbon, điều kiện tiến hành,...
+ Phản ứng của alkylamine bậc một với nitrous acid sinh ra nitrogen và alcohol.
+ Aniline phản ứng với nitrous ở nhiệt độ thấp tạo ra muối diazonium, là chất trung gian
quan trọng trong tổng hợp nhiều chất hữu cơ.
Ví dụ:
- Ethylamine phản ứng với HNO
2
, sinh ra nitrogen và ethanol.
CH
3
CH
2
NH
2
+ HNO
2
→ CH
3
CH
2
OH + N
2
↑ + H
2
O
- Aniline phản ứng với HNO
2
ở nhiệt độ thấp (0-5 °C) sinh ra muối diazonium.
C
6
H
5
NH
2
+ HNO
2
+ HCl
o
0 5 C
[C
6
H
5
N
2
]
+
Cl
-
+ 2H
2
O
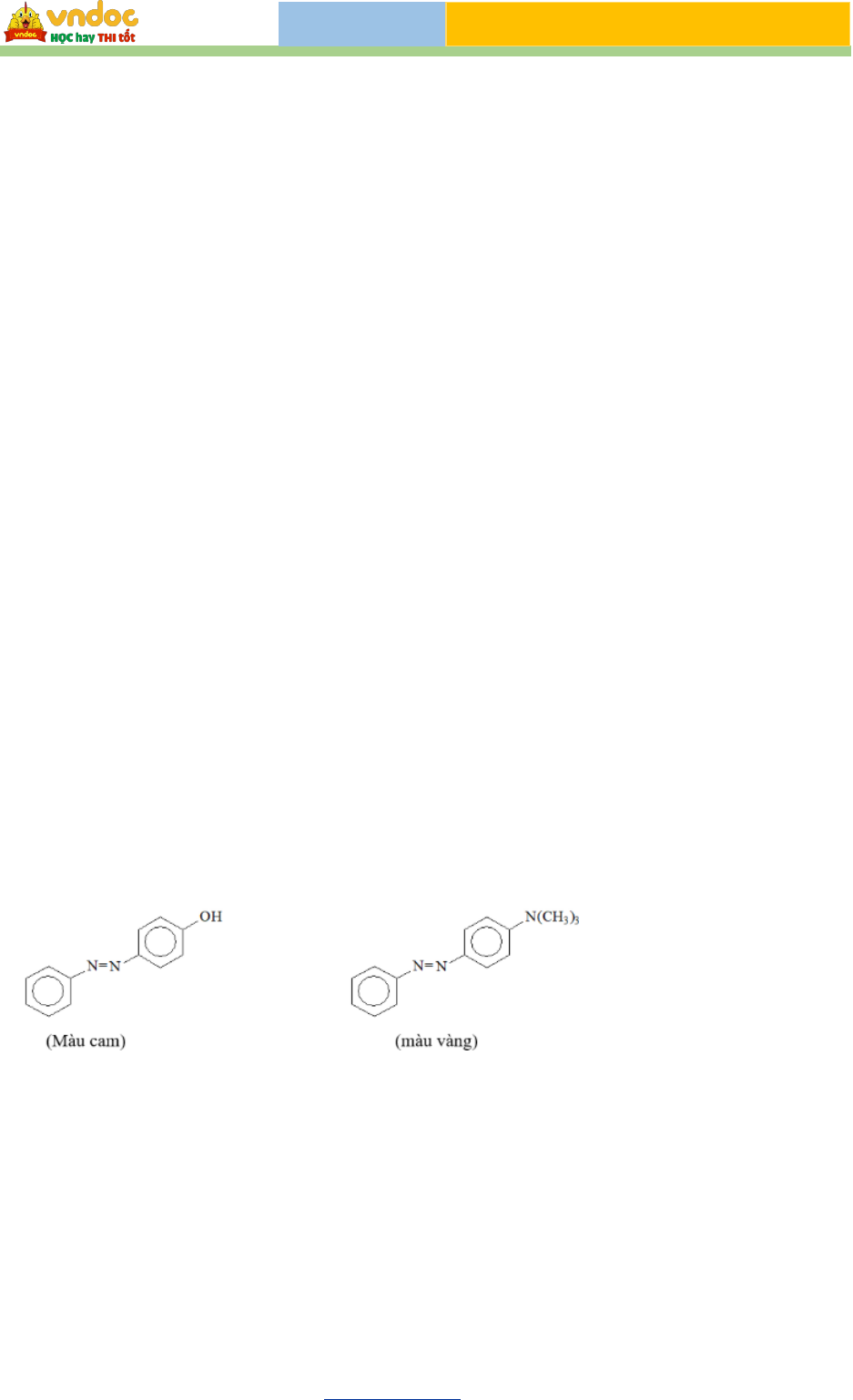
Diazonium tham gia phản ứng ghép nối với phenol hoặc arylamine tạo ra hợp chất azo có
màu, được sử dụng làm thuốc nhuộm
3. Phản ứng ở nhân thơm của aniline
Khi tham gia phản ứng thế nguyên tử hydrogen của vòng benzene, phân tử aniline ưu tiên
thế nguyên tử hydrogen ở các vị trí 2,4, 6.
Phương trình hoá học của phản ứng aniline tác dụng với bromine:
Bài tập lý thuyết Amine có lời giải
Lý thuyết amine là một chuyên đề quan trọng trong Hóa học hữu cơ, cung cấp kiến thức về cấu tạo, phân loại, tính chất vật lý và hóa học của nhóm hợp chất này. Amine có vai trò lớn trong đời sống và công nghiệp, từ sản xuất thuốc, phẩm nhuộm đến chế tạo polymer. Nắm vững lý thuyết amine giúp học sinh dễ dàng vận dụng vào giải bài tập, đặc biệt trong giai đoạn ôn thi THPT Quốc gia. Bài viết này sẽ hệ thống hóa đầy đủ kiến thức, kèm ví dụ minh họa và bài tập luyện tập để bạn học nhanh – nhớ lâu.
