Đề kiểm tra 45 phút học kì 1 môn Hóa học lớp 9 trường THCS Văn Miếu, Thanh Sơn năm 2014 - 2015
Đề kiểm tra 45 phút học kì 1 môn Hóa học lớp 9
Đề kiểm tra 45 phút học kì 1 môn Hóa học lớp 9 trường THCS Văn Miếu, Thanh Sơn năm 2014 - 2015 là đề kiểm tra 1 tiết học kì 1 lớp 9 môn Hóa học có đáp án dành cho các bạn học sinh lớp 9 tham khảo chuẩn bị cho kì thi cuối học kì I sắp tới. Mời các bạn tải tài liệu về tham khảo.
Đề thi khảo sát chất lượng đầu năm môn Toán lớp 9 trường THCS Phổ Thạnh, Quảng Ngãi năm 2015 - 2016
PHÒNG GD & ĐT THANH SƠN
TRƯỜNG THCS VĂN MIẾU
ĐỀ KIỂM TRA HỌC KÌ I
MÔN: HÓA - LỚP: 9
Thời gian: 45 phút
Năm học: 2014 - 2015
Phần I: Trắc nghiệm khách quan (3đ)
Câu 1 (3 đ): Hãy ghép các chữ A, B, C, D.... chỉ nội dung thí nghiệm với 1 chữ số1, 2, 3, 4.... chỉ hiện tượng xảy ra cho phù hợp (Ví dụ: nếu ghép ý A với 1 thì ghi vào bài là: A – 1).
| Thí nghiệm | Hiện tượng |
| A. Cho dây nhôm vào cốc đựng dung dịch NaOH đặc | 1. Không có hiện tượng gì xảy ra |
| B. Cho bột sắt vào dung dịch HCl | 2. Bọt khí xuất hiện nhiều, nhôm tan dần |
| C. Cho lá kẽm vào dung dịch CuCl2 | 3. Có khí không màu mùi hắc bay ra, dung dịch tạo thành có màu xanh |
| D. Cho dây Cu vào dung dịch FeSO4 | 4. Có chất rắn mầu đỏ tạo thành bám vào lá Zn, màu xanh của dung dịch nhạt dần, kim loại tan dần |
| E. Nhỏ dung dịch BaCl2 vào dung dịch Na2SO4 | 5. Có bọt khí thoát ra, sắt tan dần |
| F. Cho lá Cu vào H2SO4 đặc nóng | 6. Có kết tủa trắng xuất hiện |
Phần II: Tự luận (7đ)
Câu 2 (3đ): Hoàn thành các PTPƯ cho sơ đồ sau: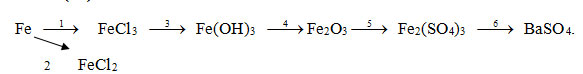
Câu 3 (4 đ): Hòa tan hoàn toàn 4,4 g hỗn hợp gồm Mg, MgO bằng dung dịch axit HCl 7,3% (vừa đủ). Sau phản ứng thu được 2,24 lít khí (ở đktc).
a, Viết PTHH.
b, Tính khối lượng mỗi chất trong hỗn hợp đầu.
c, Tính khối lượng dung dịch axit HCl 7,3% cần dùng để hòa tan hết hỗn hợp nói trên.
(Cho Mg = 24; Cl = 35,5; H = 1; O = 16)
Đáp án đề kiểm tra 45 phút học kì 1 môn Hóa học lớp 9
Câu 1:
A – 2; B – 5; C – 4; D – 1; E – 6; F - 3
Câu 2:
1. 2Fe + 3Cl2 → 2FeCl3
2. Fe + 2HCl -> FeCl2 + H2
3. 2FeCl3 + NaOH -> Fe(OH)3 + 3NaCl
4. 2Fe(OH)3→Fe2O3 +3 H2O
5. Fe2O3 + 3H2SO4 -> Fe2(SO4)3 + 3H2O
6. Fe2(SO4)3 + BaCl2 -> 3BaSO4 + 2FeCl3
Câu 3:
a, PTHH:
Mg + 2HCl -> MgCl2 + H2 (1)
MgO + 2HCl -> MgCl2 + H2O (2)
b, Khí sinh ra là khí H2.
nH2 = 2,24/22,4 = 0,1 mol
Theo PT (1): nMg = nH2 = 0,1 mol
> mMg = 0,1 x24 = 2,4 g
-> mMgO = 4,4 – 2,4 = 2 g
c, nMgO = 2/40 = 0,5 mol
Theo PT (1): nHCl = 2n H2 = 0,2 mol
Theo PT (2): nHCl = 2n MgO = 0,1 mol
-> Tổng khối lượng HCl cần dùng để hòa tan hoàn toàn hỗn hợp trên là:
mHCl = (0,2 + 0,1)x36,5 = 10,95 g
Vậy khối lượng dung dịch HCl 7,3% cần dùng là:
md2HCl = (mHCl x 100)/C% = (10,95 x 100)/ 7,3 = 150g
