Đề thi thử THPT Quốc gia năm 2020 môn Hóa học Sở GD&ĐT Hà Nội - Lần 2



Đề thi thử THPT Quốc gia năm 2020 môn Hóa học Sở GD&ĐT Hà Nội - Lần 2 được VnDoc tổng hợp, biên soạn có đáp án lời giải chi tiết ở các câu hỏi khó giúp các bạn luyện tập, cũng như đánh giá năng lực học tập. Đề thi được biên soạn giống với đề thi THPT Quốc gia các năm trước. Mời các bạn cùng tham khảo chi tiết và tải về tại đây
Đề thi thử THPT Quốc gia năm 2020 môn Hóa học Sở GD&ĐT Hà Nội - Lần 2 có đáp án
Đáp án đề thi thử THPT Quốc gia năm 2020 môn Hóa học Sở Giáo dục và Đào tạo Hà Nội - Lần 2
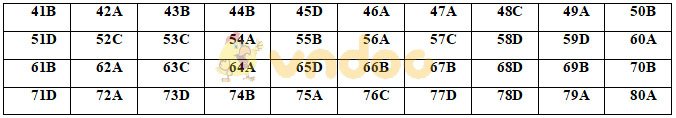
Hướng dẫn giải câu hỏi khó trong đề thi thử THPT Quốc gia năm 2020 môn Hóa học Sở Giáo dục và Đào tạo Hà Nội - Lần 2
Câu 44. Axit amino axetic (NH2-CH2-COOH) tác dụng được với dung dịch nào sau đây?
A. NaCl.
B. HCl.
C. Na2SO4.
D. NaNO3.
|
Hướng dẫn giải NH2-CH2-COOH + HCl → ClNH3-CH2-COOH |
Câu 53. Nhúng một đinh sắt sạch vào dung dịch Cu(NO3)2. Sau một thời gian lấy đinh sắt ra, làm khô, thấy khối lượng đinh sắt tăng 1 gam (giả sử toàn bộ lượng kim loại Cu sinh ra đều bám hết vào đinh sắt).
Khối lượng sắt đã phản ứng là
A. 3,5 gam.
B. 2,8 gam.
C. 7,0 gam.
D. 5,6 gam.
|
Hướng dẫn giải Áp dụng: Tăng giảm khối lượng: 1 mol Fe phản ứng làm khối lượng kim loại tăng 8 gam xmol 1 gam n Fe = 1/8 mol => m Fe = 7 gam |
Câu 54. Chất X tác dụng được với dung dịch HCl. Mặt khác khi cho chất X tác dụng với dung dịch Ca(OH)2 thì thu được kết tủa. Chất X là
A. Ca(HCO3)2.
B. BaCl2.
C. CaCO3.
D. AlCl3.
|
Hướng dẫn giải Ca(HCO3)2 + 2HCl → CaCl2 + 2CO2 + 2H2O Ca(HCO3)2 + Ca(OH)2 → 2CaCO3 + 2H2O |
Câu 56. Lên men dung dịch chứa 300 gam glucozơ thu được 92 gam ancol etylic. Hiệu suất quá trình lên men tạo thành ancol etylic là
A. 60%.
B. 54%.
C. 80%.
D. 40%.
|
Hướng dẫn giải n glucozo = 5/3 mol, n ancol etylic = 2 mol PTHH: C6H12O6 5/3 1 0/3 => H% = 2:10/3 = 60% |
Câu 57. Cho các loại tơ sau: tơ xenlulozơ axetat, tơ capron, tơ nitron, tơ visco, tơ nilon-6,6. Có bao nhiêu tơ thuộc loại tơ poliamit?
A. 1.
B. 4.
C. 2.
D. 3.
|
Hướng dẫn giải Tơ capron và tơ nilon-6,6 |
Câu 58. Thủy phân hoàn toàn 14,6 gam Gly-Ala trong dung dịch NaOH dư thu được m gam muối. Giá trị của m là
A. 21,0.
B. 11,1.
C. 18,7.
D. 20,8.
|
Hướng dẫn giải PTHH: Gly – Na + 2NaOH → GlyNa + AlaNa + H2O 0,1 → 0,1→ 0,1 => m muối = 0,1.(75 +22) + 0,1.(89 + 22)=20,8gam |
Câu 60. Cho dung dịch HCl lần lượt tác dụng với các chất sau: Fe3O4, Fe(NO3)2, FeSO4, FeCO3. Số trường hợp xảy ra phản ứng là
A. 3.
B. 2.
C. 4.
D. 1.
|
Hướng dẫn giải Fe3O4 + 8HCl → FeCl2 + 2FeCl3 + 4H2O 9Fe(NO3)2 + 12HCl →5Fe(NO3)3 + 4FeCl3 + 3NO + 6H2O FeCO3 + 2HCl → FeCl2 + H2O + CO2 |
Câu 67. Khi điều chế FeCl2 bằng cách cho Fe tác dụng với dung dịch HCl. Để bảo quản dung dịch FeCl2 thu được không bị chuyển thành hợp chất sắt(III), người ta có thể cho thêm vào dung dịch lượng dư chất nào sau đây?
A. kẽm.
B. sắt.
C. dung dịch HNO3.
D. dung dịch HCl
|
Hướng dẫn giải PTHH: Fe + 2Fe3+ → 3Fe2+ => Việc thêm Fe sẽ ngăn quá trình Fe2+ bị oxi hóa thành Fe3+ |
Câu 69. Để khử hoàn toàn 8,00 gam bột Fe2O3 bằng bột Al (ở nhiệt độ cao, trong điều kiện không có không khí) thì khối lượng bột nhôm cần dùng là
A. 5,40 gam.
B. 2,70 gam.
C. 1,35 gam.
D. 8,10 gam.
|
Hướng dẫn giải PTHH: Fe2O3 + 2Al → Al2O3 + 2Fe 0,05 →0,1 => m Al = 2,7 gam |
Câu 71. Cho các phát biểu sau:
(a) Tơ nilon-6,6 thuộc loại tơ tổng hợp.
(b) Có 4 chất trong các chất: phenol, etyl axetat, ancol etylic, axit axetic, lysin tác dụng được với dung dịch NaOH.
(c) Các este bị thủy phân trong môi trường kiềm đều tạo muối và ancol.
(d) Protein khi thủy phân hoàn toàn chỉ thu được hỗn hợp các α-amino axit.
(e) Dung dịch fructozơ có khả năng tham gia phản ứng tráng bạc.
Số phát biểu đúng là
A. 2.
B. 4.
C. 5.
D. 3.
|
Hướng dẫn giải (c) Sai vì thủy phân este trong môi trường kiềm có thể tạo muối và ancol/anđehit/xeton/H2O. (d) Sai vì protein đơn giản thủy phân ra α-amino axit còn protein phức tạp ngoài α-amino axit còn có thêm thành phần protein như chất béo, cacbonhiđrat, … |
Câu 72. Cho 26,8 gam hỗn hợp X gồm hai este đơn chức tác dụng vừa đủ với 350 ml dung dịch NaOH 1M. Sau khi phản ứng kết thúc, thu được ancol T và m gam hỗn hợp Y gồm hai muối. Đốt cháy hoàn toàn T thu được 6,72 lít khí CO2 (đktc) và 8,1 gam nước. Giá trị của m là
A. 32,1.
B. 33,9.
C. 23,9.
D. 20,5.
|
Hướng dẫn giải n CO2 = 0,3 mol; n H2O = 0,45 mol => n ancol = 0,45 - 0,3 = 0,15 mol => C ancol = 0,3/015 = 2 => C2H5OH Vì este đơn chức mà n NaOH = 0,35 > n ancol => X chứa este của phenol => n H2O = (0,35 - 0,15):2 = 0,1 mol Áp dụng BTKL ta có: 26,8 + 0,35.40 = m + 0,15.46 + 0,1.18 => m = 32,1 gam |
Câu 73. Đốt cháy hoàn toàn 17,64 gam một triglixerit X bằng oxi dư thu được 25,536 lít khí CO2 (đktc) và 18,36 gam H2O. Mặt khác, thủy phân hoàn toàn 0,015 mol X bằng dung dịch NaOH vừa đủ thu được 4,59 gam natri stearat và m gam muối của một axit béo Y. Giá trị của m là
A. 8,34.
B. 6,04.
C. 7,65.
D. 9,06.
|
Hướng dẫn giải n CO2 = 1,14 mol; n H2O =1,02 mol , BTKL => m O2 = 44.1,14 + 18,36 - 17,64 = 50,88gam => nO2= 1,59 mol BTNT (O) => nX = (2.1,14+1,02-2.1,59):6=0,02 mol => M X = 17,64 : 0,02 = 882 Xét với 0,015 mol X => nNaOH = 0,045 mol, n C3H5(OH)3 = 0,015 mol BTKL => m = 882.0,015 + 40.0,045 - 0,015.92- 4,59 = 9,06 gam |
Câu 74. Nung 20,8 gam hỗn hợp gồm Cu, Mg và Al trong oxi một thời gian thu được 21,52 gam chất rắn X. Hòa tan X trong V ml dung dịch HCl 0,5M vừa đủ thu được dung dịch Y và 0,672 lít khí H2 (ở đktc).
Giá trị của V là
A. 400.
B. 300.
C. 200.
D. 150.
|
Hướng dẫn giải BTKL => mO2 = 21,52 - 20,8 = 0,72 gam => nO2 = 0,0225 mol => n HCl = 4nO2 + 2nH2 = 4.0,0225 + 2.0,03 = 0,15 => VHCl = 0,31 = 300ml |
Câu 76. Tiến hành thí nghiệm xà phòng hoá theo các bước sau:
Bước 1: Cho vào bát sứ khoảng 1 gam mỡ động vật và 2 – 2,5 ml dung dịch NaOH nồng độ 40%.
Bước 2: Đun sôi nhẹ hỗn hợp khoảng 30 phút và khuấy liên tục bằng đũa thuỷ tinh, thỉnh thoảng thêm vài giọt nước cất để giữ cho thể tích của hỗn hợp không đổi.
Bước 3: Rót thêm vào hỗn hợp 4 – 5 ml dung dịch NaCl bão hoà nóng, khuấy nhẹ rồi để nguội.
Có các phát biểu sau:
(a) Sau bước 1, thu được chất lỏng đồng nhất.
(b) Sau bước 3, thấy có lớp chất rắn màu trắng nổi lên.
(c) Mục đích chính của việc thêm dung dịch NaCl ở bước 3 là làm tăng tốc độ của phản ứng xà phòng
hoá.
(d) Sản phẩm thu được sau bước 3 đem tách hết chất rắn không tan, chất lỏng còn lại hòa tan được Cu(OH)2 tạo thành dung dịch màu xanh lam.
(e) Có thể thay thế mỡ động vật bằng dầu thực vật.
Số phát biểu đúng là
A. 2.
B. 5.
C. 3.
D. 4.
|
Hướng dẫn giải (a) Sai vì phản ứng chưa xảy ra, chất lỏng phân lớp. (c) Sai vì mục đích chính của việc thêm NaCl là để tách muối natri của axit béo (xà phòng). |
Câu 77. Tiến hành các thí nghiệm sau:
(a) Sục 0,15 mol khí CO2 vào 100 ml dung dịch NaOH 2M.
(b) Sục khí Cl2 dư vào dung dịch FeSO4.
(c) Cho hỗn hợp NaHSO4 và NaHCO3 (tỉ lệ mol 1:1) vào nước.
(d) Cho hỗn hợp Cu và Fe2O3 (tỉ lệ mol 1:1) vào dung dịch HCl dư.
(e) Cho FeO vào dung dịch KHSO4 dư.
Sau khi các phản ứng kết thúc, số thí nghiệm thu được hai muối là
A. 2.
B. 4.
C. 5.
D. 3.
|
Hướng dẫn giải (a) 1 < T= 02/015 = 1,33< 2 => tạo 2 muối (b) 6FeSO4 + 3Cl2 → 2Fe2(SO4)3 + 2FeCl3 (c) NaHSO4 + NaHCO3 → Na2SO4 + CO2↑ + H2O (d) Fe2O3 + 6HCl → 2FeCl3 + 3H2O; Cu + 2FeCl3 → CuCl2 + 2FeCl2 (e) FeO + 2KHSO4 dư → FeSO4 + K2SO4 + H2O (KHSO4 dư) |
Để tham khảo đầy đủ chi tiết nội dung tài liệu, vui lòng ấn tải link bên dưới
Đề thi thử THPT Quốc gia năm 2020 môn Hóa học Sở GD&ĐT Hà Nội - Lần 2 vừa được VnDoc.com sưu tập kèm đáp án hướng dẫn giải và xin gửi tới bạn đọc cùng tham khảo. Đề thi gồm có 40 câu trắc nghiệm nằm trong bài thi khoa học tự nhiên, thí sinh làm đề trong thời gian 50 phút.
Trên đây VnDoc.com vừa giới thiệu tới các bạn Đề thi thử THPT Quốc gia năm 2020 môn Hóa học Sở GD&ĐT Hà Nội - Lần 2. Mong rằng qua đây các bạn có thể học tập tốt hơn môn Hóa học lớp 12 nhé. Mời các bạn cùng tham khảo thêm các môn Toán 12, Ngữ văn 12, Tiếng Anh 12, đề thi học kì 1 lớp 12, đề thi học kì 2 lớp 12...
Ngoài ra, VnDoc.com đã thành lập group chia sẻ tài liệu ôn tập THPT Quốc gia miễn phí trên Facebook: Quyết tâm đỗ Đại Học Mời các bạn học sinh tham gia nhóm, để có thể nhận được những tài liệu, đề thi mới nhất.