Đề cương ôn tập hóa 9 học kì 1 năm học 2023 - 2024
Ôn tập học kì 1 hoá 9 năm học 2022
Đề cương ôn tập hóa 9 học kì 1 năm học 2023 - 2024 được VnDoc biên soạn giúp các bạn có thêm tài liệu ôn tập hóa 9 học kì 1. Nội dung tài liệu gồm 3 phần. Phần 1 tóm tắt lý thuyết trọng tâm hóa 9 kì 1, phần 2, phần 3 lần lượt các dạng bài tập dưới câu hỏi trắc nghiệm khách quan và tự luận. Sau đây mời các bạn tham khảo chi tiết.
A. Tóm tắt nội dung kiến thức trọng tâm
Chương I: Các loại hợp chất vô cơ
1. Tính chất hóa học của oxit
| Oxit axit | Oxit bazơ | |
| Tác dụng với nước |
Một số oxit axit + H2O → dung dịch axit (đổi màu quỳ tím → đỏ) CO2 + H2O → H2CO3 Oxit axit tác dụng được với nước: SO2, SO3, N2O5, P2O5… Không tác dụng với nước: SiO2,… |
Một số oxit bazơ + H2O → dung dịch kiềm (đổi màu quỳ tím → xanh) CaO + H2O → Ca(OH)2 Oxit bazơ tác dụng được với nước: Na2O, K2O, BaO,.. Không tác dụng với nước: FeO, CuO, Fe2O3,… |
| Tác dụng với axit | Không phản ứng |
Axit + Oxit bazơ → muối + H2O FeO + H2SO4 (loãng) → FeSO4 + H2O |
| Tác dụng với bazơ kiềm |
Bazơ + Oxit axit → muối (muối trung hòa, hoặc axit) + H2O CO2 + 2NaOH → Na2CO3 + H2O CO2 + NaOH → NaHCO3 |
Không phản ứng |
| Tác dụng với oxit axit | Không phản ứng |
Oxit axit + Oxit bazơ (tan) → muối CaO + CO2 → CaCO3 |
| Tác dụng với oxit bazơ |
Oxit axit + Oxit bazơ (tan) → muối MgO + SO3 → MgSO4 |
Không phản ứng |
| Oxit lưỡng tính (ZnO, Al2O3, Cr2O3) | Oxit trung tính (oxit không tạo muối) NO, CO,… | |
| Tác dụng với nước | Không phản ứng | Không phản ứng |
| Tác dụng với axit | Al2O3 + 6HCl → 2AlCl3 + 3H2O | Không phản ứng |
| Tác dụng với bazơ | Al2O3 + 2NaOH → 2NaAlO2 + 3H2O | Không phản ứng |
| Phản ứng oxi hóa khử | Không phản ứng |
Tham gia phản ứng oxi hóa khử 2NO + O2 |
2. Tính chất hóa học của axit, bazơ
| Axit | Bazơ | |
| Chất chỉ thị | Đổi màu quỳ tím → đỏ |
đổi màu quỳ tím → xanh Đổi màu dung dịch phenolphatalein từ không màu thành màu hồng |
| Tác dụng với kim loại |
- Axit (HCl và H2SO4 loãng) + kim loại (đứng trước H trong dãy hoạt động hóa học) → muối + H2 Fe + 2HCl → FeCl2 + H2 |
Một số nguyên tố lưỡng tính như Zn, Al, Cr, … 2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2 |
| Tác dụng với bazơ |
Bazơ + axit → muối + nước NaOH + HCl → NaCl + H2O |
Một số bazơ lưỡng tính (Zn(OH)2, Al(OH)3, …) + dung dịch kiềm Al(OH)3 + NaOH → NaAlO2 + 2H2O |
| Tác dụng với axit |
Bazơ + axit → muối + nước H2SO4 + NaOH → Na2SO4 + H2O
|
|
| Tác dụng với oxit axit | Không phản ứng |
Bazơ + oxit axit → muối axit hoặc muối trung hòa + nước SO2 + NaOH → Na2SO3 + H2O SO2 + NaOH → Na2HSO3 + H2O |
| Tác dụng với oxit bazơ |
Axit +oxit bazơ → muối + nước CaO + H2SO4 → CaSO4 + H2O |
Một số oxit lưỡng tính như ZnO, Al2O3, Cr2O3,… tác dụng với dung dịch bazơ |
| Tác dụng với muối |
Axit + muối → muối mới + axit mới HCl + AgNO3 → AgCl + HNO3 |
Bazơ + muối → Bazơ mới + muối mới KOH + CuSO4 → K2SO4 + Cu(OH)2 |
| Phản ứng nhiệt phân |
Một số axit H2SO4 |
Bazơ không tan Cu(OH)2 |
3. Tính chất hóa học của muối
| Tính chất hóa học | Muối |
| Tác dụng với kim loại |
Kim loại + muối → muối mới + kim loại mới Cu + 2AgNO3 → Cu(NO3)2 + 2Ag Điều kiện: Kim loại đứng trước (trừ Na, K, Ca,…) đẩy kim loại đứng sau (trong dãy hoạt động hóa học) ra khỏi dung dịch muối của chúng. Kim loại Na, K, Ca… khi tác dụng với dung dịch muối thì không cho kim loại mới vì: Na + CuSO4 → 2Na + H2O → NaOH + H2 CuSO4 + 2NaOH → Cu(OH)2 ↓+ Na2SO4 |
| Tác dụng với bazơ |
Muối + bazơ → muối mới + bazơ mới FeCl3 + 3NaOH → Fe(OH)3 + 3NaCl |
| Tác dụng với axit |
Muối + axit → muối mới + axit mới BaCl2 + AgNO3 → Ba(NO3)2 + AgCl |
| Tác dụng với muối |
Muối + muối → 2 muối mới BaCl2 + Na2SO4 → BaSO4 + NaCl |
| Nhiệt phân muối |
Một số muối bị nhiệt phân hủy ở nhiệt độ cao CaCO3 2KMnO4 |
CHƯƠNG 2: Kim loại
1. Tính chất của Al và Fe
| Nhôm (Al) | Sắt (Fe) | |
| Tính chất vật lý |
- Là kim loại nhẹ, màu trắng, dẻo, có ánh kim, dẫn điện và dẫn nhiệt tốt. - Nhiệt độ nóng chảy 6600C. |
- Là kim loại nặng, màu trắng xám, dẻo, có ánh kim, dẫn điện, dẫn nhiệt tốt (kém Al). - Nhiệt độ nóng chảy 15390C. - Có tính nhiễm từ. |
| Tính chất hóa học | < Al và Fe có tính chất hóa học của kim loại > | |
| Tác dụng với phi kim |
2Al + 3Cl2 4Al + 3O2 |
2Fe + 3Cl2 2Fe + 3Cl2 |
| Tác dụng với axit | 2Al + 6HCl → 2AlCl3 + 3H2 | Fe + H2SO4 → FeSO4 + H2 |
| Lưu ý: Al và Fe không phản ứng với HNO3 đặc nguội và H2SO4 đặc nguội. | ||
| Tác dụng với dd muối | 2Al + 3CuSO4 → Al2(SO4)3 + 3Cu | Fe + 2AgNO3 ↓ →Fe(NO3)2 + 2Ag |
|
Tính chất khác Tác dụng với dd kiềm |
nhôm + dd kiềm→ H2 2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2 |
<Không phản ứng> |
| Trong các phản ứng: Al luôn có hóa trị III. | Trong các phản ứng: Fe có hai hóa trị: II, III. | |
| Hợp chất |
Al2O3 có tính lưỡng tính Al2O3 + 6HCl → 2AlCl3 + 3H2O Al2O3 + 2NaOH → 2NaAlO2 + H2O |
FeO, Fe2O3 và Fe3O4 là oxit bazo không tan trong nước. Fe(OH)2 ↓màu trắng Fe(OH)3 ↓màu đỏ nâu |
2. Hợp chất sắt: Gang, thép
| Hợp kim | Gang | Thép |
| Sắt với cacbon (2 – 5%) và một số nguyên tố khác như Si, Mn S. . | Sắt với cacbon (dưới 2%) và các nguyên tố khác như Si, Mn, S . | |
| Tính chất | Giòn (không rèn, không dát mỏng được) và cứng hơn sắt,. | Đàn hồi, dẻo (rèn, dát mỏng, kéo sợi được), cứng. |
| Sản xuất |
Trong lò cao - Nguyên liệu: quặng sắt - Nguyên tắc: CO khử các oxit sắt ở t0 cao. - Các phản ứng chính: Phản ứng tạo thành khí CO: C + O2 C + CO2 CO khử oxit sắt có trong quặng: Fe2O3 + 3CO Fe nóng chảy hoà tan 1 lượng nhỏ |
- Trong lò luyện thép. - Nguyên liệu: gang, khí oxitắc: Oxi hóa các nguyên tố C, Mn, Si, S, P, … có trong gang. - Các phản ứng chính Thổi khí oxi vào lò có gang nóng chảy ở nhiệt độ cao. Khí oxi oxi hoá các nguyên tố kim loại, phi kim để loại khỏi gang phần lớn các nguyên tố C, Si, Mn, S . . . Thí dụ: C + O2 Thu được sản phẩm là thép. |
3. Dãy hoạt động hóa học của kim loại
Theo chiều giảm dần độ hoạt động của kim loại:
Li, K, Ba, Ca, Na, Mg, Al, Zn, Fe, Ni, Sn, Pb, (H), Cu, Ag, Hg, Pt, Au
Lúc khó bà cần nàng may áo giáp sắt nên sang phố hàng đồng á hiệu phi âu.
Ý nghĩa dãy hoạt động hóa học của kim loại:
- Mức độ họat động hóa học của kim loại giảm dần từ trái qua phải.
- Kim loại đứng trước Mg (5 kim loại đầu tiên) tác dụng với nước ở điều kiện thường à kiềm và khí hiđro.
- Kim loại đứng trước H phản ứng với một số dd axit (HCl, H2SO4 loãng, …) à khí H2.
- Kim loại đứng trước đẩy kim loại đứng sau ra khỏi dung dịch muối (trừ 5 kim loại đầu tiên).
CHƯƠNG 3. Phi kim
1. Tính chất của clo và cacbon
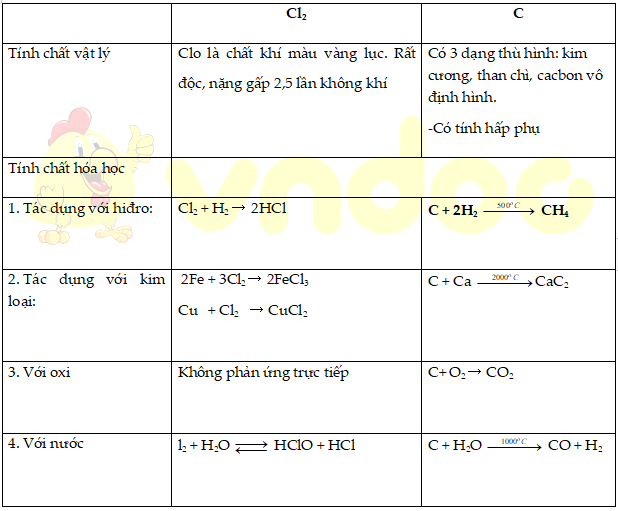
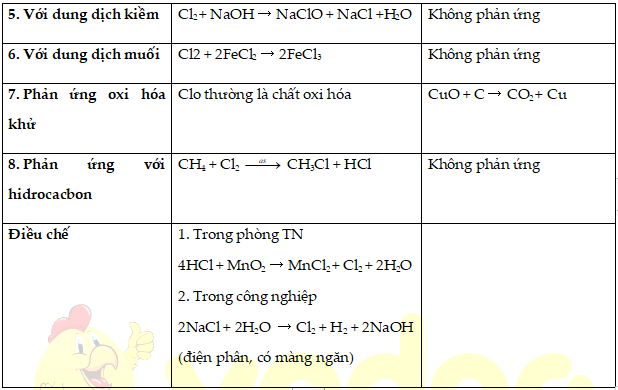
2. Tính chất của hợp chất cacbon
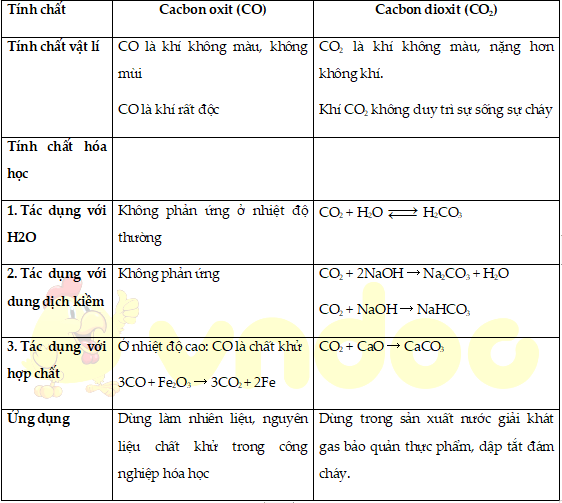
B. Bài tập vận dụng
1. Câu hỏi trắc nghiệm khách quan
Câu 1. Dung dịch H2SO4 tác dụng với dãy chất là:
A. Fe, CaO, HCl.
B. Cu, BaO, NaOH.
C. Mg, CuO, HCl.
D. Zn, BaO, NaOH.
Câu 2. Để phân biệt 2 dung dịch HCl và H2SO4. Người ta dùng thuốc thử là:
A. Quỳ tím.
B. Zn.
C. dd NaOH.
D. dd BaCl2.
Câu 3. Chất gây ô nhiễm và mưa acid là
A. Khí O2.
B.Khí SO2.
C. Khí N2.
D. Khí H2.
Câu 4. Cặp chất tạo ra chất kết tủa trắng là
A. CuO và H2SO4.
B. ZnO và HCl.
C. NaOH và HNO3.
D. BaCl2 và H2SO4
Câu 5. Các khí ẩm được làm khô bằng CaO là:
A. H2; O2; N2.
B. H2; CO2; N2.
C. H2; O2; SO2.
D. CO2; SO2; HCl.
Câu 6. Dãy chất tác dụng được với nước:
A. CuO; CaO; Na2O; CO2
B. BaO; K2O; SO2; CO2.
C. MgO; Na2O; SO2; CO2.
D. NO; P2O5; K2O; CaO
Câu 7. Chất phản ứng đượcvới dung dịch acid Clohiđric sinh ra chất khí nhẹ hơn không khí, cháy trong không khí với nhọn lửa màu xanh nhạt:
A. BaCO3
B. Zn
C.FeCl3
D. Ag
Câu 8. Oxit axit là:
A. Hợp chất với tất cả kim loại và oxi.
B. Những oxit tác dụng được với axit tạo thành muối và nước .
C. Hợp chất của tất cả các phi kim và oxi .
D. Những oxit tác dụng được với dung dịch bazơ tạo muối và nước.
Câu 9. Chất tác dụng được với HCl và CO2:
A. Sắt
B. Nhôm
C. Kẽm
D. Dung dịch NaOH.
Câu 10. Phương pháp được dùng để điều chế canxi oxit trong công nghiệp.
A. Nung đá vôi ở nhiệt độ cao là trong công nghiệp hoặc lò thủ công .
B. Nung CaSO4 trong lò công nghiệp .
C. Nung đá vôi trên ngọn lửa đèn cồn.
D. Cho canxi tác dụng trực tiếp với oxi.
Câu 11. Phương pháp được dùng để sản xuất khí sunfurơ trong công nghiệp.
A. Phân hủy canxi sunfat ở nhiệt độ cao .
B. Đốt cháy lưu huỳnh trong oxi .
C. Cho đồng tác dụng với axit sunfuric đặc, nóng.
D. Cho muối natrisunfit tác dụng với axit clohiđric.
Câu 12. Chất khi tan trong nước cho dung dịch, làm quỳ tím hóa đỏ :
A. KOH
B. KNO3
C. SO3
D. CaO
Câu 13. Chất tác dụng với axit sunfuric loãng tạo thành muối và nước:
A. Cu
B. CuO
C. CuSO4
D. CO2
Câu 14. Dùng Canxi oxit để làm khô khí:
A. Khí CO2
B. Khí SO2
C. Khí HCl
D. CO
Câu 15. Một hỗn hợp rắn gồm Fe2O3 và CaO, để hòa tan hoàn toàn hỗn hợp này người ta phải dùng dư:
A. Nước.
B. Dung dịch NaOH.
C. Dung dịch HCl.
D. dung dịch NaCl.
Câu 16. Dung dịch axit mạnh không có tính chất là:.
A. Tác dụng với oxit axit tạo thành muối và nước.
B. Tác dụng với bazơ tạo thành muối và nước.
C. Tác dụng với nhiều kim loại giải phóng khí hiđrô.
D. Làm đổi màu quỳ tím thành đỏ.
2. Bài tập tự luận
Câu 1. Có các oxit sau: CaO, Al2O3, Fe2O3, P2O5, CuO, SO3, CO2. Oxit nào có thể tác dụng được với:
a) Nước
b) Axit clohidric
c) Natri hidroxit
Câu 2. Tìm các chất kí hiệu bằng chữ cái trong sơ đồ sau và hoàn thành sơ đồ bằng phương trình phản ứng:
a) FeS2 → M → N → D → CuSO4
b) CuSO4 → B → C → D → Cu
Câu 3. Viết các phương trình phản ứng theo sơ đồ chuyển hóa sau:
a) Ca → CaO → Ca(OH)2 → CaCl2 → CaCO3
b) CaCO3 → CO2 → NaHCO3 → Na2CO3 → Na2SO4
c) Al → AlCl3 → Al(NO3)3 → Al(OH)3 → Al2O3 → Al
Câu 4. Có những chất sau: SO3, CO2, Na2O, BaO, NO, KOH, H2SO4, Fe2O3. Hãy viết phương trình những cặp chất có thể phản ứng được với nhau
Câu 5. Cho 2,24 lít khí CO2 (đktc) tác dụng với vừa đủ với 100 ml dung dịch KOH tạo thành muối K2CO3. Coi thể tích dung dịch thay đổi không đáng kể. Tính nồng độ mol của dung dịch KOH và K2CO3.
Câu 6. Dùng phương pháp nào để phân biệt các khí sau: CO, SO2, CO2.
Bằng phương pháp hóa học nào có thể nhận biết được từng chất trong mỗi dãy chất sau: CuO, MnO2, Ag2O và FeO
Câu 7. Cho 5 dung dịch riêng biệt: K2SO4, AgNO3, NaOH, Ba(OH)2, HCl. Chỉ dùng giấy quỳ tím, trình bày các bước nhận biết 5 dung dịch trên. Viết phương trình phản ứng xảy ra.
Câu 8. Nung nóng 26,2 gam hỗn hợp kim loại gồm: Mg, Al, Zn trong không khí đến khí đến khi phản ứng xảy ra hoàn toàn thu được 40,6 gam hỗn hợp 3 oxit. Để hòa tan hết lượng oxit trên cần V lít dung dịch HCl 0,5M.
a) Tính giá trị của V
b) Tính khối lượng muối clorua tạo thành sau phản ứng.
Câu 9. Từ 40 tấn quặng pirit (FeS2) chứa 40% lưu huỳnh, sản xuất được 46 tấn axit sunfuric. Hiệu suất của quá trình sản xuất H2SO4 là bao nhiêu?
Câu 10. Cho 200 g dung dịch Na2CO3 tác dụng vừa đủ với 120 gam dung dịch HCl. Sau phản ứng dung dịch sau cùng có nồng độ 20%. Tính nồng độ phần trăm của hai dung dịch chất ban đầu.
........................
Mời các bạn tham khảo thêm một số tài liệu liên quan:
Bộ đề thi học kì 1 Hóa 9
- Đề thi học kì 1 hóa 9 Đề 1
- Đề thi học kì 1 hóa 9 Đề 2
- Đề thi học kì 1 hóa 9 Đề 3
- Bộ đề thi học kì 1 hóa 9 Có đáp án
- 30 Đề thi học kì 1 môn Hóa học lớp 9 Hay Chọn Lọc
Để có thể đạt điểm cao trong kì thi học kì 1 lớp 9 sắp tới, các em học sinh cần lên kế hoạch ôn tập phù hợp, bên cạnh đó cần thực hành luyện đề để làm quen với nhiều dạng đề khác nhau cũng như nắm được cấu trúc đề thi. Chuyên mục Đề thi học kì 1 lớp 9 trên VnDoc sẽ là tài liệu phong phú và hữu ích cho các em ôn tập và luyện đề. Đây cũng là tài liệu hay cho thầy cô tham khảo ra đề. Mời thầy cô và các em tham khảo.
