Giải SBT Hóa học 10 Chân trời sáng tạo bài 2
Giải SBT Hóa học 10 bài 2: Thành phần của nguyên tử được VnDoc biên soạn hướng dẫn bạn đọc trả lời các nội dung câu hỏi bài tập môn Hóa học 10 Chân trời sáng tạo.
Bài: Thành phần của nguyên tử
Bài 2.1 trang 7 SBT Hóa học 10: Phát biểu nào dưới đây không đúng?
A. Nguyên tử được cấu thành từ các hạt cơ bản là proton, neutron và electron.
B. Hầu hết hạt nhân nguyên tử được cấu thành từ các hạt proton và neutron.
C. Vỏ nguyên tử được cấu thành bởi các hạt electron
D. Nguyên tử có cấu trúc đặc khít, gồm vỏ nguyên tử và hạt nhân nguyên tử.
Lời giải:
Đáp án đúng là: D
Phát biểu D không đúng do nguyên tử có cấu trúc rỗng.
Bài 2.2 trang 7 SBT Hóa học 10: Cho 1 mol kim loại X. Phát biểu nào dưới đây đúng?
A. 1 mol X chứa số lượng nguyên tử bằng số lượng nguyên tử trong 1 mol nguyên tử hydrogen.
B. 1 mol X chứa số lượng nguyên tử bằng số lượng nguyên tử trong ![]() \(\frac{1}{12}\) mol carbon.
\(\frac{1}{12}\) mol carbon.
C. 1 mol X có khối lượng bằng khối lượng 1 mol hydrogen.
D. 1 mol X có khối lượng bằng ![]() \(\frac{1}{12}\) khối lượng 1 mol carbon.
\(\frac{1}{12}\) khối lượng 1 mol carbon.
Lời giải:
Đáp án đúng là: A
1 mol X chứa số lượng nguyên tử bằng số lượng nguyên tử trong 1 mol nguyên tử hydrogen.
Bài 2.3 trang 7 SBT Hóa học 10: Thành phần nào không bị lệch hướng trong trường điện?
A. Tia α.
B. Proton
C. Nguyên tử hydrogen
D. Tia âm cực
Lời giải:
Đáp án đúng là: C
Nguyên tử hydrogen trung hòa về điện nên không bị lệch hướng trong trường điện.
Bài 2.4 trang 7 SBT Hóa học 10: Phát biểu nào sai khi nói về neutron?
A. Tồn tại trong hạt nhân nguyên tử.
B. Có khối lượng bằng khối lượng proton.
C. Có khối lượng lớn hơn khối lượng electron.
D. Không mang điện.
Lời giải:
Đáp án đúng là: B
Phát biểu B sai vì: Khối lượng neutron xấp xỉ bằng khối lượng proton.
Bài 2.5 trang 7 SBT Hóa học 10: Nguyên tử R có điện tích lớp vỏ nguyên tử là 41,6.10-19C. Điều khẳng định nào sau đây là không chính xác?
A. Lớp vỏ nguyên tử R có 26 electron.
B. Hạt nhân nguyên tử R có 26 proton.
C. Hạt nhân nguyên tử R có 26 neutron.
D. Nguyên tử R trung hòa về điện.
Lời giải:
Đáp án đúng là: C
Biết điện tích lớp vỏ nguyên tử chỉ xác định được số proton và số electron chưa thể xác định được số neutron.
Giải SBT Hoá học 10 trang 8
Bài 2.6 trang 8 SBT Hóa học 10: Hạt nhân của nguyên tử nguyên tố A có 24 hạt, trong đó số hạt không mang điện là 12. Số electron trong A là
A. 12
B. 24
C. 13
D. 6
Lời giải:
Đáp án đúng là: A
Xét nguyên tử nguyên tố A:
+ Hạt nhân của nguyên tử có 24 hạt ⇒ số proton + số neutron = 24.
+ Số hạt không mang điện là 12 ⇒ số neutron là 12.
Vậy nguyên tử A có số electron = số proton = 24 – 12 = 12.
Bài 2.7 trang 8 SBT Hóa học 10: Trong nguyên tử Al, số hạt mang điện tích dương là 13, số hạt không mang điện là 14. Số hạt electron trong Al là bao nhiêu?
A. 13
B. 15
C. 27
D. 14
Lời giải:
Đáp án đúng là: A
Trong nguyên tử Al, số hạt electron = số hạt mang điện tích dương = 13.
Bài 2.8 trang 8 SBT Hóa học 10: Đặc điểm của electron là
A. mang điện tích dương và có khối lượng.
B. mang điện tích âm và có khối lượng.
C. không mang điện và có khối lượng.
D. mang điện tích âm và không có khối lượng.
Lời giải:
Đáp án đúng là: B
Hạt electron mang điện tích âm và có khối lượng.
Bài 2.9 trang 8 SBT Hóa học 10: Nhận định nào sau đây không đúng?
A. Tất cả các hạt nhân nguyên tử đều chứa proton và neutron.
B. Nguyên tử có kích thước vô cùng nhỏ và trung hòa về điện.
C. Lớp vỏ nguyên tử chứa electron mang điện tích âm.
D. Khối lượng nguyên tử hầu hết tập trung ở hạt nhân.
Lời giải:
Đáp án đúng là: A
A không đúng, vì có một loại nguyên tử hydrogen không chứa neutron trong hạt nhân.
Bài 2.10 trang 8 SBT Hóa học 10: Cho các phát biểu sau:
(1) Tất cả các hạt nhân nguyên tử đều được cấu tạo từ các hạt proton và neutron.
(2) Khối lượng nguyên tử tập trung phần lớn ở lớp vỏ.
(3) Trong nguyên tử, số electron bằng số proton.
(4) Trong hạt nhân nguyên tử, hạt mang điện là proton và electron.
(5) Trong nguyên tử, hạt electron có khối lượng không đáng kể so với các hạt còn lại.
Số phát biểu đúng là:
A. 1.
B. 2.
C. 3.
D. 4.
Lời giải:
Đáp án đúng là: B
Phát biểu (3) và (5) đúng.
(1) sai vì có một loại nguyên tử hydrogen không có neutron.
(2) sai vì khối lượng nguyên tử tập trung ở hạt nhân nguyên tử.
(4) sai vì hạt nhân nguyên tử không chứa electron.
Bài 2.11 trang 8 SBT Hóa học 10: Kết quả nào trong thí nghiệm bắn phá lá vàng của Rutherford chỉ ra sự tồn tại của hạt nhân nguyên tử?
Lời giải:
Kết quả trong thí nghiệm bắn phá lá vàng của Rutherford chỉ ra sự tồn tại của hạt nhân nguyên tử:
Đa số hạt α bay xuyên thẳng qua lá vàng mỏng với hướng di chuyển không đổi. Một số hạt α bị lệch hướng, chứng tỏ có va chạm trước khi bay ra khỏi lá vàng, một số hạt α bị lệch hướng do chịu tác động của một lượng lớn điện tích dương tập trung trong không gian rất nhỏ của nguyên tử vàng. Các electron của nguyên tử quay quanh lõi trung tâm, giống như các hành tinh quay quanh Mặt Trời. Phần lõi này được gọi là hạt nhân nguyên tử.
Bài 2.12 trang 8 SBT Hóa học 10: Hãy điền những dữ liệu còn thiếu vào các chỗ trống trong các câu sau:
a) Trong ống tia âm cực, tia âm cực được phát ra từ điện cực âm được gọi là (1) ….
b) Đơn vị nhỏ nhất của một nguyên tố có thể tồn tại đơn lẻ hoặc tồn tại trong các phân tử được gọi là (2) …..
c) Hạt mang điện tích dương được tìm thấy trong hạt nhân nguyên tử được gọi là (3) ….
d) Hạt không mang điện tồn tại trong hạt nhân nguyên tử được gọi là (4) ….
e) Hạt trong nguyên tử có khối lượng nhỏ nhất và khối lượng lớn nhất, tương ứng là (5) …. và (6) …..
Lời giải:
a) Trong ống tia âm cực, tia âm cực được phát ra từ điện cực âm được gọi là (1) cathode.
b) Đơn vị nhỏ nhất của một nguyên tố có thể tồn tại đơn lẻ hoặc tồn tại trong các phân tử được gọi là (2) nguyên tử.
c) Hạt mang điện tích dương được tìm thấy trong hạt nhân nguyên tử được gọi là (3) proton.
d) Hạt không mang điện tồn tại trong hạt nhân nguyên tử được gọi là (4) neutron.
e) Hạt trong nguyên tử có khối lượng nhỏ nhất và khối lượng lớn nhất, tương ứng là (5) electron và (6) neutron.
Giải SBT Hoá học 10 trang 9
Bài 2.13 trang 9 SBT Hóa học 10: Tia âm cực phát ra trong ống âm cực bị lệch hướng khi đặt trong trường từ. Một dây dẫn mang điện cũng có thể bị hút bởi trường từ. Tia âm cực bị lệch hướng khi đặt gần một vật mang điện âm. Tính chất nào của tia âm cực được thể hiện qua các hiện tượng này?
Lời giải:
Thông qua các hiện tượng rút ra tính chất: Tia âm cực là dòng electron mang điện tích âm.
Bài 2.14 trang 9 SBT Hóa học 10: Electron sinh ra trong ống tia âm cực chứa khí neon có khác electron sinh ra trong ống tia âm cực chứa khí chlorine không? Vì sao?
Lời giải:
Electron sinh ra trong ống tia âm cực chứa khí neon giống electron sinh ra trong ống tia âm cực chứa khí chlorine. Vì các electron không khác nhau về bản chất trong các môi trường khác nhau.
Bài 2.15 trang 9 SBT Hóa học 10: Nguyên tử mang điện tích dương, điện tích âm hay trung hòa? Giải thích vì sao một nguyên tử có thể tồn tại ở trạng thái này.
Lời giải:
Nguyên tử trung hòa về điện vì trong nguyên tử, số proton bằng số electron (hay số đơn vị điện tích dương bằng số đơn vị điện tích âm).
Bài 2.16 trang 9 SBT Hóa học 10: X là nguyên tố hóa học có trong thành phần của chất có tác dụng oxi hóa và sát khuẩn cực mạnh, thường được sử dụng với mục đích khử trùng và tẩy trắng trong lĩnh vực thủy sản, diệt nhuộm, xử lí nước cấp, nước thải, nước bể bơi. Nguyên tử X có tổng số các loại hạt bằng 52, trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 16 hạt. Xác định thành phần cấu tạo của nguyên tử X.
Lời giải:
Gọi p, n và e lần lượt là số proton, neutron và electron của X. Trong đó p = e.
Theo bài ra, ta có hệ phương trình:
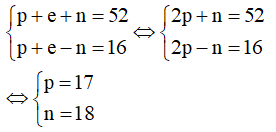
Vậy trong X có 17 proton; 17 electron và 18 neutron.
Bài 2.17 trang 9 SBT Hóa học 10: Các hợp chất của nguyên tố Y được sử dụng như là vật liệu chịu lửa trong các lò sản xuất sắt, thép, kim loại màu, thủy tinh và xi măng. Oxide của Y và các hợp chất khác cũng được sử dụng trong nông nghiệp, công nghiệp hóa chất và xây dựng. Nguyên tử Y có tổng số các hạt là 36. Số hạt không mang điện bằng một nửa hiệu số giữa tổng số hạt với số hạt mang điện tích âm. Xác định thành phần cấu tạo của nguyên tử Y.
Lời giải:
Gọi p, n và e lần lượt là số proton, neutron và electron của Y. Trong đó p = e.
Theo bài ra ta có hệ phương trình:
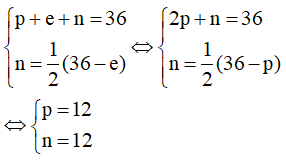
Vậy trong Y có 12 proton; 12 electron và 12 neutron.
Bài 2.18 trang 9 SBT Hóa học 10: Nitrogen giúp bảo quản tinh trùng, phôi, máu và tế bào gốc. Biết nguyên tử nitrogen có tổng số hạt là 21. Số hạt không mang điện chiếm 33,33%. Xác định số đơn vị điện tích hạt nhân của nitrogen.
Lời giải:
Gọi p, n và e lần lượt là số proton, neutron và electron của nitrogen. Trong đó p = e.
Số hạt không mang điện chiếm 33,33%
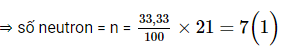
Lại có: p + e + n = 21 ⇒ 2p + n = 21 (2)
Thế n = 7 vào (2) được p = 7.
Vậy nguyên tử nitrogen có số đơn vị điện tích hạt nhân là 7.
Bài 2.19 trang 9 SBT Hóa học 10: Magnesium oxide (MgO) được sử dụng để làm dịu cơn đau ợ nóng và chua của chứng đau dạ dày. Tổng số hạt mang điện trong hợp chất MgO là 40. Số hạt mang điện trong nguyên tử Mg nhiều hơn số hạt mang điện trong nguyên tử O là 8. Xác định điện tích hạt nhân của Mg và O.
Lời giải:
Tổng số hạt mang điện trong hợp chất MgO là 40 nên:
(pMg + eMg) + (pO + eO) = 40 hay 2pMg + 2pO = 40 (1)
Lại có, số hạt mang điện trong nguyên tử Mg nhiều hơn số hạt mang điện trong nguyên tử O là 8 nên:
(pMg + eMg) - (pO + eO) = 8 hay 2pMg - 2pO = 8 (2)
Từ (1) và (2) giải hệ phương trình ta được: pMg = 12 và pO = 8.
Vậy điện tích hạt nhân Mg là +12; điện tích hạt nhân O là +8.
Giải SBT Hoá học 10 trang 10
Bài 2.20 trang 10 SBT Hóa học 10: Helium là một khí hiếm được sử dụng rộng rãi trong nhiều ngành công nghiệp như hàng không, hàng không vũ trụ, điện tử, điện hạt nhân và chăm sóc sức khỏe. Nguyên tử helium có 2 proton, 2 neutron và 2 electron. Cho biết khối lượng của electron trong nguyên tử helium chiếm bao nhêu phần trăm khối lượng nguyên tử.
Lời giải:
Ta có: mp ≈ mn ≈ 1u; me = 0,00055u.
Thành phần phần trăm khối lượng electron trong nguyên tử helium:
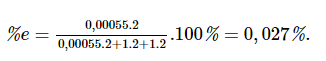
>>>> Bài tiếp theo: Giải SBT Hóa học 10 Chân trời sáng tạo bài 3
Như vậy, VnDoc đã gửi tới các bạn Giải Hóa học 10 bài 2: Thành phần của nguyên tử. Ngoài ra, các em học sinh có thể tham khảo môn Ngữ văn 10 Kết nối tri thức tập 1, Vật Lý 10 Kết nối tri thức và Toán 10 Kết nối tri thức tập 1, Toán 10 Kết nối tri thức tập 2, Sinh 10 Kết nối tri thức đầy đủ khác.

