Giải Hóa 10 Bài 2: Thành phần của nguyên tử CTST
Giải Hóa 10 Chân trời sáng tạo Bài 2: Thành phần của nguyên tử
Giải Hóa 10 Bài 2: Thành phần của nguyên tử CTST được biên soạn hướng dẫn bạn đọc giải chi tiết nội dung câu hỏi Bài 2 Thành phần của nguyên tử trang 13, 14, 15, 16, 17, 18, 19 Hóa 10 Chân trời sáng tạo. Hy vọng thông qua nội dung bạn đọc có thêm tài liệu học tập hữu ích trong quá trình học tập, soạn bạn, lĩnh hội kiến thức mới. Mời các bạn tham khảo chi tiết dưới đây.
>> Bài trước đó: Giải Hóa 10 Bài 1: Nhập môn Hóa học CTST
Mở đầu trang 13 Hóa 10 CTST
Từ rất lâu, các nhà khoa học đã nghiên cứu các mô hình nguyên tử và cập nhật chúng thông qua việc thu thập những dữ liệu thực nghiệm. Nguyên tử gồm những hạt cơ bản nào? Cơ sở nào để phát hiện ra các hạt cơ bản đó và chúng có tính chất gì?
Hướng dẫn trả lời câu hỏi
Nguyên tử gồm các hạt cơ bản: proton, electron và neutron.
+ Hạt electron kí hiệu là e, mang điện tích âm.
+ Hạt proton kí hiệu là p, mang điện tích dương.
+ Hạt neutron kí hiệu là n, không mang điện.
Cơ sở để phát hiện ra các hạt cơ bản trên là:
+ Thông qua thí nghiệm khám phá tia âm cực của Thomson đã phát hiện ra hạt electron.
+ Khi bắn phá hạt nhân nguyên tử nitrogen bằng các hạt α, Rutherford đã phát hiện ra hạt proton.
+ Khi dùng các hạt α bắn phá hạt nhân nguyên tử beryllium, J. Chadwick đã phát hiện hạt neutron.
A. Nội dung câu hỏi thảo luận và củng cố
1. Thành phần cấu tạo nguyên tử
Câu 1. Quan sát hình 2.1 cho biết thành phần nguyên tử gồm những loại hạt nào?
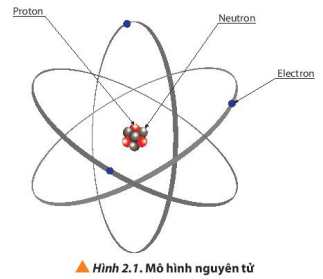
Hướng dẫn trả lời câu hỏi
Nguyên tử gồm hạt nhân chứa proton, neutron và vỏ nguyên tử chứa electron
2. Sự tìm ra Electron
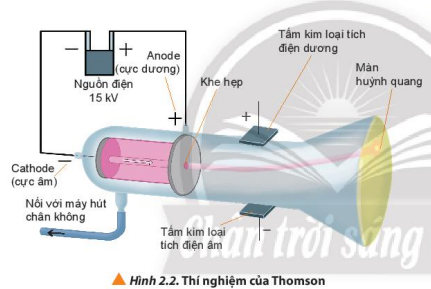
Câu 2. Cho biết vai trò của màn huỳnh quang trong thí nghiệm ở hình 2.2
Hướng dẫn trả lời câu hỏi
Vai trò của màn huỳnh quang trong thí nghiệm ở hình 2.2 dùng để Quan sát và phát hiện ra tia âm cực
Câu 3. Quan sát hình 2.2, giải thích vì sao tia âm cực bị hút về cực dương của trường điện
Hướng dẫn trả lời câu hỏi
Tia âm cực bị hút về cực dương của trường điện vì những tia âm cực tích điện âm nên bị hút về cực dương của trường điện
Câu 4. Nếu một chong chóng nhẹ trên đường đi của tia âm cực thì chong chóng sẽ quay. Từ hiện tượng đó, hãy nêu kết luận về tính chất của tia âm cực
Hướng dẫn trả lời câu hỏi
Tia âm cực (các electron) chuyển động hỗn loạn, va đập vào chong chóng làm chong chóng quay
3. Sự khám phá hạt nhân nguyên tử
 |
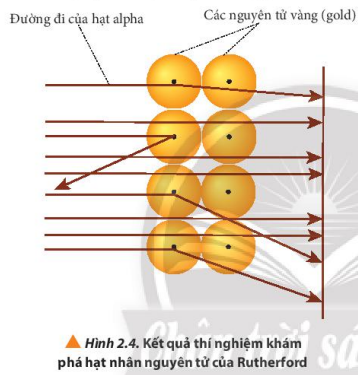 |
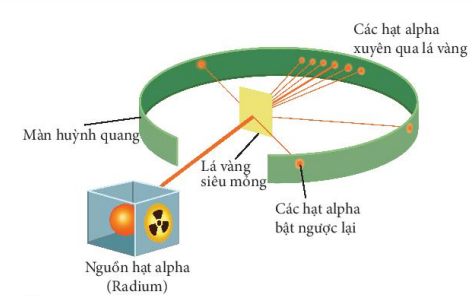
Câu 5. Quan sát hình 2.3 cho biết các hạt α có đường đi như thế nào. Dựa vào hình 2.4 giải thích kết quả thí nghiệm thu được
Hướng dẫn trả lời câu hỏi
Các hạt alpha hầu hết đều xuyên thẳng qua lá vàng.
Giải thích: do nguyên tử có cấu tạo rỗng, ở tâm chứa một hạt nhân mang điện tích dương có kích thước rất nhỏ so với kích thước nguyên tử nên các hạt alpha có thể đi xuyên qua lá vàng.
Câu hỏi củng cố: Nguyên tử oxygen có 8 electron, cho biết hạt nhân của nguyên tử này có điện tích là bao nhiêu?
Hướng dẫn trả lời câu hỏi
Nguyên tử oxygen có 8 electron
=> Số đơn vị điện tích âm của các electron trong nguyên tử oxygen là 8
Mà số đơn vị điện tích dương hạt nhân = số đơn vị điện tích âm của các electron trong nguyên tử
Vậy hạt nhân của nguyên tử oxygen có điện tích: +8
4. Cấu tạo hạt nhân nguyên tử
Câu 6. Điện tích của hạt nhân nguyên tử do thành phần nào quyết định? Từ đó rút ra nhận xét về mối quan hệ giữa số đơn vị điện tích hạt nhân và số proton
Hướng dẫn trả lời câu hỏi
Hạt nhân nguyên tử bao gồm hạt proton và hạt neutron trong đó hạt proton mang điện tích dương, còn hạt neutron không mang điện do đó:
Điện tích của hạt nhân nguyên tử do proton quyết định.
Số đơn vị điện tích hạt nhân = số proton
Câu hỏi củng cố: Nguyên tử natri (sodium) có điện tích hạt nhân là +11. Cho biết số proton và số eletron trong nguyên tử này
Hướng dẫn trả lời câu hỏi
Ta có:
Nguyên tử natri có điện tích hạt nhân là +11
=> Số đơn vị điện tích hạt nhân = 11
Mà số đơn vị điện tích hạt nhân = số proton = số electron trong nguyên tử
=> Nguyên tử natri có 11 proton và 11 electron
5. Kích thước và khối lượng nguyên tử
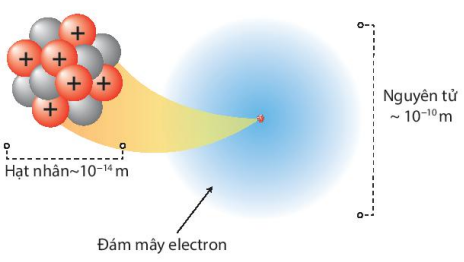
Câu 7. Quan sát hình 2.6, hãy lập tỉ lệ giữa đường kính nguyên tử và đường kính hạt nhân của nguyên tử carbon. Từ đó rút ra nhận xét
Hướng dẫn trả lời câu hỏi
Ta có nguyên tử có đường kính khoảng 10-10 m
Hạt nhân có đường kính khoảng 10-14 m
Xét tỉ lệ ta có:
![]() \(\frac{đường\: kính \: nguyên\; tử }{đường\; kính\: hạt\: nhân} = \frac{10^{-10} }{ 10^{-14}} = 10^{4}\)
\(\frac{đường\: kính \: nguyên\; tử }{đường\; kính\: hạt\: nhân} = \frac{10^{-10} }{ 10^{-14}} = 10^{4}\)
Vậy đường kính nguyên tử lớn hơn đường kính hạt nhân khoảng 10000 lần
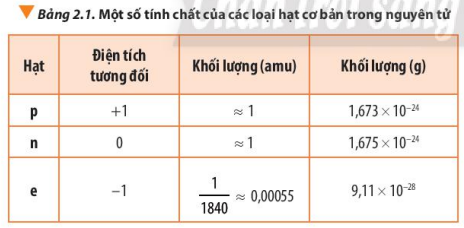
Câu 8. Dựa vào bảng 2.1 hãy lập tỉ lệ khối lượng của một proton với khối lượng của một eletron. Kết quả này nói lên điều gì?
Hướng dẫn trả lời câu hỏi
![]() \(\frac{Khối\: lượng \: proton}{Khối\: lượng \: electron} =\frac{1}{0,00055} =1,818\: lần\)
\(\frac{Khối\: lượng \: proton}{Khối\: lượng \: electron} =\frac{1}{0,00055} =1,818\: lần\)
Kết quả này cho thấy khối lượng của các hạt electron không đáng kể so với khối lượng của proton và neutron, do đó khối lượng của nguyên tử gần bằng khối lượng của hạt nhân
Câu hỏi củng cố: Nguyên tử oxygen -16 có 8 proton, 8 neutron và 8 eletron. Tính khối lượng nguyên tử oxygen theo đơn vị gam và amu
Hướng dẫn trả lời câu hỏi
Nguyên tử oxygen -16 có 8 proton, 8 neutron và 8 eletron
Khối lượng p = 1,673.10-24 gam = 1 amu
Khối lượng n = 1,675.10-24 gam = 1 amu
Khối lượng e = 9,11.10-28 gam = 0,00055 amu
Khối lượng nguyên tử oxygen theo gam là:
8 .1,673.10-24 + 8 . 1,675.10-24 + 8 . 9,11.10-28 ≈ 2,6784 .10-23 (gam)
Khối lượng nguyên tử oxygen theo amu là:
8.1 + 8.1 + 8.0,00055 = 16,0044 (amu)
B. Giải bài tập cuối SGK Hóa 10
Câu 1 trang 19 SGK Hóa 10 CTST
Hãy cho biết dữ kiện nào trong thí nghiệm Rutherford chứng minh nguyên tử có cấu tạo rỗng
Hướng dẫn giải bài tập
Khi bắn các hạt α vào lá vàng, hầu hết các hạt α đi thẳng, không va vào hạt nào (trừ các hạt va vào hạt nhân)
=> Nguyên tử có cấu tạo rỗng
Câu 2 trang 19 SGK Hóa 10 CTST
Thông tin nào sau đây không đúng?
A. Proton mang điện tích dương, nằm trong hạt nhân, khối lượng gần bằng 1 amu
B. Electron mang điện tích âm, nằm trong hạt nhân, khối lượng gần bằng 0 amu
C. Neutron không mang điện, khối lượng gần bằng 1 amu
D. Nguyên tử trung hòa về điện, có kích thước lớn hơn nhiều so với hạt nhân, nhưng có khối lượng gần bằng khối lượng hạt nhân
Hướng dẫn giải bài tập
B Sai vì Electron nằm ở vỏ nguyên tử, không phải nằm trong hạt nhân
Đáp án B
Câu 3 trang 19 SGK Hóa 10 CTST
Mỗi phát biểu dưới đây mô tả loại hạt nào trong nguyên tử?
a) Hạt mang điện tích dương
b) Hạt được tìm thấy trong hạt nhân và không mang điện
c) Hạt mang điện tích âm
Hướng dẫn giải bài tập
a) Hạt mang điện tích dương là: Proton
b) Hạt được tìm thấy trong hạt nhân và không mang điện là: Neutron
c) Hạt mang điện tích âm là: Electron
Câu 4 trang 19 SGK Hóa 10 CTST
a) Cho biết 1g electron có bao nhiêu hạt
b) Tính khối lượng của 1 mol electron (biết hằng số Avogadro có giá trị là 6,022.1023)
Hướng dẫn giải bài tập
a) 1 electron có khối lượng = 9,11.10-28 gam
1 gam electron có số hạt là:
![]() \(\frac{1\: gam\: electron}{khối\: lượng\: 1\: electron } = \frac{1}{9,11.10^{-28} } = 9,11.10^{28} hạt\)
\(\frac{1\: gam\: electron}{khối\: lượng\: 1\: electron } = \frac{1}{9,11.10^{-28} } = 9,11.10^{28} hạt\)
b)
1 electron có khối lượng = 9,11.10-28 gam
Hằng số Avogadro có giá trị là 6,022.1023 hạt electron
=> Khối lượng 1 mol electron = 9,11.10-28 .6,022.1023 = 5,49.10-4 gam
>> Bài tiếp theo: Giải Hóa 10 Bài 3 Nguyên tố hóa học CTST
C. Luyện tập trắc nghiệm Hóa 10 Bài 3
-------------------------------------
Như vậy, VnDoc.com đã gửi tới các bạn Giải Hóa 10 Bài 2: Thành phần của nguyên tử CTST. Ngoài ra, các em học sinh có thể tham khảo môn Hóa 10 Chân trời sáng tạo, Vật Lý 10 Chân trời sáng tạo và Toán 10 Chân trời sáng tạo tập 1, Sinh 10 Chân trời sáng tạo đầy đủ khác.
Hãy tham gia ngay chuyên mục Hỏi đáp các lớp của VnDoc. Đây là nơi kết nối học tập giữa các bạn học sinh với nhau, giúp nhau cùng tiến bộ trong học tập. Các bạn học sinh có thể đặt câu hỏi tại đây:
- Truy cập ngay: Hỏi - Đáp học tập
Hỏi đáp, thảo luận và giao lưu về Toán, Văn, Hóa, Lý, Sinh, Tiếng Anh,... từ Tiểu Học đến Trung học phổ thông nhanh nhất, chính xác nhất.
