Giải Hóa học 10 Kết nối tri thức bài 22
VnDoc xin giới thiệu bài Giải Hóa học 10 bài 22: Hydrogen halide - Muối halide sách Kết nối tri thức được biên soạn hướng dẫn bạn đọc trả lời các nội câu hỏi bài tập SGK Hóa 10 Kết nối tri thức. Hy vọng thông qua nội dung tài liệu, sẽ giúp bạn đọc hoàn thành tốt các nội dung câu hỏi.
Bài: Hydrogen halide - Muối halide
Mở đầu trang 112 Hóa học 10: Hydrochloric acid được sử dụng rộng rãi trong sản xuất, điển hình là dùng để đánh sạch bề mặt kim loại trước khi gia công, sơn, hàn, mạ điện,… Trong công đoạn này, thép được đưa qua các bể chứa dung dịch HCl (được gọi là bể Picking) để tẩy bỏ lớp rỉ sét, sau đó rửa sạch bằng nước trước khi qua các công đoạn tiếp theo. Vậy các ứng dụng trên dựa vào tính chất quan trọng nào của hydrochloric acid?
Phương pháp giải:
Acid tác dụng với kim loại
Lời giải:
- Khi thép được đưa qua các bể chứa dung dịch HCl để tẩy bỏ lớp rỉ sét
=> Thể hiện tính chất tác dụng với kim loại của hydrochloric acid, cụ thể là tác dụng với kim loại sắt
Fe + 2HCl → FeCl2 + H2
I. Hydrogen halide
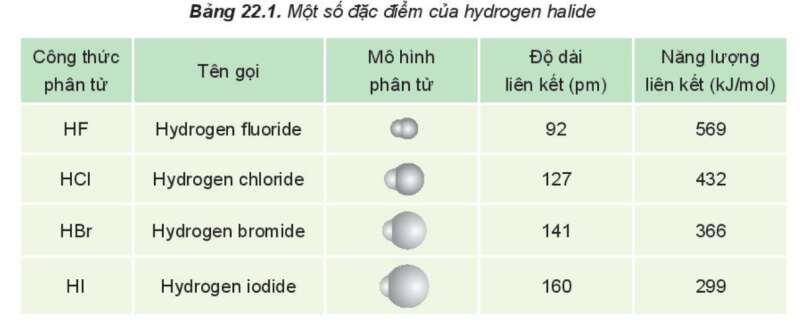
Câu hỏi 1 trang 113 Hóa học 10: Nêu xu hướng biến đổi độ dài liên kết trong dãy HX
Phương pháp giải:
Quan sát bảng 22.1
Lời giải:
Quan sát Bảng 22.1 nhận thấy từ HF đến HI, độ dài liên kết HX tăng dần
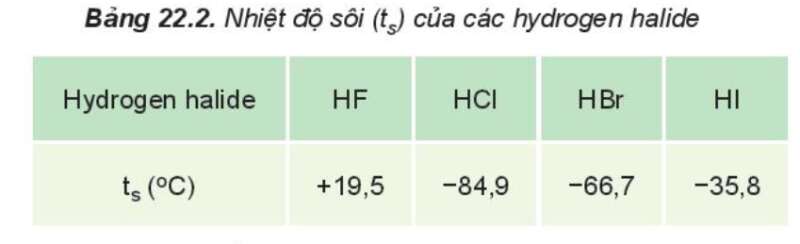
Câu hỏi 2 trang 113 Hóa học 10: Từ Bảng 22.2, hãy nhận xét xu hướng biến đổi nhiệt độ sôi của các hydrogen halide. Giải thích
Phương pháp giải:
Nhiệt độ sôi phụ thuộc vào
+ Lực tương tác van der Waals giữa các phân tử
+ Khối lượng phân tử
Lời giải:
Từ Bảng 22.2 nhận thấy:
- HF lỏng có nhiệt độ sôi cao bất thường là do phân tử HF phân cực mạnh, có khả năng tạo liên kết hydrogen: H-F…H-F…H-F
- Từ HCl đến HI, nhiệt độ sôi tăng do:
+ Lực tương tác van der Waals giữa các phân tử tăng
+ Khối lượng phân tử tăng
II. Hydrohalic acid
Câu hỏi 3 trang 113 Hóa học 10: Ở một nhà máy sản xuất vàng từ quặng, sau khi cho dung dịch chứa hợp chất tan của vàng chảy qua cột chứa kẽm hạt, thu được chất rắn gồm vàng và kẽm. Đề xuất phương pháp thu được vàng tinh khiết
Phương pháp giải:
- Dung dịch HCl hòa tan được kẽm nhưng không hòa tan được vàng
Lời giải:
- Để thu được vàng tinh khiết từ hỗn hợp vàng – kẽm. Ta cho hỗn hợp vào dung dịch HCl
=> Kẽm tác dụng với HCl, vàng không tác dụng với HCl
Zn + 2HCl → ZnCl2 + H2
Giải hóa học 10 trang 114 Kết nối tri thức
Câu hỏi 4 trang 114 Hóa học 10: Viết phương trình hóa học khi cho dung dịch hydrochloric acid lần lượt tác dụng với: Fe, MgO, Cu(OH)2, AgNO3
Phương pháp giải:
- Acid + Kim Loại → Muối + H2
- Acid + Oxide base → Muối + H2O
- Acid + Base → Muối + H2O
- Acid + Muối → Muối mới + Acid mới
Lời giải:
Fe + 2HCl → FeCl2 + H2↑
MgO + 2HCl → MgCl2 + H2O
Cu(OH)2 + 2HCl → CuCl2 + H2O
AgNO3 + HCl → AgCl↓ + HNO3
Câu hỏi 5 trang 114 Hóa học 10: Hydrochloric acid thường được dùng để đánh sạch lớp oxide, hydroxide, muối carbonate bám trên bề mặt kim loại trước khi sơn, hàn, mạ điện
Ứng dụng này dựa trên tính chất hóa học nào của hydrochloric acid?
Lời giải:
- Hydrochloric acid thường được dùng để đánh sạch lớp oxide, hydroxide, muối carbonate vì
+ HCl tác dụng với oxide, hydroxide → Muối + H2O
+ HCl tác dụng với muối carbonate → Muối mới + CO2 + H2O
III. Muối halide
Câu hỏi 6 trang 116 Hóa học 10: Cho biết vai trò của NaBr và NaI khi tham gia phản ứng với sulfuric acid đặc
Phương pháp giải:
NaBr và NaI sẽ đóng vai trò là chất khử khi tham gia phản ứng với sulfuric acid đặc
Lời giải:
- NaBr khử H2SO4 từ S+6 xuống S+4 => NaBr đóng vai trò là chất oxi hóa
2NaBr−1+ 2H2SO4→ Na2SO4 + Br20 + SO2 + 2H2O
- NaI khử H2SO4 từ S+6 xuống S-2 => NaI đóng vai trò là chất oxi hóa
8NaBr−1 + 5H2SO4→4Na2SO4 + 4I20+H2S−2+4H2O
Câu hỏi 7 trang 116 Hóa học 10: Vì sao không dùng trực tiếp nước biển làm nước uống, nước tưới cây?
Phương pháp giải:
Trong nước biển có nồng độ muối ăn cao và có nhiều tạp chất hóa học khác
Lời giải:
- Trong nước biển có nồng độ muối ăn khá cao, từ 3,1 – 3,5% mà thận người chỉ có thể điều tiết lượng muối trong cơ thể ở mức 0,9%
=> Nước biển rất mặn. Việc uống quá nhiều muối vào cơ thể sẽ khiến cho chúng ta mất nhiều nước hơn để thải chính lượng muối đó ra ngoài
Câu hỏi 8 trang 116 Hóa học 10: Nước muối sinh lí thường chia làm 2 loại: loại dùng để tiêm truyền tĩnh mạch và loại dùng để nhỏ mắt, nhỏ mũi, súc miệng, rửa vết thương
a) Loại nào cần vô trùng tuyệt đối và phải dùng theo chỉ định của bác sĩ?
b) Để pha 1 lít nước muối sinh lí NaCl 0,9% dùng làm nước súc miệng thì cần bao nhiêu gam muối ăn?
Phương pháp giải:
a) Tiêm truyền tĩnh mạch là tiêm vào bên trong mạch máu, tiêm vào bên trong cơ thể => Cần phải vô trùng tuyệt đối
b) Nước muối sinh lí = Nước + Muối
- Nước: Dung mỗi hòa tan muối là nước tinh khiết
- Muối: Chỉ thành phần hòa tan trong dung dịch là muối NaCl
Lời giải:
a)
- Nước muối sinh lí dùng để tiêm truyền tĩnh mạch cần phải vô trùng tuyệt đối và dùng theo chỉ định của bác sĩ. Vì nước muối này được tiêm vào mạch máu, tiêm vào bên trong cơ thể người. Do đó cần phải vô trùng hết sức nghiêm ngặt
- Còn nước muối để nhỏ mắt, nhỏ mũi, súc miệng, rửa vết thương (không đưa vào bên trong cơ thể người) thường để loại bỏ chất bẩn chứ không có tác dụng sát khuẩn nên không cần vô trùng tuyệt đối
b) Nước muối sinh lí = Nước + Muối
- 1L nước cất tương đương với 1 kg
- Vì nồng độ muối thấp nên có thể coi 1L dung dịch muối = 1 kg = 1000g
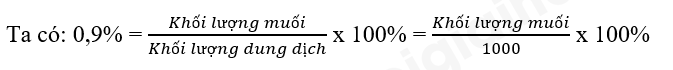
=> Khối lượng muối = 9 gam
Vậy để pha 1 lít nước muối sinh lí NaCl 0,9% dùng làm nước súc miệng thì cần 9 gam muối ăn
>>> Bài tiếp theo: Giải Hóa học 10 Kết nối tri thức bài 23
Như vậy, VnDoc.com đã gửi tới các bạn Giải Hóa học 10 bài 22: Hydrogen halide - Muối halide. Ngoài ra, các em học sinh có thể tham khảo môn Ngữ văn 10 Kết nối tri thức tập 1, Vật Lý 10 Kết nối tri thức và Toán 10 Kết nối tri thức tập 1, Toán 10 Kết nối tri thức tập 2, Sinh 10 Kết nối tri thức đầy đủ khác.
