Chất nào sau đây vừa có tính oxi hóa vừa có tính khử?
Chất nào sau đây vừa có tính oxi hóa vừa có tính khử? được chúng tôi sưu tầm và tổng hợp lí thuyết trong chương trình giảng dạy. Nội dung tài liệu sẽ giúp các bạn học sinh học tốt môn Hóa học lớp 10 hiệu quả hơn. Mời các bạn tham khảo.
Chất nào sau đây vừa có tính oxi hóa vừa có tính khử
Câu hỏi: Chất nào sau đây vừa có tính oxi hóa vừa có tính khử?
- H2S
- O3
- SO2
- H2SO4
Trả lời:
Đáp án đúng: C. SO2
Giải thích
Oxi có số oxi hóa là 0 và -2
S có số oxi hóa là -2, 0 , +4, +6 => S0 và S+4 vừa có tính oxi hóa, vừa có tính khử
=> Trong 4 đáp án có SO2 (S+4) thỏa mãn
I. Sự Oxi hóa và sự khử
1. Sự khử là gì?
- Định nghĩa: Sự khử là sự tách oxi ra khỏi hợp chất
* Ví dụ: CuO + H2 → Cu + H2O
- Trong PTPƯ trên, ta thấy H đã kết hợp với nguyên tố oxi tạo thành H2O, hay H chiếm oxi của CuO.
2. Sự Oxi hóa là gì?
- Định nghĩa: Sự Oxi hóa là sự tác dụng của Oxi với một chất.
* Ví dụ: Fe + O2 → Fe3O4
II. Chất khử và chất Oxi hóa
- Chất khử là chất chiếm oxi của chất khác.
- Chất oxi hóa là đơn chất oxi hoặc chất nhường oxi cho chất khác.
* Ví dụ 1: CuO + H2 → Cu + H2O
- Ta có: Chất khử là: H2 và chất Oxi hóa là CuO
* Ví dụ 2: Mg + CO2 →MgO + C
- Ta có: Chất khử là: Mg và chất Oxi hóa là CO2
III. Phản ứng oxi hoá khử
Phản ứng oxi hóa khử là phản ứng hóa học, trong đó có sự chuyển electron giữa các chất trong phản ứng hay phản ứng oxi hóa khử là phản ứng hóa học trong đó có sự thay đổi số oxi hóa của một số nguyên tố.
1. Lập phương trình phản ứng oxi hóa- khử
Để lập phương trình phản ứng oxi hóa - khử theo phương pháp tháng bằng electron, ta thực hiện các bước sau đây:
- Bước 1: Ghi số oxi hóa của những nguyên tố có số oxi hoá thay đổi
- Bước 2: Viết quá trình oxi hóa và quá trình khử, cân bằng mỗi quá trình
- Bước 3: Tìm hệ số thích hợp sao cho tổng số electron do chất khử nhường bằng tổng số electron mà chất oxi hóa nhận
+ Bước 1 : Xác định số oxi hóa, chất oxi hóa, chất khử

Bước 3: Tìm hệ số cho hai quá trình oxi hóa và khử
Bội số chung nhỏ nhất (BSCNN) = 6 do đó hệ số mỗi quá trình như sau:
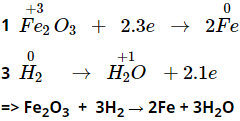
2. Ý nghĩa của phản ứng oxi hóa khử là gì?
Phản ứng oxi hóa khử là quá trình quan trọng của thiên nhiên. Chúng tồn tại ở các dạng như: quá trình trao đổi chất, sự hô hấp của con người, quá trình thực vật hấp thụ khí cacbonic giải phóng oxi.
Ngoài ra, phản ứng này cũng xảy ra ở sự đốt cháy nhiên liệu trong các động cơ, quá trình điện phân, phản ứng trong pin và trong acquy…
Quá trình sản xuất ví dụ như luyện kim, chế tạo hóa chất, chất dẻo, dược phẩm, phân bón hóa học… cũng đều có sự xuất hiện của phản ứng oxi hóa khử.
IV. Bài tập vận dụng
Bài 1: Cho phản ứng sau:
- 2HgO → to2Hg + O2.
- CaCO3→ toto CaO + CO2.
- 2Al(OH)3→ to Al2O3 + 3H2O.
- 2NaHCO3→ to Na2CO3+ CO2 + H2O.
phản ứng oxi hóa – khử là đáp án nào
Lời giải:
Những phản ứng theo đề bài cho, phản ứng oxi hóa – khử là: A.
2HgO → to 2Hg + O2.
Hg2+ + 2e → Hg0
2O2- → O2 + 4e
Còn các phản ứng khác không phải là phản ứng oxi hóa khử.
Bài 2: Cho các phản ứng sau:
- 4NH3+ 5O2→ 4NO + 6H2O.
- 2NH3+ 3Cl2→ N2 + 6HCl.
- 2NH3+ 3CuO → 3Cu + N2+ 3H2O.
- 2NH3+ H2O2 + MnSO4→ MnO2 + (NH4)2SO4.
Ở phản ứng nào NH3 không đóng vai trò chất khử?
Lời giải:
Phản ứng NH3 không đóng vai trò chất khử.
D. 2NH3+ H2O2 + MnSO4→ MnO2 + (NH4)2SO4.
Do N không thay đổi số oxi hóa trước và sau phản ứng.
Bài 3: Trong số các phản ứng sau:
- HNO3+ NaOH → NaNO3 + H2O.
- N2O5+ H2O → 2HNO3.
- 2HNO3+ 3H2S → 3S + 2NO + 4H2O.
- 2Fe(OH)3→ Fe2O3+ 3H2O.
Phản ứng nào là phản ứng oxi hóa – khử.
Lời giải:
Trong các phản ứng trên chỉ có phản ứng C là phản ứng oxi hóa – khử vì có sự thay đổi số oxi hóa của các nguyên tố.
Bài 4: Trong phản ứng 3NO2 + H2O → 2HNO3 + NO. NO2 đóng vai trò gì?
- Chỉ là chất oxi hóa.
- Chỉ là chất khử.
- Là chất oxi hóa, nhưng đồng thời cũng là chất khử.
- Không là chất oxi hóa, không là chất khử.
Chọn đáp án đúng.
Lời giải:
NO2 đóng vai trò vừa là chất oxi hóa vừa là chất khử: C đúng
Bài 5: Phân biệt chất oxi hóa và sự oxi hóa, chất khử và sự khử. Lấy thí dụ để minh họa.
Lời giải:
Chất oxi hóa là chất nhận electron.
Sự oxi hóa một chất là làm cho chất đó nhường electron.
Chất khử là chất nhường electron.
Sự khử một chất là sự làm cho chất đó thu electron.
- Nguyên tử Fe nhường electron, là chất khử. Sự nhường electron của Fe được gọi là sự oxi hóa nguyên tử sắt.
- Ion đồng nhận electron, là chất oxi hóa. Sự nhận electron của ion đồng được gọi là sự khử ion đồng.
----------------------------------------
Trên đây VnDoc đã giới thiệu tới các bạn nội dung bài Chất nào sau đây vừa có tính oxi hóa vừa có tính khử? Để có kết quả học tập tốt và hiệu quả hơn, VnDoc xin giới thiệu tới các bạn học sinh tài liệu Giải bài tập Hóa học 10, Chuyên đề Vật Lý 10, Chuyên đề Hóa học 10, Giải bài tập Toán 10. Tài liệu học tập lớp 10 mà VnDoc tổng hợp biên soạn và đăng tải.

