Giải Hóa học 10 Cánh diều bài 17
Giải Hóa học 10 bài 17: Nguyên tố và đơn chất halogen được VnDoc biên soạn hướng dẫn bạn đọc trả lời các nội dung câu hỏi bài tập sách giáo khoa Hoá 10 Cánh diều.
Bài: Nguyên tố và đơn chất halogen
Mở đầu trang 99 Hóa học 10: Vì sao nước chlorine được sử dụng phổ biến để khử trùng, sát khuẩn?
Lời giải:
- Nước chlorine có thành phần là HCl và HClO có tính oxi hóa mạnh
=> Nước chlorine có tính tẩy màu được dùng để khử trùng và sát khuẩn, tẩy trắng sợi, vải, giấy
I. Giới thiệu về nguyên tố nhóm VIIA
II. Đơn chất halogen
Phương pháp giải:
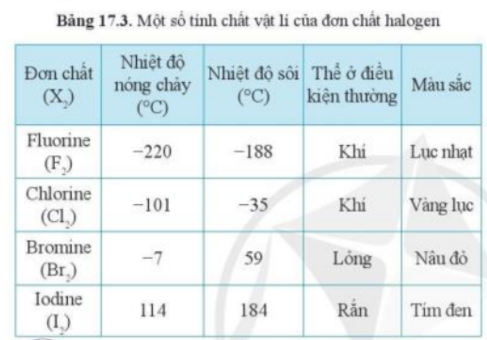
Trong bảng 17.3, thể của các halogen ở điều kiện thường biến đổi từ khí → lỏng → rắn
Lời giải:
- Theo bảng 17.3, xu hướng biến đổi trạng thái của các halogen ở điều kiện thường từ: khí → lỏng → rắn
- Mà astatine đứng dưới cùng trong nhóm halogen
=> Astatine tồn tại ở thể rắn trong điều kiện thường
- Giải thích: Do sự tăng khối lượng phân tử và sự tăng tương tác van der Waals
Luyện tập 2 trang 101 Hóa học 10: Trong điều kiện thường, halogen nào ở thể rắn? Vì sao
Phương pháp giải:
- Dựa vào thông tin bảng 17.3

- Giải thích: Khối lượng phân tử, sự tăng tương tác van der Waals
Lời giải:
- Quan sát Bảng 17.3, nhận thấy trong điều kiện thường có Iodine (I2) là ở thể rắn
- Giải thích:
+ Khối lượng phân tử cao
+ Lực tương tác van der Waals giữa phân tử iodine mạnh
Phương pháp giải:
- Các nguyên tố halogen có 7 electron ở lớp ngoài cùng
- Nguyên tố calcium có 2 electron ở lớp ngoài cùng
Lời giải:
- Nguyên tử Fluorine có 7 electron ở lớp ngoài cùng => Nhận 1 electron từ nguyên tử Calcium để đạt cấu hình electron của khí hiếm
- Nguyên tử Calcium có 2 electron ở lớp ngoài cùng => Nhường 2 electron cho 2 nguyên tử Fluorine để đạt cấu hình electron của khí hiếm
Phương pháp giải:
- Nguyên tử Phosphorus có 5 electron ở lớp ngoài cùng => Có xu hướng nhận thêm 3 electron
- Nguyên tử Chlorine có 7 electron ở lớp ngoài cùng => Có xu hướng nhận thêm 1 electron
Lời giải:
- Trong phân tử phosphorus trichloride gồm 2 nguyên tố: P và Cl
+ Nguyên tử P có 5 electron ở lớp ngoài cùng => Góp chung 3 electron độc thân để hình thành 3 liên kết cộng hóa trị
+ Nguyên tử Cl có 7 electron ở lớp ngoài cùng => 3 nguyên tử Cl, mỗi nguyên tử góp chung 1 electron độc thân để hình thành 3 liên kết cộng hóa trị với P.
=> Khi đó, quanh P và Cl đều có 8 electron như khí hiếm Argon.
- Công thức Lewis của phân tử:
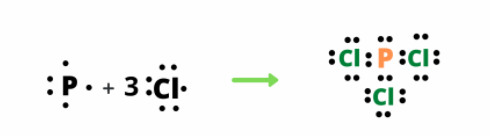
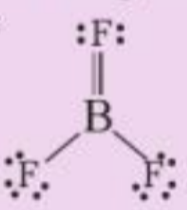
a) Viết phương trình hóa học tạo chất trên từ các đơn chất
b) Phân tử BF3 có bao nhiêu liên kết σ và bao nhiêu liên kết п?
Phương pháp giải:
a) Phương trình hóa học: B + F2 → ?
b) Liên kết đơn còn gọi là liên kết σ, liên kết đôi gồm 1 liên kết σ và 1 liên kết п
Lời giải:
a) Phương trình hóa học: 2B + 3F2 → 2BF3
b) Trong phân tử BF3 có 2 liên kết đơn, 1 liên kết đôi (gồm 1 liên kết σ và 1 liên kết п)
=> Trong phân tử BF3 có 3 liên kết σ và 1 liên kết п
Phương pháp giải:
Phản ứng hóa học: Br2(aq) + H2O(l) ⇌ HBr(aq) + HBrO(aq)
Lời giải:
Sau khi nhỏ nhanh vài giọt bromine vào ống nghiệm chứa nước, dung dịch bromine có những chất: Br2, H2O, HBr, HBrO.
Br2(aq) + H2O(l) ⇌ HBr(aq) + HBrO(aq)
- Vì phản ứng xảy ra thuận nghịch nên trong dung dịch có cả chất tham gia và chất sản phẩm
Phương pháp giải:
Halogen là những chất oxi hóa mạnh
Lời giải:
- Halogen là những chất oxi hóa mạnh, dễ dàng tác dụng với các chất khác trong tự nhiên: tác dụng với nước, hydrogen,…
=> Trong tự nhiên, các halogen không tồn tại ở dạng đơn chất mà tồn tại ở dạng hợp chất
Bài tập (trang 107, 108)
Phương pháp giải:
Các halogen có tính oxi hóa mạnh hơn sẽ phản ứng với muối halide của halogen có tính oxi hóa yếu hơn để tạo ra các halogen có tính oxi hóa yếu hơn
Lời giải:
Cl2 + 2NaBr → 2NaCl + Br2
=> Cl2 có tính oxi hóa mạnh hơn sẽ phản ứng với NaBr tạo thành halogen có tính oxi hóa yếu hơn là Br2
=> Chlorine có tính oxi hóa mạnh hơn bromine
NaCl (aq) + H2O (l) → A (aq) + X (g) + Y (g) (*)
Từ phản ứng giữa Y với dung dịch A sẽ sản xuất được hỗn hợp tẩy rửa phổ biến.
Từ phản ứng kết hợp giữa X và Y sẽ sản xuất được hydrogen chlorine
a) Hãy cho biết công thức hóa học của A, X, Y
b) Hoàn thành phương trình hóa học (*)
Phương pháp giải:
- Chất tẩy rửa phổ biến là nước Javel: NaCl và NaClO
- Để sản xuất được hydrogen chloride cần: Cl2 và H2
Lời giải:
- Chất tẩy rửa phổ biến là nước Javel gồm có NaCl và NaClO
=> Hai chất tác dụng với nhau để tạo thành nước Javel là: NaOH và Cl2
- Vì A ở dạng dung dịch, Y ở dạng khí
=> A là dung dịch NaOH, Y là khí Cl2
- Để sản xuất được hydrogen chloride cần: Cl2 và H2
- Mà Y là khí Cl2
=> X là khí H2
a) Công thức hóa học của A, X, Y lần lượt là: NaOH, H2, Cl2
b) Phương trình hóa học
2NaCl (aq) + 2H2O (l) → 2NaOH (aq) + H2 (g) + Cl2 (g) (*)
Dựa vào xu hướng biến đổi một số tính chất của nhóm halogen, hãy dự đoán:
a) Tính oxi hóa của nguyên tử astatine mạnh hơn hay yếu hơn so với nguyên tử iodine?
b) Đơn chất astatine có màu đậm hơn hay nhạt hơn so với đơn chất iodine?
Phương pháp giải:
- Trong nhóm halogen, đi từ F đến I, tính oxi hóa giảm dần
- Trong nhóm halogen, đi từ F đến I, màu sắc đậm dần
Lời giải:
a) Trong nhóm halogen, đi từ F đến I có độ âm điện giảm dần
=> Tính oxi hóa giảm dần
=> Tính oxi hóa của nguyên tử astatine yếu hơn so với nguyên tử iodine
b) Trong nhóm halogen, đi từ F đến I có màu sắc của các đơn chất đậm dần
=> Đơn chất astatine có màu đậm hơn so với đơn chất iodine
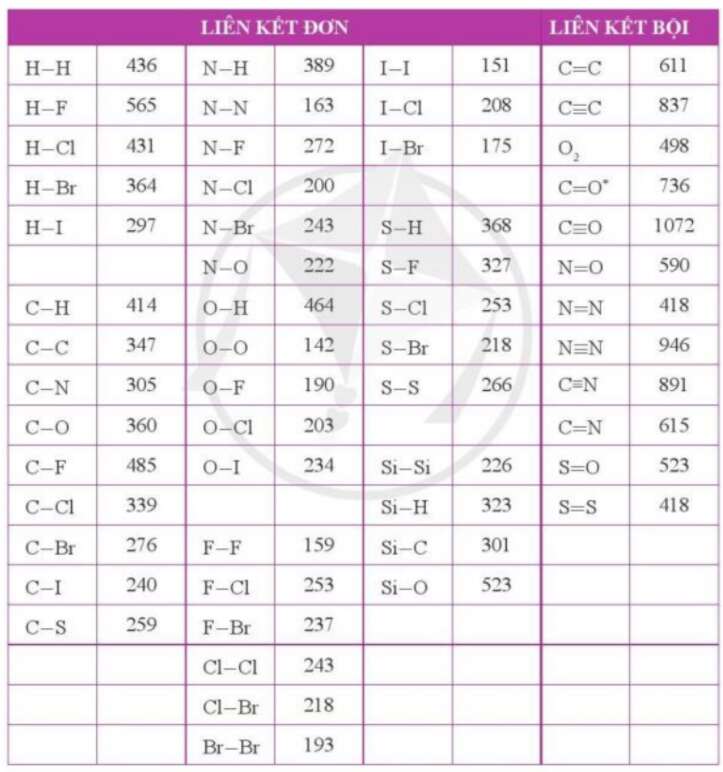
Bài 4 trang 107 Hóa học 10: Tra cứu các giá trị năng lượng liên kết ở phụ lục 2
a) Hãy tính biến thiên enthalpy chuẩn ∆rH0298 của 2 phản ứng dưới đây:
F2(g) + H2(g) → 2HF (g)
O2(g) + 2H2(g) → 2H2O(g)
b) Ở hai phản ứng trên, fluorine và oxygen đều đóng vai trò là chất oxi hóa. Dựa vào giá trị ∆rH0298, cho biết phản ứng oxi hóa – khử nào thuận lợi hơn
Phương pháp giải:
a)
∆rH0298 = Eb(F2) + Eb(H2) – 2xEb(HF)
∆rH0298 = Eb(O2) + 2xEb(H2) – 2x2xEb(OH)
b)
Giá trị biến thiên enthalpy nào âm hơn thì phản ứng đó diễn ra thuận lợi hơn
Lời giải:
a)
- Xét phản ứng: F2(g) + H2(g) → 2HF (g)
+ Ta có: ∆rH0298 = Eb(F2) + Eb(H2) – 2xEb(HF) = 159 + 436 – 2x565 = -535 (kJ/mol)
- Xét phản ứng: O2(g) + 2H2(g) → 2H2O(g)
+ Ta có: ∆rH0298 = Eb(O2) + 2xEb(H2) – 2x2xEb(OH) = 142 + 2x436 – 2x2x464 = -842 (kJ/mol)
b)
Giá trị biến thiên enthalpy của phản ứng (2) âm hơn giá trị biến thiên enthalpy của phản ứng (1)
=> Phản ứng oxi hóa – khử (2) diễn ra thuận lợi hơn
Theo quy chuẩn kĩ thuật quốc gia (QCVN 01 – 1: 2018/BYT), hàm lượng chlorine tự do đối với nước sạch sử dụng cho mục đích sinh hoạt từ 0,2 – 1 mgL-1. Nếu hàm lượng chlorine nhỏ hơn 0,2 – 1 mgL-1 thì không tiêu diệt hết vi khuẩn và không xử lí được hết chất hữu cơ. Ngược lại, lượng chlorine trong nước lớn hơn 1,0 mgL-1 sẽ gây dị ứng
Carbon trong than hoạt tính sẽ tương tác trực tiếp với chlorine, giúp loại bỏ chlorine và các hợp chất chlorine và các hợp chất chlorine bằng cơ chế hấp thụ bề mặt. Khi chiếu tia cực tím với cường độ cao vào nước cũng làm giảm lượng chlorine. Các máy lọc nước RO (reverse osmosis: thẩm thấu ngược) cũng có thể giúp loại bỏ lượng chlorine trong nước một cách hiệu quả
Hãy trả lời các câu hỏi sau đây:
a) Dấu hiệu nào cho thấy chlorine có trong nước sinh hoạt
b) Vì sao người ta cần cho chlorine đến dư vào nước sinh hoạt
c) Cho biết một số phương pháp có thể loại bỏ khí chlorine dư trong nước sinh hoạt
Phương pháp giải:
a) Chlorine có mùi xốc
b) Ngăn ngừa sự tái nhiễm của vi khuẩn
c) Tham khảo phần cuối của đoạn văn trên
Lời giải:
a) Chlorine có mùi xốc, nên khi sử dụng nước sinh có chlorine, chúng ta sẽ ngửi thấy mùi của nước chlorine
b) Trong quá trình khử trùng, người ta phải cho một lượng chlorine dư vào nước sinh hoạt. Lượng chlorine dư trong nước sinh hoạt còn có tác dụng ngăn ngừa sự tái nhiễm của vi khuẩn trong quá trình phân phối trong đường ống dẫn nước và trữ nước tại nhà
c) Một số phương pháp để loại bỏ khí chlorine dư trong nước sinh hoạt:
- Sử dụng máy lọc nước than hoạt tính
- Phơi chậu nước ra ngoài ánh nắng mặt trời => Tia cực tím với cường độ cao vào nước cùng làm giảm lượng chlorine
- Sử dụng máy lọc nước RO (thẩm thấu ngược) cũng có thể giúp loại bỏ lượng chlorine trong nước
>>>> Bài tiếp theo: Giải Hóa học 10 Cánh diều bài 18
Như vậy, VnDoc.com đã gửi tới các bạn Giải Hóa 10 bài 17: Nguyên tố và đơn chất halogen. Ngoài ra, các em học sinh có thể tham khảo môn: Vật Lý 10 Cánh Diều và Toán 10 Cánh Diều Tập 1, Toán 10 Cánh Diều Tập 2, Sinh 10 Cánh Diều đầy đủ khác.

