Hợp chất của nguyên tố R với hidro là RH2 công thức oxit cao nhất của R
Hợp chất của nguyên tố R với hidro là RH2 công thức oxit cao nhất của R được VnDoc sưu tầm và tổng hợp lí thuyết trong chương trình giảng dạy. Nội dung tài liệu sẽ giúp các bạn học sinh học tốt môn Hóa học lớp 10 hiệu quả hơn. Mời các bạn tham khảo.
Hợp chất của một nguyên tố có công thức RH2
Câu hỏi: Hợp chất của một nguyên tố có công thức RH2. Oxit cao nhất của R chiếm 40% khối lượng R. R là:
- N (M=14)
- Se (M=79)
- S (M=32)
- Ca (M=40)
Trả lời:
Chọn C
Oxit cao nhất của R có dạng RO3. Theo bài ra có:
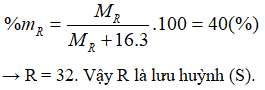
A. Dạng bài tập xác định tên nguyên tố khi biết thành phần nguyên tố trong hợp chất
I. Lý thuyết và phương pháp giải
Cần nhớ một số điểm sau:
- Hóa trị cao nhất với oxi của nguyên tố = STT nhóm A.
- Hóa trị với H (nếu có) = 8 - hóa trị cao nhất với oxi.
- % khối lượng của A trong hợp chất AxBy là: %A= MA*100/M.
- Muốn xác định nguyên tố đó là nguyên tố nào cần tìm được M =?.
II. Ví dụ minh họa
Ví dụ 1. Một nguyên tố tạo hợp chất khí với hidro có công thức RH3. Nguyên tố này chiếm 25,93% về khối lượng trong oxit bậc cao nhất. Xác định tên nguyên tố.
Hướng dẫn:
Hợp chất với Hiđro là RH3 ⇒ Chất cao nhất với oxi có công thức là: R2 O5
Ta có: (2.R) / (16.5) = 25,93/74,07
⇒ R= 14 ⇒ R là nguyên tố Nitơ
Ví dụ 2. Nguyên tố R có hóa trị cao nhất trong oxit gấp 3 lần hóa trị trong hợp chất với hiđro. Hãy cho biết hóa trị cao nhất của R trong oxit.
Hướng dẫn:
Gọi hóa trị cao nhất của R trong oxit là m, hóa trị trong hợp chất với hiđro là n. Ta có: m + n = 8.
Theo bài: m = 3n. Từ đây tìm được m = 6; n = 2.
Ví dụ 3. Oxit cao nhất của nguyên tố R có dạng R2O5. Trong hợp chất của R với hiđro ở thể khí có chứa 8,82 % hiđro về khối lượng. Công thức phân tử của hợp chất khí với hiđro là (C = 12, N= 14, P= 31, S= 32)
A. NH3.
B. H2S.
C. PH3.
D. CH4.
Hướng dẫn:
Oxit cao nhất của R là R2O5 nên R thuộc nhóm VA.
⇒ Hợp chất với H là RH3
Ta có 3/R = 8,82 / 91,18 ⇒ R=31 (P)
⇒ Chọn C
Ví dụ 4. Oxit cao nhất của một nguyên tố chứa 72,73% oxi, còn trong hợp chất khí với hidro chứa 75% nguyên tố đó. Viết công thức oxit cao nhất và hợp chất khí với hidro.
Hướng dẫn:
Gọi hợp chất với hidro có công thức là : RHx
⇒ Hợp chất với oxi có công thức là R2 Ox-8
Ta có:
(1) (2.R) / 16(8-x )= 27,27/72,73.
(2) R/x = 75/ 25 = 3
⇒ R= 3x thay vào pt(1) ta có đáp án : x= 4 và ⇒ R = 12
Vậy R là cacbon ⇒ CO2 và CH4
Ví dụ 5. Oxit cao nhất của nguyên tố R thuộc nhóm VIA có 60% oxi về khối lượng. Hãy xác nguyên tố R và viết công thức oxit cao nhất.
Hướng dẫn:
Nhóm VIA nên hợp chất oxit bậc cao là RO3
Ta có: R/ 48 = 40/60 vậy R= 32 (Lưu huỳnh)
⇒ Công thức Oxit cao nhất là: SO3
B. Dạng bài tập xác định nguyên tố thông qua nguyên tử khối
I. Lý thuyết và phương pháp giải
Muốn xác định tên nguyên tố cần tìm được M dựa vào thành phần phần trăm nguyên tố M trong hỗn hợp; dựa vào các phản ứng hóa học, các tính chất của M.….
II. Ví dụ minh họa
Ví dụ 1. Oxit cao nhất của một nguyên tố ứng với công thức RO3. Hợp chất của nó với hidro có 5,88% H về khối lượng. Xác định R.
Hướng dẫn:
Oxit cao nhất là RO3 → R thuộc nhóm VIA.
Hợp chất với hidro có dạng RH2.

Đó là nguyên tố lưu huỳnh (S).
Ví dụ 2. Cho 10 gam kim loại A (thuộc nhóm IIA) tác dụng với nước, thu được 6,11 lit khí hiđro (đo ở 25oC và 1 atm).
a. Hãy xác định tên của kim loại M đã dùng.
b. Cho 4 gam kim loại A vào cốc đựng 2,5lit dung dịch HCl 0,06M thu được dung dịch B.
Hướng dẫn:
A + 2H2O → A(OH)2 + H2
a a
Số mol khí H2 = 0,25 (mol) ⇒ a = 0,25
Ta có: MA = 10/0,25 = 40 (Ca).
Số mol Ca = 4/40 = 0,1 mol. Các phương trình phản ứng:
Ca + 2HCl → CaCl2 + H2
(mol): 0,075 0,15 0,075
Ca + 2H2O → Ca(OH)2 + H2
(mol): 0,025 0,025
Dung dịch B gồm: CaCl2 = 0,075 mol và Ca(OH)2 = 0,025 mol.
Ví dụ 3: Nguyên tử của nguyên tố C có cấu hình electron lớp ngoài cùng là ns2np4. Trong hợp chất khí của X với hidro, X chiếm 94,12% khối lượng. Phần trăm khối lượng của nguyên tố X trong oxit cao nhất là:
A. 50,00%
B. 27,27%
C. 60,00%
D. 40,00%
Hướng dẫn:
X: ns2np4 → X thuộc nhóm IVA → hợp chất khí với H là XH2 → oxit cao nhất là XO3.
C. Cách giải bài tập xác định tên nguyên tố dựa vào đặc điểm chu kì, nhóm hay, chi tiết
I. Lý thuyết và phương pháp giải
Cần nhớ:
- Tổng số hiệu nguyên tử 4 < ZT < 32 thì A, B sẽ thuộc các chu kỳ nhỏ hay ZA - ZB = 8.
- Nếu ZT > 32 thì ta phải xét cả 3 trường hợp:
+ A là H.
+ A và B cách nhau 8 đơn vị.
+ A và B cách nhau 18 đơn vị.
Do hai nguyên tố thuộc cùng một nhóm nên tính chất tương tự nhau, vì vậy với những bài toán liên quan đến hỗn hợp phản ứng ta thay hỗn hợp bằng một công thức chung, sau đó tìm M− rồi chọn nguyên tố thuộc hay chu kì của cùng nhóm sao cho:
MA < M− < MB (MA < MB)
II. Ví dụ minh họa
Ví dụ 1. Cho 8,8 gam một hỗn hợp hai kim loại nằm ở hai chu kì liên tiếp nhau và thuộc nhóm IIIA, tác dụng với HCl dư thì thu được 6,72 lít khí hidro (đktc). Dựa vào bảng tuần hoàn cho biết tên hai kim loại đó.
Hướng dẫn:
Kí hiệu hai kim loại nhóm IIIA là M, nguyên tử khối trung bình là M−
Phương trình hóa học có dạng: 2M + HCl → 2MCl2 + 3H2
nH2 = 6,72/22,4 = 0,3 (mol)
nM = 2/3 nH2 = 0,2 (mol)
theo đầu bài: M− .0,2 = 8,8 → M− = 44
hai kim loại thuộc hai chu kì liên tiếp, một kim loại có nguyên tử khối nhỏ hơn 44 và một kim loại có nguyên tử khối lớn hơn 44.
Dựa vào bảng tuần hoàn, hai kim loại đó là:
Al (M = 27 < 44) và Ga (M = 69,72 > 44).
Ví dụ 2: A và B là hai nguyên tố ở cùng một nhóm và thuộc hai chu kì liên tiếp trong bảng tuần hoàn. Tổng số proton trong hai hạt nhân nguyên tử của A và B bằng 32. Hãy viết cấu hình electron của A, B và của các ion mà A và B có thể tạo thành.
Hướng dẫn:
Theo bài ra, tổng số proton trong hai hạt nhân nguyên tử của A và B bằng 32 nên ZA + ZB = 32.
Trường hợp 1: ZB - ZA = 8. Ta tìm được ZA = 12; ZB = 20.
Cấu hình electron:
A : 1s22s22p63s2 (chu kỳ 3, nhóm IIA).
và B: 1s22s22p63s23p64s2 (chu kỳ 4, nhóm IIA).
Ion A2+: 1s22s22p6 và B2+: 1s22s22p63s23p6.
Trường hợp 2: ZB - ZA = 18. Ta tìm được ZA = 7; D = 25.
Cấu hình electron:
A: 1s22s22p3 (chu kỳ 2, nhóm VA).
và B: 1s22s22p63s23p63d54s2 (chu kỳ 4, nhóm VIIB).
Trường hợp này A, B không cùng nhóm nên không thỏa mãn.
----------------------------------------
Trên đây VnDoc đã giới thiệu tới các bạn nội dung bài Hợp chất của nguyên tố R với hidro là RH2 công thức oxit cao nhất của R. Để có kết quả học tập tốt và hiệu quả hơn, VnDoc xin giới thiệu tới các bạn học sinh tài liệu Giải bài tập Hóa học 10, Chuyên đề Vật Lý 10, Chuyên đề Hóa học 10, Giải bài tập Toán 10. Tài liệu học tập lớp 10 mà VnDoc tổng hợp biên soạn và đăng tải.


