Cách điều chế Iot
Cách điều chế Iot được chúng tôi sưu tầm và tổng hợp lí thuyết trong chương trình giảng dạy. Nội dung tài liệu sẽ giúp các bạn học sinh học tốt môn Hóa học lớp 10 hiệu quả hơn. Mời các bạn tham khảo.
Cách điều chế Iot
Câu hỏi: Cách điều chế Iot
Lời giải:
- Trong công nghiệp, iot được sản xuất từ rong biển.
- Iốt có thể thu được ở dạng rất tinh khiết bằng phản ứng giữa KI với sunfat đồng (II). Cũng có vài cách khác để tách nguyên tố hóa học này. Mặc dù nguyên tố này khá hiếm, tảo bẹ và một số loài cây khác có khả năng hấp thụ và tập trung iốt trong cơ thể chúng, dẫn đến việc mang iốt vào dây chuyền thức ăn tự nhiên và giúp việc điều chế iốt có giá thành thấp.
- Cho tác dụng dung dịch với chất oxi hoá để oxi hoá I- thành I2
2NaI + Cl2 -> 2NaCl + I2
I. Trạng thái tự nhiên
- So với các halogen khác, iot có trong vỏ trái đất ít nhất.
- Hợp chất iot có trong nước biển nhưng rất ít.
- Iot còn có trong tuyến giáp của người tuy nhỏ nhưng rất quan trọng vì nếu thiếu sẽ bị bệnh bướu cổ.
II. Tính chất
1. Tính chất vật lý
- Iot là tinh thể màu đen tím, có vẻ sáng kim loại.
- Hiện tượng thăng hoa:
+ Đun nóng, iot không nóng chảy mà biến thành thể hơi.
+ Làm lạnh, hơi iot chuyển thành tinh thể, không thông qua thể lỏng.
- Ít tan trong nước, tan nhiều trong dung môi hữu cơ.
2. Tính chất hóa học
Tác dụng với kim loại
- Iot oxi hóa được nhiều kim loại nhưng chỉ xảy ra khi đun nóng hoặc có xúc tác.
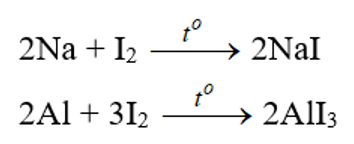
Tác dụng với hidro
- Ở nhiệt độ cao iot mới phản ứng với hiđro:
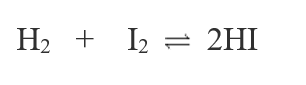
- Hiđro iotua không bền, ngay ở những điều kiện tạo thành một phần bị phân hủy thành hiđro và iot:
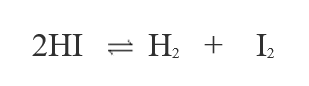
- Do vậy, phản ứng giữa hiđro và iot không thực hiện đến cùng.
* Lưu ý:
- Hiđro iotua tan trong nước tạo thành axit tương ứng có cùng công thức: Axit Iothiđric HI là axit mạnh.
HF < HCl < HBr < HI
- Không dùng dung dịch H2SO4 đặc và muối iodua để điều chế HI: Tính khử của HI
8HI + H2SO4đ → 4I2 + H2S + 4H2O
Iot có tính oxi hóa kém clo và brom:
Cl2 + 2NaI → 2NaCl + I2
Br2 + 2NaI → 2NaBr + I2
Tính khử của axit HI
- HI có tính khử mạnh có thể khử được axit H2SO4 đặc.
8HI + H2SO4 → 4I2 + H2S + 4H2O
2HI + 2FeCl3 → FeCl2 + I2 + 2HCl
Tính chất đặc trưng của Iot
- Iot có tính chất đặc trưng là tác dụng với hồ tinh bột tạo thành hợp chất có màu xanh.
III. Ứng dụng, điều chế
Ứng dụng
- Dùng nhiều dưới dạng cồn iot (dd iot 5% trong ancol etylic) làm chất sát trùng.
- Có trong thành phần của nhiều dược phẩm.
- Trộn với lượng nhỏ KI và KIO3 thành muối iot giúp tránh các rối loạn do thiếu iot.
Điều chế
- Iốt có thể thu được ở dạng rất tinh khiết bằng phản ứng giữa KI với sunfat đồng (II). Cũng có vài cách khác để tách nguyên tố hóa học này. Mặc dù nguyên tố này khá hiếm, tảo bẹ và một số loài cây khác có khả năng hấp thụ và tập trung iốt trong cơ thể chúng, dẫn đến việc mang iốt vào dây chuyền thức ăn tự nhiên và giúp việc điều chế iốt có giá thành thấp.
- Cho tác dụng dung dịch với chất oxi hoá để oxi hoá I- thành I2
2NaI + Cl2 -> 2NaCl + I2
----------------------------------------
Trên đây VnDoc đã giới thiệu tới các bạn nội dung bài Cách điều chế Iot. Để có kết quả học tập tốt và hiệu quả hơn, VnDoc xin giới thiệu tới các bạn học sinh tài liệu Giải bài tập Hóa học 10, Chuyên đề Vật Lý 10, Chuyên đề Hóa học 10, Giải bài tập Toán 10. Tài liệu học tập lớp 10 mà VnDoc tổng hợp biên soạn và đăng tải.
