Kí hiệu nguyên tử là gì? Cách viết kí hiệu nguyên tử?
VnDoc xin giới thiệu bài Kí hiệu nguyên tử là gì? Cách viết kí hiệu nguyên tử? được chúng tôi sưu tầm và tổng hợp lí thuyết trong chương trình giảng dạy. Nội dung tài liệu sẽ giúp các bạn học sinh học tốt môn Hóa học lớp 10 hiệu quả hơn. Mời các bạn tham khảo.
Kí hiệu nguyên tử là gì?
Câu hỏi: Kí hiệu nguyên tử là gì? Cách viết kí hiệu nguyên tử? Nêu ví dụ minh họa
Trả lời
- Kí hiệu của nguyên tử
+ Là sự thể hiện những đặc trưng cơ bản của nguyên tử
+ Bao gồm: số đơn vị điện tích hạt nhân (Z) và số khối (A).
- Cách viết kí hiệu nguyên tử:
+ Đặt kí hiệu các chỉ số đặc trưng ở bên trái kí hiệu nguyên tố X với số khối A ở phía trên
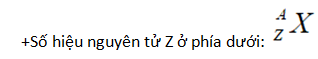
Trong đó:
X: là ký hiệu của nguyên tố
Z: là số hiệu nguyên tử
A: là số khối, A = Z + N.
1. Nguyên tử là gì?
+ Nguyên tử là hạt siêu nhỏ và trung hòa về điện.
+ Thành phần nguyên tử bao gồm hạt nhân nguyên tử (Proton và Notron) và vỏ nguyên tử (Electron).
+ Khối lượng của nguyên tử bằng khối lượng của hạt nhân nguyên tử.
2. Các hạt cấu tạo nên nguyên tử
a, Proton
Proton được cấu tạo nên từ những hạt khác có tên gọi là quark. Thường sẽ có ba quark trong mỗi proton – hai quark “lên” (up) và một quark “xuống” (down) và chúng được liên kết lại với nhau bởi những hạt khác nữa gọi là gluon.
Ví dụ: nguyên tử Cacbon có 6 proton, nguyên tử oxygen có 8 proton và nguyên tử hydrogen có 1 proton. Số lượng proton trong 1 nguyên tử được gọi là số nguyên tử của nguyên tố đó.
b, Notron
Neutron là hạt không mang điện tích và được tìm thấy trong hạt nhân của nguyên tử. Khối lượng của 1 notron thường lớn hơn khối lượng của 1 proton.
Tương tự như proton thì neutron cũng được cấu tạo từ quark – một quark “lên” và hai quark “xuống”. Neutron được khám phá ra bởi nhà Vật Lý người Anh – James Chadwick vào năm 1932.
c, Electron
Electron có điện tích âm sẽ bị hút điện về phía các proton tích điện dương. Các Electron bao xung quanh hạt nhân nguyên tử trong những lộ trình được gọi là orbital. Các orbital bên trong vây xung quanh nguyên tử có dạng hình cầu, còn những orbital bên ngoài thì phức tạp hơn.
Cấu hình electron của một nguyên tử là mô tả orbital đến vị trí của các electron trong một nguyên tử không bị kích thích. Do vậy nhờ vào việc sử dụng cấu hình electron và các nguyên lí vật lí thì các nhà hóa học có thể dự đoán các tính chất của một nguyên tử, ví dụ: độ ổn định, điểm sôi và độ dẫn.
3. Khối lượng nguyên tử là?
Khối lượng nguyên tử là do sự đóng góp của proton và neuton trong hạt nhân của nó. Tổng số những hạt này trong nguyên tử được gọi là số khối, số khối này chỉ đơn giản là một số tự nhiên và có đơn vị là nucleon.
Ví dụ: Số khối của cacbon – 12 nên nó sẽ có 12 nucleon (có 6 proton và 6 neuton)
Khối lượng thực tế của nguyên tử khi nó đứng yên thường được biểu diễn bằng đơn vị khối lượng của nguyên tử.
Đơn vị khối lượng nguyên tử hay dalton (ký hiệu SI: u hoặc Da), là một đơn vị đo khối lượng trong hóa học và vật lý, sử dụng đo khối lượng của các nguyên tử và phân tử. Nó được quy ước bằng một phần mười hai khối lượng của nguyên tử carbon đồng vị 12.
Nguyên tử có khối lượng vô cùng nhỏ bé, nếu tính bằng gram thì số trị vô cùng nhỏ, không tiện dụng. Thí dụ, khối lượng của một nguyên tử Cacbon (C) là: 0,000 000 000 000 000 000 000 019 926 g (= 1,9926.10−23 g)
Tại Việt Nam, người ta quy ước lấy 1/12 khối lượng của nguyên tử Cacbon làm đơn vị khối lượng cho nguyên tử, được gọi là Đơn vị Cacbon, viết tắt là đvC.
Trong Hệ Đo lường Quốc tế (SI), nó được ký hiệu bằng chữ "u". Theo quy ước trong hệ Đo lường Quốc tế:
1 u = 1/NA gam = 1/(1000 NA) kg
(Với NA là hằng số Avogadro)
1 u ≈ 1.66053886 x 10−27 kg
1 u ≈ 1.6605 x 10−24 g
----------------------------------------
Trên đây VnDoc đã giới thiệu tới các bạn nội dung bài Kí hiệu nguyên tử là gì? Cách viết kí hiệu nguyên tử? Để có kết quả học tập tốt và hiệu quả hơn, VnDoc xin giới thiệu tới các bạn học sinh tài liệu Giải bài tập Hóa học 10, Chuyên đề Vật Lý 10, Chuyên đề Hóa học 10, Giải bài tập Toán 10. Tài liệu học tập lớp 10 mà VnDoc tổng hợp biên soạn và đăng tải.

