Đề thi chọn học sinh giỏi lớp 12 môn Hóa học năm học 2019-2020 sở GD&ĐT Quảng Trị


Đề thi chọn học sinh giỏi môn Hóa học lớp 12 có đáp án
Đề thi chọn học sinh giỏi lớp 12 môn Hóa học năm học 2019-2020 sở GD&ĐT Quảng Trị có kèm theo đáp án là tài liệu tham khảo hỗ trợ các em ôn luyện và bồi dưỡng kiến thức môn Ngữ văn 12. Mời các bạn tham khảo
|
SỞ GIÁO DỤC VÀ ĐÀO TẠO QUẢNG TRỊ ĐỀ CHÍNH THỨC (Đề thi có 2 trang) |
KỲ THI CHỌN HỌC SINH GIỎI VĂN HÓA LỚP 12 THPT Khóa ngày 02 tháng 10 năm 2019 Môn thi: HÓA HỌC 12 Thời gian làm bài: 180 phút |
Câu 1. (4,0 điểm)
1. Nêu hiện tượng và viết các phương trình phản ứng xảy ra với mỗi trường hợp sau:
a) Cho dung dịch H2SO4 đặc vào saccarozơ sau đó đun nhẹ.
b) Cho dung dịch FeCl2 vào dung dịch AgNO3 dư.
c) Cho đạm Ure vào dung dịch nước vôi trong.
d) Cho từ từ dung dịch H2SO4 đến dư vào dung dịch NaAlO2.
2. Cho hỗn hợp rắn gồm FeS2, NaCl, NaBr và NaI phản ứng với dung dịch axit H2SO4 đặc, nóng, thu được hỗn hợp khí. Viết các phương trình phản ứng xảy ra.
3. Cho m gam Na vào 300 ml dung dịch hỗn hợp A gồm HCl 1M và AlCl3 0,5M. Viết các phương trình phản ứng và tính giá trị của m để khi kết thúc các phản ứng thu được 0,1 mol kết tủa.
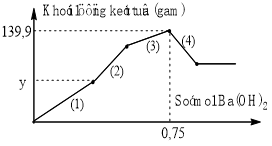
4. Hòa tan hoàn toàn Al bằng V ml dung dịch H2SO4 1M và HCl 1M, thu được dung dịch Y chứa Al2(SO4)3, AlCl3 và H2SO4 dư. Cho từ từ đến dư dung dịch Ba(OH)2 vào Y, thấy khối lượng kết tủa tạo thành phụ thuộc vào số mol Ba(OH)2 theo đồ thị hình bên. Dựa vào đồ thị, hãy viết các phản ứng ứng xảy ra ứng với mỗi đoạn và tìm giá trị của y.
Câu 2. (4,0 điểm)
1. Ở trạng thái cơ bản, nguyên tử của nguyên tố R có cấu hình electron lớp ngoài cùng là 4s1. Viết cấu hình electron, xác định vị trí trong bảng tuần hoàn và tính số electron độc thân của nguyên tử nguyên tố R ở trạng thái cơ bản.
2. Viết phương trình phản ứng dưới dạng ion thu gọn cho các thí nghiệm sau:
a) Hòa tan FeSx trong dung dịch HNO3 đặc, dư và đun nóng.
b) Cho dung dịch K2S dư vào dung dịch Fe2(SO4)3.
c) Cho dung dịch NH4HSO4 vào dung dịch Ba(HSO3)2.
d) Cho a mol kim loại Ba vào dung dịch chứa a mol NH4HCO3.
3. Cho hỗn hợp gồm a mol Mg và b mol Cu tác dụng với 200 ml dung dịch hỗn hợp AgNO3 0,3M và Cu(NO3)2 0,25 M. Sau phản ứng hoàn toàn thu được dung dịch A và chất rắn B. Cho A tác dụng với dung dịch NaOH dư, lọc lấy kết tủa nung trong không khí đến khối lượng không đổi thu được 3,6 gam hỗn hợp gồm 2 oxit. Hòa tan hoàn toàn B trong H2SO4 đặc, nóng được 0,09 mol khí SO2. Tính giá trị của a và b.
4. Hòa tan hoàn toàn 27,04 gam hỗn hợp X gồm Mg, Al, Al2O3 và Mg(NO3)2 vào dung dịch chứa hai chất tan NaNO3 và 1,08 mol H2SO4 (loãng). Sau khi kết thúc các phản ứng, thu được dung dịch Y chỉ chứa các muối và 0,28 mol hỗn hợp Z gồm N2O, H2. Tỷ khối của Z so với H2 bằng 10. Dung dịch Y tác dụng tối đa với dung dịch chứa 2,28 mol NaOH, thu được 27,84 gam kết tủa. Tính phần trăm khối lượng của nhôm kim loại có trong X.
Câu 3. (4,0 điểm)
1. Nêu hiện tượng xảy ra và viết phương trình phản ứng khi cho:
a) Dung dịch Na2CO3 vào dung dịch FeCl3.
b) Dòng khí H2S qua dung dịch FeCl3.
c) Dung dịch KI vào dung dịch FeCl3, khi phản ứng xong cho thêm vài giọt hồ tinh bột.
d) Từ từ dung dịch NaHSO4 vào dung dịch Na2CO3 theo tỉ lệ số mol 1:1 và đun nóng.
2. Sắp xếp các dung dịch: H2SO4, HCl, NaOH, Na2CO3 và Na2SO4 có cùng nồng độ 0,1M theo chiều tăng pH của dung dịch và giải thích bằng số liệu cụ thể thứ tự sắp xếp đó.
3. Hòa tan hoàn toàn m gam hỗn hợp X gồm Fe và kim loại M (hóa trị n không đổi) trong dung dịch H2SO4 đặc, nóng, dư, thu được dung dịch A và khí SO2 (sản phẩm khử duy nhất). Hấp thụ hết lượng SO2 bằng dung dịch chứa 0,1 mol NaOH (dư), thu được dung dịch chứa 5,725 gam chất tan. Thêm vào m gam X một lượng kim loại M gấp đôi lượng kim loại M có trong X, thu được hỗn hợp Y. Cho Y tan hết trong dung dịch HCl dư, thu được 0,0775 mol H2. Thêm vào m gam X một lượng Fe bằng lượng Fe có trong X, thu được hỗn hợp Z. Cho Z tác dụng với dung dịch H2SO4 loãng, dư, thu được dung dịch B chứa 5,605 gam muối. Viết các phương trình phản ứng và xác định M.
4. Hòa tan hoàn toàn 6,84 gam hỗn hợp E gồm Mg và kim loại M có hóa trị không đổi cần một lượng dung dịch HNO3 loãng, vừa đủ, thu được 0,896 lít (đktc) hỗn hợp khí X gồm N2 và N2O có tỉ khối so với H2 là 16 và dung dịch F. Chia F thành 2 phần bằng nhau.
Đem cô cạn phần 1, thu được 25,28 gam muối khan.
Phần 2 cho tác dụng với dung dịch NaOH dư, thu được 4,35 gam kết tủa. Viết các phương trình phản ứng và xác định kim loại M.
Câu 4. (4,0 điểm)
Xác định các chất A1, A2, A3, A4, A5, A6 là các hiđrocacbon khác nhau và viết các phương trình phản ứng theo sơ đồ chuyển hóa sau đây:
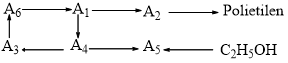
2. Các chất hữu cơ A, B, C, D có cùng công thức phân tử C4H6O4 đều phản ứng với dung dịch NaOH theo tỷ lệ mol 1:2. Trong đó: A, B đều tạo ra một muối, một rượu; C, D đều tạo ra một muối, một rượu và nước. Biết rằng khi đốt cháy muối do A, C tạo ra thì trong sản phẩm cháy không có nước. Xác định A, B, C, D và viết phương trình phản ứng với dung dịch NaOH.
3. Đốt cháy 26,7 gam chất hữu cơ F bằng không khí vừa đủ, sản phẩm cháy cho qua bình 1 đựng H2SO4 đặc, dư và bình 2 đựng nước vôi trong dư. Kết thúc các phản ứng, khối lượng bình 1 tăng thêm 18,9 gam, bình 2 xuất hiện 90 gam kết tủa, khí thoát ra khỏi bình 2 có thể tích 104,16 lít (đktc). Cho không khí có 20% thể tích là O2 và 80% thể tích là N2, F có công thức phân tử trùng với công thức đơn giản nhất. Xác định công thức phân tử của F.
4. Cho X và Y là hai axit cacboxylic đơn chức, mạch hở (có một nối đôi C=C); Z là ancol no, mạch hở; T là este ba chức tạo bởi X, Y và Z. Chia 40,38 gam hỗn hợp E gồm X, Y, Z, T thành 3 phần bằng nhau. Đốt cháy hoàn toàn phần 1, thu được 0,5 mol CO2 và 0,53 mol H2O. Phần 2 cho tác dụng với dung dịch brom dư, thấy có 0,05 mol Br2 phản ứng. Phần 3 cho tác dụng với lượng vừa đủ dung dịch hỗn hợp gồm KOH 1M và NaOH 3M, cô cạn, thu được m gam muối khan. Tìm giá trị của m.
Câu 5. (4,0 điểm)
1. Viết các phương trình phản ứng theo sơ đồ chuyển hóa sau:
![]()
Biết a mol C7H8O2 tác dụng vừa đủ với 2a mol Na, còn khi tác dụng với dung dịch NaOH thì cần a mol NaOH và các nhóm thế ở các vị trí liền kề.
2. Công thức đơn giản nhất của chất M là C3H4O3 và chất N là C2H3O3. Biết M là một axit no đa chức, N là một axit no chứa đồng thời nhóm chức –OH; M và N đều là mạch hở. Viết công thức cấu tạo có thể có của M và N.
3. Hỗn hợp P gồm hai anđehit đơn chức là đồng đẳng kế tiếp. Đem 10,4 gam P tác dụng hoàn toàn với dung dịch AgNO3 trong NH3 đun nóng, thu được 1 mol Ag. Nếu đem 10,4 gam P tác dụng hoàn toàn với H2 (xúc tác Ni, t0), thu được hỗn hợp X gồm hai ancol Y và Z (MY < MZ). Đun nóng X với H2SO4 đặc ở 1400C, thu được 4,52 gam hỗn hợp ba ete. Biết hiệu suất phản ứng tạo ete của Y bằng 50%. Viết các phương trình phản ứng và tính hiệu suất phản ứng tạo ete của Z.
4. Hỗn hợp X1 gồm 4 este mạch hở, trong đó có 1 este đơn chức và ba este hai chức là đồng phân của nhau. Đốt cháy hết 11,88 gam X1 cần 0,66 mol O2, thu được 0,57 mol CO2. Đun nóng 11,88 gam X1 với 310 ml dung dịch NaOH 1M, cô cạn dung dịch sau phản ứng, thu được m gam chất rắn Y1 và phần hơi chỉ chứa 1 ancol đơn chức Z1. Cho hết lượng Z1 tác dụng với Na dư thì khối lượng bình chứa Na tăng 5,85 gam. Trộn m gam Y1 với CaO rồi nung nóng (không có mặt oxi), thu được 2,016 lít khí (đktc) một hiđrocacbon duy nhất. Biết các phản ứng xảy ra hoàn toàn. Viết các phương trình phản ứng và công thức cấu tạo của các este trong hỗn hợp X1.
Cho: H=1; C=12; N=14; O=16; Na=23; Mg=24; Al=27; S=32; Cl=35,5; Ca=40; Fe=56; Cu=64; Ag=108; Ba=137.
------------Hết--------------
HƯỚNG DẪN CHẤM ĐỀ THI CHÍNH THỨC MÔN HÓA HỌC
KỲ THI CHỌN HỌC SINH GIỎI VĂN HÓA LỚP 12 THPT
Khóa ngày 02 tháng 10 năm 2019
Môn thi: HÓA HỌC
(Hướng dẫn chấm có 5 trang)
Câu 1.
Ý 1: 1điểm
a) C12H22O11 12C + 11H2O
C + 2H2SO4 đặc CO2 + 2SO2 + 2H2O
b) Xuất hiện kết tủa trắng và dung dịch chuyển sang màu vàng nâu
FeCl2 + 2AgNO3 → 2AgCl + Fe(NO3)2
Fe(NO3)2 + AgNO3 →Fe(NO3)3 + Ag
c) Có khí mùi khai thoát ra và xuất hiện kết tủa trắng
(NH2)2CO + 2H2O →(NH4)2CO3
Ca(OH)2 + (NH4)2CO3 →CaCO3 + 2NH3 + 2H2O
d) Xuất hiện kết tủa keo trắng sau đó kết tủa tan ra trong axit dư
H2SO4 + 2H2O + 2NaAlO2 →2Al(OH)3 + Na2SO4
3H2SO4 + 2Al(OH)3 →Al2(SO4)3 + 6H2O
Ý 2: 1 điểm
2FeS2 + 14H2SO4 đặc, nóng → Fe2(SO4)3 + 15SO2 + 14H2O
NaCl + H2SO4 đặc, nóng → NaHSO4 + HCl
2FeS2 + 14H2SO4 đặc, nóng → Fe2(SO4)3 + 15SO2 + 14H2O
NaCl + H2SO4 đặc, nóng → NaHSO4 + HCl
Ý 3: 1 điểm
Do có kết tủa nên Na đã tác dụng với H2O
Mặt khác: số mol kết tủa < số mol AlCl3 có 2 TH xảy ra
Cho Na vào nước thu được dung dịch A
Na + HCl → NaCl + 1/2 H2 (1)
Na + H2O → NaOH + 1/2H2 (2)
3NaOH + AlCl3 → Al(OH)3 + 3NaCl (3)
NaOH + Al(OH)3 → NaAlO2 + 2H2O (4)
TH1: AlCl3 dư, không có (4)
Ta có: nNa = nHCl + 3nAl(OH)3 = 0,6 mol m = 0,6.23 = 13,8 gam
TH2: Kết tủa bị hòa tan một phần, có (4)
Ta có: nNa = nHCl + 4nAlCl3 – nAl(OH)3 = 0,3 + 0,15.4 – 0,1 = 0,8 mol
m = 0,8.23 = 18,4 gam
.................. Hết ...................
Để tải và xem hướng dẫn giải chi tiết đề thi học sinh giỏi lớp 12 hóa học vui lòng ấn TẢI VỀ phía dưới
Đề thi tổng hợp các dạng bài tập tự luận bám sát những kiến thức các em đã được học và có phần nâng cao, giúp các em làm quen với các dạng đề thi học sinh giỏi. Các em có thể tự ôn luyện bài và đối chiếu kết quả với đáp án của đề. Để đạt kết quả cao các em có thể xem thêm Đề thi học sinh giỏi lớp 12 của các môn học khác.
VnDoc xin giới thiệu tới các em Đề thi chọn học sinh giỏi lớp 12 môn Hóa học năm học 2019-2020 sở GD&ĐT Quảng Trị. Hi vọng đây sẽ là tài liệu hữu ích hỗ trợ các em ôn luyện và đạt kết quả cao. Mời các em tham khảo thêm các tài liệu khác tại mục Tài liệu học tập lớp 12 do VnDoc tổng hợp và đăng tải như: Trắc nghiệm Tiếng Anh 12, Trắc nghiệm Hóa học 12, Trắc nghiệm Sinh học 12,...
Ngoài ra, VnDoc.com đã thành lập group chia sẻ tài liệu ôn tập THPT Quốc gia miễn phí trên Facebook: Quyết tâm đỗ Đại Học Mời các bạn học sinh tham gia nhóm, để có thể nhận được những tài liệu, đề thi mới nhất.
