Acid có tên gọi sulfurous acid
Sulfurous acid là tên gọi của acid nào sau đây?
Sulfurous acid là tên gọi của acid H2SO3.
Cùng nhau luyện tập, củng cố kiến thức Khoa học tự nhiên 8 qua bài kiểm tra giữa học kì 2 nha
Điểm khả dụng: 0 điểm
Bạn sẽ dùng 50 điểm để đổi lấy 1 lượt làm bài.
Bạn không đủ điểm để đổi.
Acid có tên gọi sulfurous acid
Sulfurous acid là tên gọi của acid nào sau đây?
Sulfurous acid là tên gọi của acid H2SO3.
Tác dụng của dòng điện khi chạy qua bóng đèn sợi đốt
Dòng điện chạy qua bóng đèn sợi đốt để làm cho đèn phát sáng, đồng thời dòng điện qua đèn này còn có tác dụng nào dưới đây?
Dòng điện chạy qua bóng đèn sợi đốt để làm cho đèn phát sáng, đồng thời dòng điện qua đèn này còn có tác dụng nhiệt.
Giải thích nguyên nhân
Tại sao trong các thí nghiệm về tĩnh điện, người ta phải treo các vật nhiễm điện bằng các sợi tơ mảnh và khô?
Trong các thí nghiệm về tĩnh điện, người ta phải treo các vật nhiễm điện bằng các sợi tơ mảnh và khô vì tơ là chất không cho điện tích truyền qua và rất nhẹ.
Dãy chất gồm các base không tan trong nước
Dãy chất nào sau đây chỉ gồm các base không tan trong nước?
Dãy chất chỉ gồm các base không tan trong nước là: Mg(OH)3, Fe(OH)2, Cu(OH)2.
Nguyên nhân trẻ bị viêm họng thường dễ dẫn đến viêm tai giữa
Vì sao trẻ bị viêm họng thường dễ dẫn đến viêm tai giữa?
Trẻ em bị viêm họng thường dễ bị viêm tai giữa là do vì vi sinh vật gây viêm họng có thể theo vòi nhĩ tới khoang tai giữa và gây viêm tại vị trí này.
Sự thay đổi thể tích lồng ngực khi hít vào và thở ra
Sự thay đổi thể tích lồng ngực khi hít vào thở ra đó là:
Các cử động hít vào và thở ra là sự phối hợp nhịp nhàng của cơ hoành, các xương sườn và xương liên sườn,… trong đó hít vào làm tăng thể tích lồng ngực để chứa nhiều khí và ngược lại thở ra làm giảm thể tích lồng ngực.
Bộ phận của mắt được xem như là một thấu kính hội tụ
Bộ phận nào sau đây của mắt được xem như là một thấu kính hội tụ?
Thuỷ tinh thể là bộ phận của mắt đóng vai trò như một thấu kính hội tụ.
Dung dịch thu được sau phản ứng
Cho 300 ml dung dịch NaOH 0,1 M vào 100 ml dung dịch H2SO4 0,1 M. Dung dịch thu được sau phản ứng
nNaOH = 0,3.0,1 = 0,03 (mol)
nH2SO4 = 0,1.0,1 = 0,01 (mol)
Phương trình phản ứng xảy ra:
2NaOH + H2SO4 → Na2SO4 + 2H2O
mol: 2 1
mol: 0,03 0,01
Ta có:
⇒ Sau phản ứng H2SO4 hết, NaOH dư.
Vậy dung dịch sau phản ứng làm quỳ tím hóa xanh.
Xác định sơ đồ mạch điện được mắc đúng
Sơ đồ mạch điện nào dưới đây được mắc đúng?
Chốt dương của ampe kế phải mắc với chốt dương của nguồn điện, chốt âm của ampe kế mắc với các thiết bị điện tới cực âm của nguồn điện.
Kí hiệu của điôt
Kí hiệu của điôt trong mạch điện là
Kí hiệu của điôt là ![]()
Phương trình hóa học xảy ra
Cho dung dịch HCl loãng vào một ống nghiệm chứa lá nhôm thấy có bọt khí thoát ra, lá nhôm bị tan dần, phương trình hóa học xảy ra là:
Phương trình hóa học xảy ra là:
2Al + 6HCl → 2AlCl3 + 3H2.
Bộ phận có vai trò chứa nước tiểu khi thải ra ngoài
Bộ phận có vai trò chứa nước tiểu khi thải ra ngoài là
Bộ phận có vai trò chứa nước tiểu khi thải ra ngoài là bóng đái (bàng quang).
Cách phòng chống bệnh bứu cổ
Cách phòng chống bệnh bứu cổ:
Việc bổ sung đầy đủ iodine trong khẩu phần ăn hằng ngày giúp cơ thể sản sinh đủ lượng thyroxine, nhờ đó giảm nguyn cơ mắc bệnh bứu cổ.
Sơ đồ mà vôn kế có chỉ số bằng 0
Vôn kế trong sơ đồ nào dưới đây có số chỉ bằng 0?
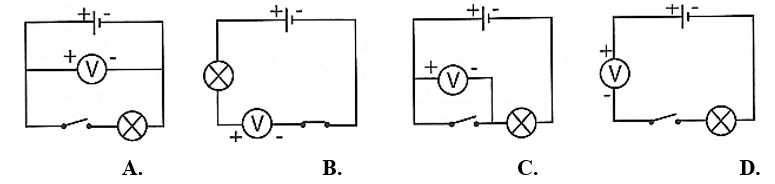
Vì công tắc K mở không có dòng điện chạy qua và vôn kế mắc nối tiếp nên không thể hiệu điện thế giữa hai cực để hở của nguồn điện.
Giải thích nguyên nhân
Trên các nóc nhà cao tầng người ta thường dựng một cây sắt nhỏ lên cao và nối với đất bằng một dây dẫn. Người ta làm như vậy để làm gì? Chọn kết quả đúng trong các kết quả sau:
Trên các nóc nhà cao tầng người ta thường dựng một cây sắt nhỏ lên cao và nối với đất bằng một dây dẫn. Phương pháp này sử dụng để chống sét cho các tòa nhà
Tìm phát biểu đúng
Phát biểu đúng là:
Môi trường acid có pH < 7
Môi trường kiềm có pH > 7.
Môi trường trung tính có pH = 7.
Tính nồng độ mol/l của acid HCl trong dung dịch ban đầu
Để trung hòa 10 ml dung dịch hỗn hợp acid gồm H2SO4 và HCl cần dùng 40 ml dung dịch NaOH 0,5 M. Mặt khác lấy 100 ml dung dịch acid đem trung hòa một lượng xút vừa đủ rồi cô cạn thì thu được 13,2 gam muối khan. Nồng độ mol/l của acid HCl trong dung dịch ban đầu là
Gọi nồng độ mol ban đầu của HCl và H2SO4 lần lượt là x và y (M).
Lần 1: 10 ml dung dịch hỗn hợp acid + NaOH: 0,02 (mol)
HCl + NaOH → NaCl + H2O
mol: 0,01x → 0,01x
H2SO4 + 2NaOH → Na2SO4 + 2H2O
mol: 0,01y → 0,02y
Ta có:
∑nNaOH = 0,01x + 0,02y = 0,02 (1)
Lần 2: 100 ml dung dịch hỗn hợp acid + NaOH vừa đủ → 13,2 g muối
⇒ mmuối = mNaCl + mNa2SO4
⇒ 0,1x.58,5 + 0,1y.142 = 13,2 (2)
Từ (1) và (2) ⇒ x = 0,8 và y = 0,6
Vậy nồng độ ban đầu của HCl = 0,8 M và H2SO4 = 0,6 M.
Vật mang điện tích khi dùng mảnh vải khô cọ xát
Dùng mảnh vải khô để cọ xát, thì có thể làm cho vật nào dưới đây mang điện tích?
Ống nhựa có khả năng bị nhiễm điện bằng cách cọ xát nó với mảnh vải khô.
Dung dịch nào có độ acid mạnh nhất trong các dung dịch
Dung dịch nào có độ acid mạnh nhất trong các dung dịch có giá trị pH sau?
Ta có: pH càng nhỏ thì độ acid của dung dịch càng lớn, pH càng lớn thì độ base của dung dịch cành lớn.
⇒ Dung dịch có pH = 2 có độ acid mạnh nhất.
Cơ thể có thể sống chỉ với một quả thận
Vì sao cơ thể có thể sống chỉ với một quả thận?
2 quả thận có cấu tạo giống nhau, một quả thận có khả năng lọc máu bài tiết cho cơ thể đủ để duy trì sự sống nhưng sẽ khiến thận phải hoạt động mệt mỏi.
Tính khối lượng hỗn hợp muối thu được sau phản ứng
Hoà tan 12,1 g hỗn hợp bột kim loại Zn và Fe cần 400 ml dung dịch HCl 1 M. Khối lượng hỗn hợp muối thu được sau phản ứng là
Gọi số mol của Zn và Fe lần lượt là x, y (mol).
Phương trình hóa học:
Zn + 2HCl → ZnCl2 + H2
mol: x → 2x → y
Fe + 2HCl → FeCl2 + H2
mol: y → 2y → y
Ta có hệ phương trình:
Khối lượng hỗn hợp muối thu được sau phản ứng là:
mmuối = mZnCl2 + mFeCl2 = 0,1.136 + 0,1.127 = 26,3 (gam)
Tính hiệu điện thế đo được
Dùng vôn kế có giới hạn đo là 6 V, trên mặt số được chia làm 30 khoảng nhỏ nhất. Dùng vôn kế để đo hiệu điện thế giữa hai đầu mạch điện kín thì thấy kim chỉ thị ở khoảng thứ 14. Hiệu điện thế đo được là:
Độ chia nhỏ nhất của Vôn kế đó là:
6 : 30 = 0,2 (V)
Hiệu điện thế đo được là:
14.0,2 = 2,8 (V)
Vậy khi kim chỉ thị ở khoảng thứ 14 thì hiệu điện thế đo được là 2,8 V.
Trường hợp dây may so của bếp sẽ đứt
Biết cường độ dòng điện định mức của một bếp điện là 4,5A. Cho các dòng điện có các cường độ sau đây chạy qua bếp, hỏi trường hợp nào dây may so của bếp sẽ đứt?
Nếu cường độ dòng điện định mức của một bếp điện là 4,5 A thì cho dòng điện 5,5 A chạy qua bếp dây may so của bếp sẽ đứt.
Chức năng chính của mũi
Chức năng chính của mũi là:
Chức năng chính của mũi: chứa và dẫn không khí, khi đi qua mũi, các dị vật sẽ được giữ lại, đồng thời không khí được sưởi ấm trước khi đi vào các cơ quan khác của đường dẫn khí.
Tính số phát biểu đúng
Cho các phát biểu sau:
(1) Để đảm bảo an toàn, tránh bị điện giật thì cần tránh cầm tay vào các bộ phận dẫn điện ở mạch điện, đi chân đất khi sửa chữa điện.
(2) Cơ thể người là vật cách điện nên dòng điện không đi qua được.
(3) Dòng điện đi qua dung dịch copper(II) sulfate có thể làm tách đồng từ dung dịch.
(4) Khi dòng điện chạy qua con muỗi bị mắc ở vợt muỗi gây ra tác dụng hóa học.
Số phát biểu đúng là
(1) Sai. Để đảm bảo an toàn, tránh bị điện giật thì cần tránh cầm tay vào các bộ phận dẫn điện ở mạch điện, đi giày hay dép cách điện khi sửa chữa điện.
(2) Sai. Cơ thể người là vật dẫn điện nên dòng điện đi qua được.
(3) Đúng.
(4) Sai. Khi dòng điện chạy qua con muỗi bị mắc ở vợt muỗi gây ra tác dụng sinh lí.
Tuyến là tuyến nội tiết
Tuyến nào sau đây là tuyến nội tiết?
Tuyến yên là một tuyến nội tiết.
Xác định kim loại Z
Cho 1,08 g kim loại Z vào dung dịch H2SO4 loãng dư. Lọc dung dịch, đem cô cạn thu được 6,84 g một muối khan duy nhất. Vậy kim loại Z là
Gọi kim loại R có hóa trị n (n = 1, 2, 3, 4).
2R + nH2SO4 → R2(SO4)n + nH2
;
Theo phản ứng:
nR = 2nR2(SO4)n
⇒ R = 9n
Biện luận ta có:
| n | 1 | 2 | 3 | 4 |
| M | 9 (loại) | 18 (loại) | 27 (Al) | 36 (loại) |
Vậy R là kim loại Al.
Trường hợp làm quỳ tím hóa đỏ
Lần lượt nhỏ lên bốn mẩu giấy quỳ tím mỗi dung dịch sau:(1) nước đường, (2) nước chanh, (3) nước muối (dung dịch NaCl) và (4) dung dịch nước vôi trong (Ca(OH)2). Trường hợp nào quỳ tím sẽ chuyển sang màu đỏ?
Trường hợp (2) nước chanh sẽ làm quỳ tím chuyển sang màu đỏ do nước chanh chứa nhiều acid citric.
Vì sao không nên lạm dụng đồ trang điểm
Không nên lạm dụng đồ trang điểm vì:
Không nên lạm dụng đồ trang điểm vì đồ trang điểm làm bít tắc lỗ chân lông trên → da xuất hiện mụn.
Nhận định không đúng về thân nhiệt
Nhận định nào dưới đây không đúng về thân nhiệt?
Ở người bình thường, nhiệt độ cơ thể trung bình khoảng 36,5oC – 37oC.
Theo Nghị định 147/2024/ND-CP, bạn cần xác thực tài khoản trước khi sử dụng tính năng này. Chúng tôi sẽ gửi mã xác thực qua SMS hoặc Zalo tới số điện thoại mà bạn nhập dưới đây: