Bộ đề thi thử THPT Quốc gia năm 2016 môn Hóa học - Số 5
Bộ đề thi thử THPT Quốc gia môn Hóa học năm 2016
Bộ đề thi thử THPT Quốc gia 2016 môn Hóa học - Số 5 gồm nhiều đề thi thử THPT Quốc gia môn Hóa có đáp án đi kèm. Đây là tài liệu ôn tập môn Hóa hữu ích, giúp các bạn luyện thi THPT Quốc gia, ôn thi Đại học, Cao đẳng khối A, khối B hiệu quả. Mời các bạn tham khảo.
39 đề thi thử THPT Quốc gia 2016 môn Hóa học có đáp án
Đề cương ôn thi THPT Quốc gia năm 2016 môn Hóa học

Chi tiết: Đề thi thử Quốc gia môn Hóa học trường THPT Đô Lương 1, Nghệ An
|
SỞ GD & ĐT NGHỆ AN TRƯỜNG THPT ĐÔ LƯƠNG 1
|
ĐỀ THI KHẢO SÁT CHẤT LƯỢNG KHỐI 12 LẦN 2 Môn thi: Hoá học Thời gian làm bài: 90 phút; (50 câu trắc nghiệm) |
|
|
|
Mã đề thi 246 |
|
Họ, tên thí sinh:.........................................................Số báo danh: .................
Cho biết nguyên tử khối của các nguyên tố :
H = 1; C = 12; N = 14; O = 16; Na = 23; Mg = 24; Al = 27; S = 32; Cl = 35,5; K = 39; Ca = 40; Pb = 207, Fe = 56; Cu = 64; Zn = 65; Ag=108; Ba = 137.
Câu 1: X là một amin đơn chức bậc một chứa 23,73% nitơ về khối lượng. Hãy chọn công thức phân tử đúng của X:
A. C3H7NH 2. B. C4H7NH 2. C. C3H5NH 2. D. C5H9NH 2.
Câu 2: Có các nhận định sau:
- Phenol làm quỳ tím chuyển thành màu đỏ.
- Ancol etylic tác dụng được với NaOH.
- Axetandehit có công thức là CH3CHO.
- Từ 1 phản ứng có thể chuyển ancol etylic thành axit axetic.
- Từ CO có thể điều chế được axit axetic.
Số nhận định không đúng là
A. 5. B. 3. C. 2. D. 4.
Câu 3: Nhúng thanh Mg vào dung dịch chứa 0,1 mol muối sunfat trung hoà của một kim loại M, sau phản ứng hoàn toàn lấy thanh Mg ra thấy khối lượng thanh Mg tăng 4,0 gam. Số muối của kim loại M thoả mãn là
A. 1. B. 0. C. 3. D. 2.
Câu 4: Cho hợp chất X có công thức phân tử là C4H8. Số đồng phân cấu tạo làm mất màu dung dịch Brom ứng với X là
A. 4. B. 3. C. 5. D. 6.
Câu 5: Trước đây người ta thường trộn vào xăng chất Pb(C2H5)4. Khi đốt cháy xăng trong các động cơ, chất này thải vào không khí PbO, đó là một chất rất độc. Hằng năm người ta đã dùng hết 227,25 tấn Pb(C2H5)4 để pha vào xăng (nay người ta không dùng nữa). Khối lượng PbO đã thải vào khí quyển gần với giá trị nào sau đây nhất ?
A. 185 tấn. B. 155 tấn. C. 145 tấn. D. 165 tấn.
Câu 6: Hỗn hợp X gồm tripeptit A và tetrapeptit B đều được cấu tạo bởi glyxin và alanin. % khối lượng nitơ trong A và B theo thứ tự là 19,36% và 19,44%. Thủy phân hoàn 0,1 mol hỗn hợp X bằng một lượng dung dịch NaOH vừa đủ, thu được dd Y. Cô cạn dung dịch Y thu được 36,34 gam hỗn hợp muối. Tỉ lệ mol giữa A và B trong hỗn hợp X là
A. 7:3. B. 2:3. C. 3:2. D. 3:7.
Câu 7: Cho 3 thí nghiệm sau:
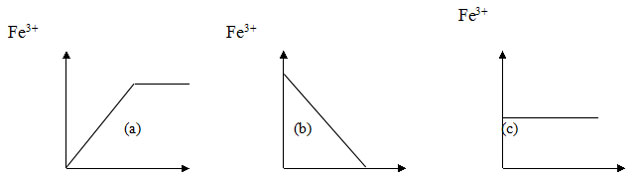
(1) Cho từ từ dung dịch AgNO3 đến dư vào dung dịch Fe(NO3)2
(2) Cho từ từ AgNO3 vào dd FeCl3
(3) Cho bột sắt từ từ đến dư vào dd FeCl3
Thí nghiệm nào ứng với sơ đồ sau:
A. 1-b, 2-a, 3-c B. 1-a, 2-b, 3-c C. 1-c, 2-b, 3-a D. 1-a, 2-c, 3-b
Câu 8: Trong số các dung dịch sau: (1) glucozơ, (2) 3-clopropan-1,2-điol, (3) etilenglicol, (4) tripeptit, (5) axit axetic, (6) propan-1,3-điol. Số dung dịch hoà tan được Cu(OH)2 là
A. 6. B. 4. C. 3. D. 5.
Câu 9: Vật làm bằng hợp kim Zn-Fe trong môi trường không khí ẩm (hơi nước có hoà tan O2) đã xảy ra quá trình ăn mòn điện hoá. Tại anot xảy ra quá trình:
A. Khử Zn. B. Khử O2. C. Ôxi hoá Zn. D. Ôxi hoá Fe.
Câu 10: Cho dãy các chất: CH3COOCH2CH2Cl, ClH3N-CH2COOH, C6H5Cl (thơm),HCOOC6H5 (thơm), C6H5COOCH3 (thơm), HO-C6H4-CH2OH (thơm), CH3COOCH=CH2. Có bao nhiêu chất khi tác dụng với dung dịch NaOH đặc, nhiệt độ cao, áp suất cao có thể cho sản phẩm chứa hai muối?
A. 5. B. 3. C. 2. D. 4.
(Còn tiếp)
Chi tiết: Đề thi thử THPT Quốc gia môn Hóa học trường THPT Thị xã Quảng Trị, Quảng Trị
|
TRƯỜNG THPT THỊ XÃ QUẢNG TRỊ
|
ĐỀ THI THỬ THPT QUỐC GIA LẦN I MÔN HÓA HỌC (Thời gian làm bài 90 phút, không kể thời gian giao đề) |
|
|
|
Mã đề thi 132 |
|
Họ, tên thí sinh:..........................................................................
Số báo danh:...............................................................................
Cho biết nguyên tử khối của H = 1; C = 12; N = 14; O = 16; Na = 23; Mg = 24; Al = 27; S = 32; Cl = 35,5; K = 39; Ca = 40; Fe = 56; Cu = 64; Ag = 108 và Ba = 137.
Câu 1: Có các phát biểu sau:
(a) Tất cả các phản ứng của N2 với kim loại đều cần phải đun nóng.
(b) Nitơ lỏng được dùng để bảo quản máu và các mẫu vật sinh học.
(c) Trong y khoa, ozon được dùng chữa sâu răng.
(d) Chất dùng bó bột khi gãy xương là thạch cao sống (CaSO4.2H2O)
(e) Axit clohidric dùng để khắc chữ lên thủy tinh.
Trong các phát biểu trên, số phát biểu đúng là
A. 3. B. 5. C. 2. D. 4.
Câu 2: Anion X- và cation Y2+ đều có cấu hình electron lớp ngoài cùng là 3s23p6. Vị trí của các nguyên tố trong BTH là:
A. X có STT 18, chu kỳ 3, nhóm VIA; Y có STT 20, chu kỳ 4, nhóm IIA.
B. X có STT 17, chu kỳ 4, nhóm VIIA; Y có STT 20, chu kỳ 4, nhóm IIA.
C. X có STT 17, chu kỳ 3, nhóm VIIA; Y có STT 20, chu kỳ 4, nhóm IIA.
D. X có STT 18, chu kỳ 3, nhóm VIIA;Y có STT 20, chu kỳ 3, nhóm IIA.
Câu 3: Nung hỗn hợp gồm 3,24 gam Al và 9,28 gam Fe3O4 trong môi trường không có không khí sau một thời gian, thu được hỗn hợp rắn X. Hòa tan hoàn toàn X trong dung dịch HCl dư thu được 3,36 lít (đktc) khí H2 và m gam muối. Giá trị của m là
A. 33,39. B. 34,10. C. 32,58. D. 31,97.
Câu 4: Thuỷ phân este Z trong môi trường axit thu được hai chất hữu cơ X và Y (MX < MY). Bằng một phản ứng có thể chuyển hoá X thành Y. Chất Z không thể là
A. etyl axetat. B. metyl axetat. C. metyl propionat. D. vinyl axetat.
Câu 5: Tiến hành các thí nghiệm sau
(a) Cho dung dịch NH3 dư vào dung dịch AlCl3
(b) Sục khí SO2 vào dung dịch H2S
(c) Cho dung dịch AgNO3 vào dung dịch Fe(NO3)2
(d) Cho dung dịch AgNO3 vào dung dịch HCl
(e) Cho dung dịch AgNO3 vào dung dịch HF
Sau khi kết thúc thí nghiệm, số trường hợp thu được kết tủa là
A. 2. B. 5. C. 3. D. 4.
Câu 6: Cho X, Y, Z, T là các chất khác nhau trong số 4 chất: HCOOH; CH3COOH; HCl; C6H5OH (phenol) và pH của các dung dịch trên được ghi trong bảng sau:
|
Chất |
X |
Y |
Z |
T |
|
pH (dung dịch nồng độ 0,01M ở 250C) |
6,48 |
3,22 |
2,00 |
3,45 |
Nhận xét nào sau đây đúng?
A. T có khả năng phản ứng tráng bạc. B. X được điều chế trực tiếp từ ancol etylic.
C. Y tạo kết tủa trắng với nước brom. D. Z tạo kết tủa trắng với dung dịch AgNO3.
Câu 7: Điện phân dung dịch có chứa 0,1 mol CuSO4 và 0,2 mol FeSO4 với điện cực trơ, bình điện phân không có màng ngăn. Sau một thời gian thu được 2,24 lít (đktc) khí ở anot thì dừng lại, để yên bình điện phân đến khi khối lượng catot không còn thay đổi. Khối lượng kim loại thu được ở catot là
A. 6,4 gam. B. 12 gam. C. 17,6 gam. D. 7,86 gam.
Câu 8: Cho 400 ml dung dịch E gồm AlCl3 x mol/lít và Al2(SO4)3 y mol/lít tác dụng với 612 ml dung dịch NaOH 1M, sau khi các phản ứng kết thúc thu được 8,424 gam kết tủa. Mặt khác, khi cho 400 ml E tác dụng với dung dịch BaCl2 (dư) thì thu được 33,552 gam kết tủa. Tỉ lệ x : y là
A. 4 : 3 B. 3 : 4 C. 7 : 4 D. 3 : 2
Câu 9: Nhiệt phân 5,8 gam FeCO3 trong không khí một thời gian được 4,36 gam hỗn hợp rắn X. Hòa tan hết X trong dung dịch HCl vừa đủ được dung dịch Y . Cho dung dịch AgNO3 dư vào dung dịch Y thì sau khi phản ứng xong thu được m gam kết tủa. Giá trị m là
A. 12,72. B. 21,17. C. 21,68. D. 34,82.
Câu 10: Khi cho ankan X (trong phân tử có phần trăm khối lượng hiđro bằng 16,28%) tác dụng với clo theo tỉ lệ số mol 1:1 (trong điều kiện chiếu sáng) chỉ thu được 2 dẫn xuất monoclo đồng phân của nhau. Tên của X là
A. butan. B. 2,3-đimetylbutan. C. 3-metylpentan. D. 2-metylpropan.
(Còn tiếp)
Chi tiết: Đề thi thử THPT Quốc gia môn Hóa học trường THPT Phước Vĩnh, Bình Dương
| Trường THPT Phước Vĩnh | ĐỀ THI THỬ TNTHPT |
(Cho biết nguyên tử khối của các nguyên tố: H = 1; C = 12; N = 14; O = 16; Na = 23; Mg = 24; Al = 27; P = 31; S = 32; Cl = 35,5; K = 39; Ca = 40; Fe = 56; Cu = 64; Br = 80; Ag = 108; Ba = 137; Be=9; Sr= 88)
Câu 1: Glucozơ và fructozơ đều
A. có phản ứng thủy phân. B. có nhóm –CH=O trong phân tử.
C. có công thức phân tử C12H12O11. D. thuộc loại monosaccarit.
Câu 2: X và Y là hai nguyên tố thuộc cùng một phân nhóm chính và hai chu kỳ liên tiếp. Số proton của nguyên tử Y nhiều hơn số proton của nguyên tử X. Tổng số hạt proton trong nguyên tử X và Y là 32. Nhận xét nào sau đây là đúng?
A. Đều là kim loại kiềm thổ.
B. Lớp ngoài cùng của nguyên tử Y (ở trạng thái cơ bản) có 1 electron.
C. Phân lớp ngoài cùng của nguyên tử X (ở trạng thái cơ bản) có 3 electron.
D. Là kim loại kiềm.
Câu 3: Một dung dịch X gồm 0,02 mol Na+; 0,01 mol Ca2+; 0,02 mol HCO3- và a mol ion X (bỏ qua sự điện li của nước). Ion X và giá trị của a là
A. OH- và 0,02 B. Cl- và 0,02 C. NO3- và 0,01 D. CO32- và 0,01
Câu 4: Từ dung dịch Na2CO3 ta có thể điều chế Na bằng cách
A. Cô cạn dung dịch rồi điện phân Na2CO3 nóng chảy.
B. Chuyển dung dịch Na2CO3 thành dung dịch NaCl, cô cạn rồi điện phân nóng chảy NaCl
C. Chuyển dung dịch Na2CO3 thành dung dịch NaCl, rồi điện phân dung dịch NaCl
D. Điện phân dung dịch Na2CO3.
Câu 5: Cho sơ đồ chuyển hóa
![]()
Các chất Y và T lần lượt là
A. Fe và NaNO3 B. Fe2O3 và Cu(NO3)2 C. Fe và AgNO 3 D. Fe2O3 và AgNO3
Câu 6: Thủy phân hoàn toàn m1 gam 1 este X mạch hở bằng dung dịch NaOH dư, thu được m2 gam ancol Y (không có khả năng phản ứng với Cu(OH)2) và 15 gam hỗn hợp muối của hai axit cacboxylic đơn chức Z và T (MZ < MT). Đốt cháy hoàn toàn m2 gam Y bằng oxi dư, thu được 0,3 mol CO2 và 0,4 mol H2O. Tên gọi của axit Z là
A. axit metacrylic. B. axit axetic. C. axit acrylic. D. axit fomic.
Câu 7: Thủy phân este X mạch hở có công thức phân tử C4H6O2, sản phẩm thu được có khả năng tráng bạc. Số este X thỏa mãn tính chất trên là
A. 3 B. 5 C. 6 D. 4
Câu 8: Ứng dụng nào sau đây không phải của ozon?
A. Tẩy trắng các loại tinh bột, dầu ăn.
B. Chữa sâu răng, bảo quản hoa quả.
C. Điều chế oxi trong phòng thí nghiệm.
D. Khử trùng nước uống, khử mùi.
Câu 9: Kim loại nào sau đây không tan hết trong nước dư ở nhiệt độ thường
A. Al B. Na C. Ba D. K
Câu 10: Số đồng phân este ứng với công thức phân tử C4H8O2 là
A. 6. B. 4. C. 5. D. 7.
(Còn tiếp)
Chi tiết: Đề thi thử THPT Quốc gia môn Hóa học trường THPT Nguyễn Trãi, Thái Bình
|
SỞ GD & ĐT THÁI BÌNH TRƯỜNG THPT NGUYỄN TRÃI
|
ĐỀ THI THỬ THPTQUỐC GIA Môn: HOÁ HỌC Thời gian: 90 phút (Không kể thời gian giao đề) |
Cho biết khối lượng nguyên tử (theo đvC) của các nguyên tố:
H=1; C=12; N=14; O=16; F=19; Na=23; Mg=24; Al=27; P=31; S=32; Cl=35,5; K=39; Ca=40; Cr=52; Mn=55; Fe=56; Cu=64; Zn=65; Br=80; Ag=108; I=127; Ba=137.
Thí sinh không được sử dụng bảng hệ thống tuần hoàn các nguyên tố hóa học
Mức 1 (25 câu):
Câu 1: Một mẫu nước cứng có chứa các ion: Ca2+, Mg2+, HCO3-, Cl-, SO42-. Chất làm mềm mẫu nước cứng trên là
A. HCl. B. NaHCO3. C. Na3PO4. D. BaCl2.
Câu 2: Chất nào sau đây chứa cả 3 loại liên kết (ion, cộng hoá trị, cho - nhận)?
A. K2CO3. B. NaHCO3. C. NaNO3. D. HNO3.
Câu 3: Cho 200 gam dung dịch chứa glucozơ tác dụng với dung dịch AgNO3/NH3 dư, khối lượng Ag sinh ra cho vào dung dịch HNO3 đậm đặc dư thấy sinh ra 0,2 mol khí NO2. Vậy nồng độ % của glucozơ trong dung dịch ban đầu là
A. 18 % . B. 9 %. C. 27% D. 36%
Câu 4 : Khối lượng tripeptit được tạo thành từ 178 gam alanin và 75 gam glyxin là:
A. 253 g B. 235 g C. 217 g D. 199 g.
Câu 5: Phản ứng nào sau đây không thuộc phản ứng tự oxi hoá, tự khử?
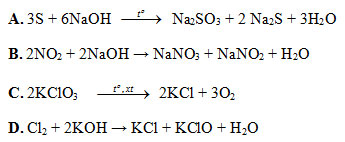
Câu 6: Phát biểu nào sau đây đúng?
A. Thủy phân hoàn toàn protein đơn giản thu được các α-amino axit.
B. Lòng trắng trứng gặp HNO3 tạo thành hợp chất có màu tím.
C. Tất cả các peptit đều có phản ứng màu biure với Cu(OH)2.
D. Tất cả các protein đều tan trong nước tạo thành dung dịch keo.
Câu 7: Cho các cân bằng sau
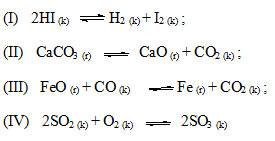
Khi giảm áp suất của hệ, số cân bằng bị chuyển dịch theo chiều nghịch là
A. 3 B. 1 C. 2 D. 4
Câu 8: Cho dung dịch Ba(HCO3)2 lần lượt vào các dung dịch: CaCl2, Ca(NO3)2, NaOH, Na2CO3, KHSO4, Na2SO4, Ca(OH)2, H2SO4, HCl. Số trường hợp có tạo ra kết tủa là
A. 6. B. 7. C. 4. D. 5.
Câu 9: Có thể dùng NaOH( ở thể rắn) để làm khô các chất khí sau:
A. N2, Cl2, O2, CO2, H2 B. NO2, N2, CO2, CH4, H2
C. NH3, O2, N2, CH4, H2 D. NH3, SO2, CO, Cl2
Câu 10: Trong các tiểu phân sau: 24Cr2+, 26Fe2+, 25Mn2+, 29Cu2+. Tiểu phân có số electron độc thân lớn nhất là
A. Fe2+ B. Cr2+ C. Cu2+ D. Mn2+
(Còn tiếp)
Chi tiết: Đề thi thử THPT Quốc gia môn Hóa học trường THPT Phan Đăng Lưu, Tp Hồ Chí Minh
|
SỞ GIÁO DỤC VÀ ĐÀO TẠO THÀNH PHỐ HỒ CHÍ MINH TRƯỜNG THPT PHAN ĐĂNG LƯU ĐỀ CHÍNH THỨC |
KÌ THI THỬ TNPT MÔN: HÓA HỌC KHỐI LỚP: 12 Thời gian làm bài: 60 phút (không kể thời gian phát đề) (40 câu trắc nghiệm – 5 trang) |
Mã đề 132
Cho nguyên tử khối: Na = 23; Mg = 24; Al = 27; K = 39; Ca = 40; Ba = 137; Fe = 56; Cr = 52; Ag = 108; Zn = 65; Cu = 64; Ni = 59; Sn = 119; I = 127; Cl = 35,5; S = 32; O = 16; N = 14; C = 12; H = 1.
Câu 1: Trong thực tế người ta thường dùng những kim loại nào sau đây để làm dây dẫn điện?
A. Zn và Fe B. Ag và Au C. Al và Cu D. Ag và Cu
Câu 2: Số hiệu nguyên tử đặc trưng cho một nguyên tố hóa học vì nó:
A. là kí hiệu của một nguyên tố hóa học.
B. cho biết tính chất của một nguyên tố hóa học.
C. là điện tích hạt nhân của một nguyên tố hóa học.
D. là tổng số proton và nơtron trong nhân.
Câu 3: Cho 5,4 gam Al tác dụng hết với khí Cl2 (dư), thu được m gam muối. Giá trị của m là
A. 26,7. B. 25,0. C. 12,5. D. 19,6.
Câu 4: Có bao nhiêu tripeptit (mạch hở) sau khi thủy phân hoàn toàn đều thu được sản phẩm gồm có alanin và glyxin?
A. 6 B. 7 C. 8 D. 5
Câu 5: Khi hòa tan hoàn toàn m gam mỗi kim loại vào nước dư, từ kim loại nào sau đây thu được thể tích khí H2 (cùng điều kiện nhiệt độ và áp suất) là nhỏ nhất?
A. Ca B. K C. Li D. Na
Câu 6: Người ta tổng hợp poli(metyl metacrylat) từ axit và ancol tương ứng qua 2 giai đoạn là este hóa (H=60%) và trùng hợp (H=80%). Khối lượng axit và ancol cần dùng để thu được 1,2 tấn polime là bao nhiêu.
A. 86 tấn và 32 tấn. B. 2,15 tấn và 0,8 tấn.
C. 68 tấn và 23 tấn. D. 21,5 tấn và 8 tấn.
Câu 7: Trường hợp nào sau đây không xảy ra sự ăn mòn điện hoá?
A. Sự gỉ của gang trong không khí ẩm.
B. Sự ăn mòn vỏ tàu trong nước biển.
C. Nhúng thanh Zn trong dung dịch H2SO4 có nhỏ vài giọt CuSO4.
D. Nhúng thanh Cu trong dung dịch Fe2(SO4)3 có nhỏ vài giọt dung dịch H2SO4.
Câu 8: Trong dung dịch, NH3 là một bazơ yếu vì:
A. Khi tan trong H2O, chỉ một phần nhỏ các phân tử NH3 kết hợp với ion H+ của H2O tạo ra các ion NH4+ và OH-.
B. Phân tử NH3 là phân tử có cực.
C. Amoniac tan nhiều trong H2O.
D. Khi tan trong H2O, NH3 kết hợp với H2O tạo ra các ion NH4+ và OH-
Câu 9: Hỗn hợp X gồm Fe2(SO4)3, FeSO4 và Al2(SO4)3. Thành phần phần trăm về khối lượng của oxi trong X là 49,4845%. Cho 97 gam X tác dụng với dung dịch NH3 dư thu được kết tủa có khối lượng là
A. 31,375 gam. B. 50,5 gam. C. 76 gam. D. 37,75 gam.
Câu 10: Cho 4 chất sau: 1/ Ancol etylic. 2/ Phenol. 3/ Benzen. 4/ Axit axetic.
Độ linh động của nguyên tử hiđro trong phân tử các chất trên được sắp xếp theo thứ tự giảm dần nào sau đây?
A. 3 > 1 > 2 > 4. B. 4 > 2 > 1 > 3. C. 3 > 2 > 1 > 4. D. 4 > 1 > 2 > 3.
(Còn tiếp)