Amino axit là gì? - Đầy đủ kiến thức từ A-Z để ôn thi THPT QG 2020
VnDoc xin giới thiệu tới bạn đọc Amino axit là gì? - Đầy đủ kiến thức từ A-Z để ôn thi THPT QG 2020. Chắc chắn tài liệu sẽ giúp các bạn học tốt môn Hóa học 12 hiệu quả nhất. Mời các bạn tham khảo.
Amino axit là gì? - Đầy đủ kiến thức từ A-Z để ôn thi THPT QG 2020
Amino axit là gì?
Amino axit là một loại hợp chất hữu cơ tạp chức. Bên trong phân tử có chứa đồng thời – NH2 nhóm amino và -COOH nhóm cacbonxyl.
Ví dụ: NH2– C2H4– COOH
Công thức tổng quát của amino axit là: R(NH2)x(COOH)y hoặc CnH2n+2-2k-x-y(NH2)x(COOH)y
Tên thay thế của amino axit là gì?
Chúng ta sẽ sử dụng công thức sau để đọc đúng tên thay thế của một amino axit.
| Axit + Số chỉ vị trí nhóm –NH2 + amino + tên hidrocacbon no tương ứng ở mạch chính + oic |
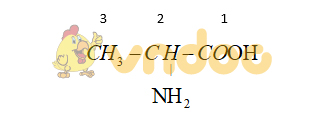
Axit 2-aminopropanoic
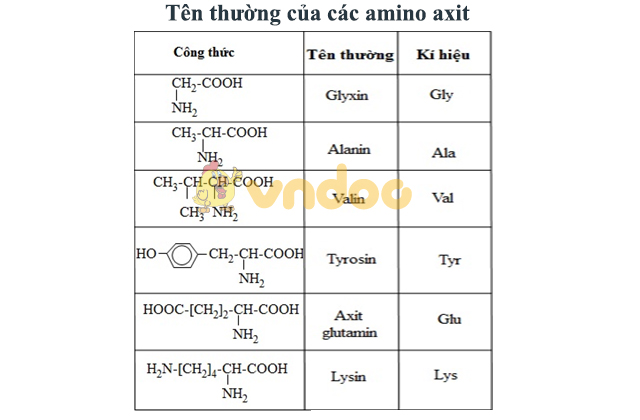
Tên thường của amino axit
Sau đây là một số tên thường của các amino axit cần nhớ.
Cấu tạo phân tử của amino axit
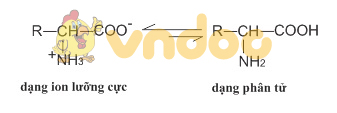
Amino axit là những hợp chất có cấu tạo inon lưỡng cực nên ở điều kiện thường chúng là chất rắn kết tinh, tương đối dễ tan trong nước và có nhiệt độ nóng chảy cao.
Đồng phân của amino axit
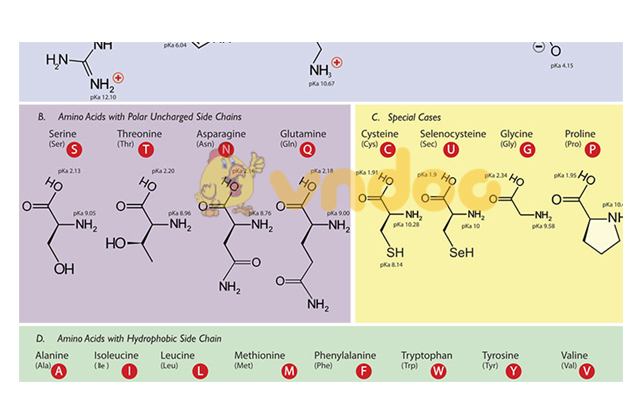
Để viết được đồng phân của một amino axit ta sẽ viết đồng phân của axit tương ứng trước. Sau đó đặt nhóm amino -NH2 vào mạch.
Ví dụ: Viết đồng phân của amino axit C4H9O2N.
Cách viết: Tính độ bất bão hòa k = (2.4 +2-9+1) : 2 = 1.
⇒ Amino axit chứa toàn liên kết đơn trừ liên kết đôi trong nhóm -COOH.
Các đồng phân viết như sau:

Ở đâu có dấu ↓ thì em hãy đặt nhóm -NH2. Như vậy, C4H9O2N có 5 đồng phân.
Tính chất hóa học của amino axit
Amino axit phân li trong dung dịch
H2N-CH2-COOH ↔ H3N+-CH2-COO–
Amino axit có tính lưỡng tính
Có thể tác dụng được với cả dung dịch axit và bazơ.
Khi tác dụng với axit mạnh sẽ tạo muối:
NH2-CH2-COOH + HCl → ClNH3 – CH2 – COOH
Tác dụng với bazơ mạnh tạo muối và nước.
NH2-CH2-COOH + KOH → NH2-CH2-COOK + H2O
Amino axit tham gia phản ứng trùng ngưng theo phương trình:
nNH2-CH2-COOH → (- NH-CH2-CO-)n + nH2O (H+)
Khi trùng ngư 6-aminohexanoic hay 7-aminoheptanoic có xúc tác ta được polime thuộc loại poliamit.
Từ n aminoaxit khác nhau ta có thể tạo ra n! polipeptit có chưa n gốc amino axit khác nhau; nn polipeptit có chứa n gốc amino axit.
Amino axit phản ứng với HNO2
HOOC-R-NH2 + HNO2 → HOOC-R-OH + N2 + H2O
Phản ứng este hóa của amino axit là gì?
NH2-CH2-COOH + ROH → NH2-CH2-COOR + H2O (khí HCl). Trong phản ứng este hóa, các em cần nhớ đây là phản ứng riêng của gốc – COOH.
Bên cạnh đó một câu hỏi đặt ra là aminoaxit có làm đổi màu quỳ tím hay không?
Thực tế để biết được một amino axit có làm đổi màu quỳ tím hay không cần dựa vào quan hệ giữa gốc – COOH và NH2.
R(NH2)x(COOH)y. Nếu x = y thì qùy tím không đổi màu.
Nếu x < y thì quỳ tím chuyển sang màu đỏ.
Khi x > y thì quỳ tím chuyển sang màu xanh.
Trong phản ứng của amino axit với dd axit và bazơ nếu sau phản ứng axit hay bazơ còn dư thì muối được tạo thành sẽ tiếp tục phảng ứng với dd axit hoặc kiềm.
Tất tần tật các dạng bài tập amino axit trọng tâm
Dạng 1: Lý thuyết trọng tâm
Trong đề thi THPT QG sẽ có những câu hỏi kiểm tra lý thuyết. Để trả lời được, em cần nắm thật chắc lý thuyết cơ bản. Vận dụng chúng giải bài tập nhanh chóng.
Ví dụ: Amino axit X có phân tử khối là 117g/mol. Tên của X là:
A. Alanin
B. Glyxin
C. Valin
D. Lysin
Đáp án C. Valin
Muốn chọn được đáp án đúng em phải nhớ được công thức cấu tạo hoặc khối lượng mol của các chất trên.
Dạng 2: Phản ứng đốt cháy
Phương pháp giải bái toán đốt cháy amino axit là gì? Hãy dựa vào phương trình phản ứng tổng quát và một số công thức tính nhanh sau:
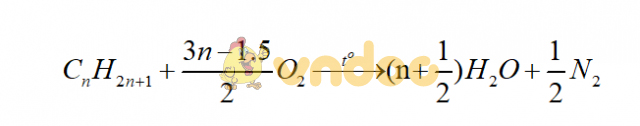
Công thức tính nhanh:
nH2O – n CO2 = 0.5naminoaxit
Định luật bảo toàn nguyên tố:
BTNT O:
1/ Số nO (amino axit) = 2namino axit
2/ Số Số nO (amino axit) + 2n Opư= 2nCO2 + nH2O
BTNT N:
namino axit = 2nN2 (sinh ra)
Định luật bảo toàn khối lượng
m amino axit = mC + mH + mO + mN
m amino axit + mO2 pư = mCO2 + mH2O + mN2
Dạng 3: Tính axit bazơ
Khi giải các dạng bài tập về tính axit bazơ các em cần ghi nhớ một số ý quan trọng sau:
Lys là quỳ tím chuyển sang màu xanh.
Gly, Ala, Val không làm đổi màu quỳ.
Glu làm quỳ tím chuyển màu đỏ.
Phương trình tổng quát của amino axit tác dụng với HCl
H2N)b – R – (COOH)a + bHCl → (ClH3N)b – R- (COOH)a + aH2O
m amino axit + 36.5. nHCl pư = m muối → nHCl pư = (m muối – mamioaxit): 36.5
Mời các bạn tham khảo thêm các bài viết dưới đây của chúng tôi:
- Giải bài tập Hóa 12 nâng cao bài 12
- Đề thi giữa học kì 2 lớp 12 môn Hóa học năm 2018 - 2019 trường THPT Trần Phú - TP. Hồ Chí Minh
- Đề thi giữa học kì 2 lớp 12 môn Hóa học năm 2018 - 2019 trường THPT Nguyễn Chí Thanh - TP. HCM
- Đề thi giữa học kì 2 lớp 12 môn Hóa học năm 2018 - 2019 trường THPT Ngô Quyền - Hải Phòng
- Đề thi học kì 2 lớp 12 môn Hóa học năm 2018 - 2019 trường THPT Yên Lạc 2 - Vĩnh Phúc
- Đề thi học kì 2 lớp 12 môn Hóa học năm 2018 - 2019 trường THPT Nguyễn Chí Thanh - TP. HCM
Trên đây VnDoc đã giới thiệu tới các bạn Amino axit là gì? - Đầy đủ kiến thức từ A-Z để ôn thi THPT QG 2020. Để có kết quả cao hơn trong học tập, VnDoc xin giới thiệu tới các bạn học sinh tài liệu Giải bài tập Toán lớp 12, Giải bài tập Hóa học lớp 12, Giải bài tập Vật Lí 12, Tài liệu học tập lớp 12 mà VnDoc tổng hợp và đăng tải.
