Đề thi thử THPT Quốc gia năm 2020 môn Hóa học Trường THPT Chuyên Trần Phú, Hải Phòng



Đề thi thử THPT Quốc gia năm 2020 môn Hóa học Trường THPT Chuyên Trần Phú, Hải Phòng được VnDoc tổng hợp, biên soạn kèm đáp án, hướng dẫn giải chi tiết. Hy vọng với đề thi thử THPT của các trường đưa ra sẽ giúp các em ôn luyện đề tốt hơn, chuẩn bị cho kì thi THPT quốc gia môn Hóa học.
Để tài đề thi và xem toàn bộ nội dung chi tiết tài liệu vui lòng kéo xuống ấn tải link bên dưới
Đề thi thử tốt nghiệp THPT Quốc gia 2020 môn Hóa Chuyên Trần Phú
Đáp án đề thi thử THPT Quốc gia năm 2020 môn Hóa học Trường THPT Chuyên Trần Phú, Hải Phòng
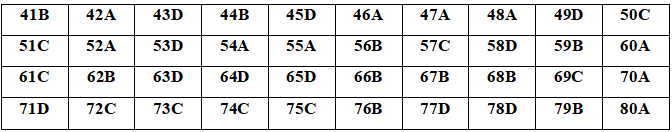
Hướng dẫn lời giải chi tiết đề thi thử THPT Quốc gia năm 2020 môn Hóa học Trường THPT Chuyên Trần Phú, Hải Phòng
Câu 41: Kim loại nào sau đây tác dụng với dung dịch kiềm, giải phóng khí H2?
A. Cu
B. Al
C. Fe
D. Ag
Hướng dẫn giải
Câu 42: Ở điều kiện thích hợp, kim loại Al không tác dụng với chất nào sau đây?
A. MgO
B. ZnO
C. Fe3O4
D. CuO
Hướng dẫn giải
Al tác dụng được với các oxit kim loại yếu hơn Al (phản ứng nhiệt nhôm)
Câu 43: Chất phản ứng được với dung dịch H2SO4 tạo thành kết tủa màu trắng là
A. NaOH
B. NaCl
C. Na2CO3
D. BaCl2
Hướng dẫn giải
Câu 44: Este nào sau đây tác dụng với dung dịch NaOH thu được anđehit axetic?
A. CH2=CHCOOCH3
B. CH3COOCH=CH2
C. CH3COOCH3
D. HCOOCH2CH=CH2
Hướng dẫn giải
Câu 48: Chất nào sau đây vừa phản ứng với dung dịch NaOH loãng, vừa phản ứng với dung dịch HCl loãng?
A. Fe(NO3)2
B. CrCl3
C. NaAlO2
D. Cr2O3
Hướng dẫn giải
Câu 53: Dung dịch Fe2(SO4)3 không tác dụng với chất nào sau đây?
A. BaCl2
B. Fe
C. NaOH
D. Ag
Hướng dẫn giải
Câu 58: Hiđro hóa hiđrocacbon X thu được butan. X tác dụng với dung dịch AgNO3 trong NH3, thu được kết tủa. Số công thức cấu tạo của X là
A. 2
B. 4
C. 1
D. 3
Hướng dẫn giải
Các CTCT phù hợp của X là:
Câu 60: Hỗn hợp X gồm Zn và kim loại M. Cho 14,9 gam X tác dụng với dung dịch NaOH dư thu được 2,24 lít khí (đktc) và chất rắn không tan. Mặt khác cho 14,9 gam X tác dụng hoàn toàn với lượng dư dung dịch HNO3 đặc, nóng, thu được 14,56 lít khí NO2 (là sản phẩm khử duy nhất, đktc). Kim loại M là
A. Fe
B. Mg
C. Ag
D. Cu
Hướng dẫn giải
Với NaOH dư chỉ có Zn tan nên
Với HNO3 dư thì M có hóa trị x.
Câu 64: Cho hỗn hợp X gồm 0,15 mol Na và 0,2 mol Al vào nước dư, sau phản ứng hoàn toàn thấy thoát ra V lít khí H2 (đktc). Giá trị của V là
A. 7,84
B. 1,12
C. 4,48
D. 6,72
Hướng dẫn giải
nAl (pư) = nNa = 0,15
(pư) =>
Câu 67: Cho 0,05 mol hỗn hợp 2 este đơn chức X và Y phản ứng vừa đủ với dung dịch NaOH thu được hỗn hợp các chất hữu cơ Z. Đốt cháy hoàn toàn Z thu được 0,165 mol CO2 và 0,035 mol Na2CO3. Nếu làm bay hơi hỗn hợp Z thu được m gam chất rắn khan. Giá trị của m là
A. 5,64
B. 5,72
C. 4,56
D. 3,40
Hướng dẫn giải
hỗn hợp ban đầu có este của ancol (0,03 mol) và este của phenol (0,02 mol)
Este của phenol ít nhất 7C nên este của ancol 2C hoặc 3C
TH1:
Cấu tạo:
Muối gồm HCOONa (0,05) và C6H5Ona (0,02) => mmuối = 5,72 gam
TH2: vô nghiệm
Câu 69: Cho a gam Gly-Ala-Glu tác dụng hết với một lượng dư dung dịch NaOH, đun nóng. Sô mol NaOH đã tham gia phản ứng là 0,6 mol. Tổng khối lượng muối thu được là
A. 75,4
B. 79,8
C. 59,85
D. 60,45
Hướng dẫn giải
=> mmuối = 59,85 gam
Câu 71: Hỗn hợp X gồm tristearin, tripanmitin và axit stearic, axit panmitic. Đốt cháy hoàn toàn m gam X cần dùng vừa đủ 4,38 mol O2, thu được 3,06 mol CO2 và 2,98 mol H2O. Cho m gam X tác dụng hoàn toàn với dung dịch NaOH dư, thu được a gam hỗn hợp muối. Giá trị của a là
A. 51,24
B. 49,60
C. 48,12
D. 50,34
Hướng dẫn giải
X gồm chất béo (tổng a mol), axit béo (tổng b mol)
Chất béo có k = 3 và axit béo có k = 1 nên
Ngoài ra các bạn có thể tham khảo thêm một số đề thi thử năm 2020 môn Hóa học mới nhất của các trường THPT
- Đề thi thử THPT Quốc gia năm 2020 môn Hóa học Sở GD&ĐT Ninh Bình lần 2
- Đề thi thử THPT Quốc gia năm 2020 môn Hóa học cụm Sóc Sơn Hà Nội
- Bộ đề thi thử THPT quốc gia năm 2020 môn Hóa học
Đề thi thử THPT Quốc gia năm 2020 môn Hóa học Trường THPT Chuyên Trần Phú, Hải Phòng được đánh giá là đề thi thử THPT Quốc gia với nhiều câu hỏi hay, nội dung đề thi bám sát khung đề thi THPT Quốc gia do Bộ GD&ĐT đưa ra trước đó, với đề thi này thì sẽ phân hóa được học sinh ở các mức học tập khác nhau.
Trên đây VnDoc đã giới thiệu Đề thi thử THPT Quốc gia năm 2020 môn Hóa học Trường THPT Chuyên Trần Phú, Hải Phòng tới bạn đọc. Để có kết quả cao hơn trong kì thi, VnDoc xin giới thiệu tới các bạn học sinh tài liệu Thi thpt Quốc gia môn Toán, Thi THPT Quốc gia môn Hóa học, Thi THPT Quốc gia môn Vật Lý, mà VnDoc tổng hợp và đăng tải.
Ngoài ra, VnDoc.com đã thành lập group chia sẻ tài liệu ôn tập THPT Quốc gia miễn phí trên Facebook: Quyết tâm đỗ Đại Học Mời các bạn học sinh tham gia nhóm, để có thể nhận được những tài liệu, đề thi mới nhất.