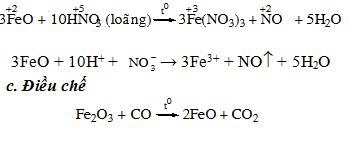Giáo án Hóa học lớp 12 bài 32: Hợp chất của sắt
Giáo án môn Hóa học lớp 12
Giáo án Hóa học lớp 12 bài 32: Hợp chất của sắt được VnDoc sưu tầm và giới thiệu để có thể chuẩn bị giáo án và bài giảng hiệu quả, giúp quý thầy cô tiết kiệm thời gian và công sức làm việc. Giáo án môn Hóa học 12 này được soạn phù hợp quy định Bộ Giáo dục và nội dung súc tích giúp học sinh dễ dàng hiểu bài học hơn.
Giáo án Hóa học lớp 12 bài 30: Thực hành tính chất của natri, magie, nhôm và hợp chất của chúng
I. MỤC TIÊU BÀI HỌC
1. Kiến thức:
Biết được: tính chất vật lí, nguyên tắc điều chế và ứng dụng của một số hợp chất của sắt.
Hiểu được:
- Tính khử của hợp chất sắt (II): FeO, Fe(OH)2, muối sắt (II).
- Tính oxi hoá của hợp chất sắt (III): Fe2O3, Fe(OH)3, muối sắt (III).
2. Kỹ năng:
- Dự đoán, kiểm tra bằng thí nghiệm và kết luận được tính chất hoá học các hợp chất của sắt.
- Viết các PTHH phân tử hoặc ion rút gọn minh hoạ tính chất hoá học.
- Nhận biết được ion Fe2+, Fe3+ trong dung dịch.
- Tính % khối lượng các muối sắt hoặc oxit sắt trong phản ứng.
- Xác định công thức hoá học oxit sắt theo số liệu thực nghiệm.
Trọng tâm:
- Khả năng phản ứng của các hợp chất sắt (II) và sắt (III).
- Phương pháp điều chế các hợp chất sắt (II) và sắt (III).
3. Tư tưởng: Yêu thích và ham mê học tập môn Hóa học
II. CHUẨN BỊ CỦA GIÁO VIÊN VÀ HỌC SINH
1. Giáo viên: Đinh sắt, mẩu dây đồng, dung dịch HCl, dung dịch NaOH, dung dịch FeCl3.
2. Học sinh: Làm BTVN, đọc bài mới trước khi đến lớp
III. PHƯƠNG PHÁP
Kết hợp khéo léo giữa đàm thoại, nêu vấn đề và hoạt động nhóm
IV. TIẾN TRÌNH BÀI GIẢNG
Tiết 54
1. Ổn định tổ chức:
2. Kiểm tra bài cũ: Tính chất hoá học cơ bản của sắt là gì? Dẫn ra các PTHH để minh hoạ.
3. Bài mới:
|
Hoạt động của Giáo viên và Học sinh |
Nội dung ghi bảng |
|
* Hoạt động 1: - GV: Em hãy cho biết tính chất hoá học cơ bản của hợp chất sắt (II) là gì? Vì sao? HS: Trả lời |
I – HỢP CHẤT SẮT (II) Tính chất hoá học cơ bản của hợp chất sắt (II) là tính khử. Fe2+ → Fe3+ + 1e |
|
* Hoạt động 2: - GV: Yêu cầu HS cho biết TCVL của FeO HS: nghiên cứu tính chất vật lí của sắt (II) oxit. - GV: Yêu cầu HS lên bảng minh họa TCHH của FeO HS: viết PTHH của phản ứng biểu diễn tính khử của FeO. - GV: giới thiệu cách điều chế FeO. HS: Nghe TT |
1. Sắt (II) oxit a. Tính chất vật lí: (SGK) b. Tính chất hoá học
|
|
* Hoạt động 3: - GV: Yêu cầu HS cho biết TCVL của Fe(OH)2 HS: nghiên cứu tính chất vật lí của sắt (II) hiđroxit. - GV: biểu diễn thí nghiệm điều chế Fe(OH)2. HS: quan sát hiện tượng xảy ra và giải thích vì sao kết tủa thu được có màu trắng xanh rồi chuyển dần sang màu nâu đỏ. |
2. Sắt (II) hiđroxit a. Tính chất vật lí : (SGK) b. Tính chất hoá học Thí nghiệm: Cho dung dịch FeCl2 + dung dịch NaOH FeCl2 + 2NaOH → Fe(OH)2¯ + 2NaCl 4Fe(OH)2 + O2 + 2H2O → 4Fe(OH)3 c. Điều chế: Điều chế trong điều kiện không có không khí. |
|
* Hoạt động 4: - GV: Yêu cầu HS cho biết TCVL của muối sắt (II) HS: nghiên cứu tính chất vật lí của muối sắt (II). |
3. Muối sắt (II) a. Tính chất vật lí : Đa số các muối sắt (II) tan trong nước, khi kết tinh thường ở dạng ngậm nước. Thí dụ: FeSO4.7H2O; FeCl2.4H2O |
|
- GV: Yêu cầu HS lên bảng minh họa TCHH của muối sắt (II) HS: lấy thí dụ để minh hoạ cho tính chất hoá học của hợp chất sắt (II). - GV: giới thiệu phương pháp điều chế muối sắt (II). HS: Nghe TT - GV: Vì sao dung dịch muối sắt (II) điều chế được phải dùng ngay? HS: Nghe TT |
b. Tính chất hoá học c. Điều chế: Cho Fe (hoặc FeO; Fe(OH)2) tác dụng với HCl hoặc H2SO4 loãng. Fe + 2HCl → FeCl2 + H2 FeO + H2SO4 → FeSO4 + H2O % Dung dịch muối sắt (II) điều chế được phải dùng ngay vì trong không khí sẽ chuyển dần thành muối sắt (III). |
4. Củng cố bài giảng:
Viết PTHH của các phản ứng trong quá trình chuyển đổi sau:
5. Bài tập về nhà:
- Bài tập về nhà: 1 → 3 trang 145 (SGK)
- Xem trước phần HỢP CHẤT SẮT III