Bộ đề thi thử THPT Quốc gia năm 2016 môn Hóa học - Số 3
Đề thi thử THPT Quốc gia 2016 môn Hóa học
Bộ đề thi thử THPT Quốc gia năm 2016 môn Hóa học - Số 2 được VnDoc.com sưu tầm và đăng tải, là tài liệu luyện thi Đại học, Cao đẳng 2016, ôn thi THPT Quốc gia hữu ích dành cho các bạn học sinh lớp 12, mời các bạn tham khảo. Đề thi có đáp án đi kèm, các bạn có thể tra cứu thuận tiện khi làm bài.
Bộ đề thi thử THPT Quốc gia năm 2016 môn Hóa học - Số 1
Bộ đề thi thử THPT Quốc gia năm 2016 môn Hóa học - Số 2
Chi tiết: Đề thi thử THPT Quốc gia môn Hóa học trường THPT Phú Nhuận, TP. HCM
|
SỞ GD&ĐT TP HỒ CHÍ MINH THPT PHÚ NHUẬN |
ĐỀ THI THỬ ĐẠI HỌC 2015 – LẦN 1 MÔN: HÓA – KHỐI A, B Thời gian: 90 phút (50 câu trắc nghiệm) |
|
|
|
Mã đề thi 134 |
|
Cho biết nguyên tử khối của các nguyên tố:
H = 1; C = 12; N = 14; O = 16; Na = 23; Mg = 24; Al = 27; P = 31; S = 32; Cl = 35,5; K= 39 ; Fe = 56 ; Cu = 64 ; Ag=108 ; Ba = 137.
Câu 1: Cho hỗn hợp gồm 1 mol chất X và 1 mol chất Y tác dụng hết với dung dịch H2SO4 đặc nóng (dư) tạo ra 1 mol khí SO2 (sản phẩm khử duy nhất). Hai chất X, Y là:
A. Fe, Fe2O3. B. FeO, Fe3O4 C. Fe, FeO D. Fe3O4, Fe2O3.
Câu 2: Phát biểu nào sau đây là sai ?
A. Cho Cu(OH)2 vào dung dịch lòng trắng trứng thấy xuất hiện màu vàng
B. Dung dịch lysin làm xanh quỳ tím.
C. Anilin tác dụng với nước brom tạo thành kết tủa trắng.
D. Dung dịch glyxin không làm đổi màu quỳ tím.
Câu 3: Amino axit X trong phân tử chỉ chứa hai loại nhóm chức. Cho 0,1 mol X tác dụng vừa đủ với 0,2 mol NaOH, thu được 17,7 gam muối. Số nguyên tử hiđro trong phân tử X là
A. 6. B. 9. C. 7. D. 8.
Câu 4: Nhỏ từ từ đến dư dung dịch NaOH loãng vào mỗi dung dịch sau: FeCl3, CuCl2, AlCl3, FeSO4, BaCl2. Sau khi các phản ứng xảy ra hoàn toàn, số trường hợp thu được kết tủa là :
A. 3 B. 4 C. 2 D. 1
Câu 5: Khí X làm đục nước vôi trong và được dùng để làm chất tẩy trắng bột gỗ trong công nghiệp giấy. Chất X là :
A. NH3. B. O3. C. SO2 D. CO2.
Câu 6: Có bao nhiêu tripeptit (mạch hở) khi thủy phân hoàn toàn đều thu được sản phẩm gồm alanin và glyxin?
A. 4. B. 5. C. 7. D. 6.
Câu 7: Hấp thụ hoàn toàn 3,36 lít khí CO2 (đktc) vào dung dịch chứa 0,15 mol NaOH và 0,1 mol Ba(OH)2, thu được khối lượng kết tủa là:
A. 14,775 g B. 9,85 g C. 29,55 g D. 19,7 g
Câu 8: Từ xenluloz và axit nitric đem điều chế xenluloz trinitrat (chất dễ cháy, dễ nổ mạnh). Thể tích axit nitric 99,67% (d=1,52g/ml) cần để sản xuất 59,4 kg xenluloz trinitrat (hiệu suất 90%) là:
A. 27,72 lít B. 11,2 lít C. 26,52 lít D. 32,52 lít
Câu 9: Phản ứng nào dưới đây thuộc loại phản ứng oxi hóa – khử?
A. AgNO3 + HCl → .. . B. NO2 + NaOH → .. .
C. CaO + CO2 → .. . D. NaOH + HCl → .. .
Câu 10: Hổn hợp X gồm Fe và kim loại M có hóa trị không đổi. Chia 7,22g X thành 2 phần bằng nhau .
- Phần I: Tác dụng với dd HCl dư cho ra 2,128 lit H2 (đkc)
- Phần II: Tác dụng với dd HNO3 loãng dư cho ra khí duy nhất là NO có thể tích là 1,792 lit khí (ĐKC). Kim loại M và % m kim loại M trong hh X là:
A. Al & 53,68% B. Cu & 25,87% C. Zn & 48,12 % D. Al & 22,44%
(Còn tiếp)
Chi tiết: Đề thi thử THPT Quốc gia môn Hóa học trường THPT Đoàn Thượng, Hải Dương
|
SỞ GD & ĐT HẢI DƯƠNG TRƯỜNG THPT ĐOÀN THƯỢNG |
ĐỀ THI THỬ THPT QUỐC GIA LẦN III NĂM HỌC 2014 - 2015 Môn thi: Hóa học Thời gian làm bài: 90 phút (đề thi gồm 05 trang, 50 câu trắc nghiệm) |
|
|
|
Mã đề thi 132 |
|
Cho nguyên tử khối của một số nguyên tố: H=1, C=12, N=14, O=16, Li=7, Na=23, Mg=24, Al=27, S=32, Cl=35,5, K=39, Ca=40, Fe=56, Cu=64, Zn=65, Br=80, Ag=108, Ba=137.
Câu 1: Cho các chất sau: Fe2O3, ZnO, Fe3O4, FeSO4, Ag, CuO, Al. Số chất tác dụng với H2SO4 đặc, nóng giải phóng khí SO2 là
A. 5. B. 3. C. 4. D. 6.
Câu 2: Công thức cấu tạo của metyl propionat là
A. HCOOCH3. B. C2H5COOCH = CH2.
C. CH3COOC2H5. D. C2H5COOCH3.
Câu 3: Phát biểu nào sau đây là sai?
A. Thiếc có thể dùng để phủ lên bề mặt của sắt để chống gỉ.
B. Nhôm là kim loại dẫn điện tốt hơn đồng.
C. Chì (Pb) có ứng dụng để chế tạo thiết bị ngăn cản tia phóng xạ.
D. Trong y học, ZnO được dùng làm thuốc giảm đau dây thần kinh, chữa bệnh eczema, bệnh ngứa.
Câu 4: Hỗn hợp X gồm một số amino axit no (chỉ có nhóm chức –COOH và –NH2, không có nhóm chức khác) có tỉ lệ khối lượng mO: mN = 48:19. Để tác dụng vừa đủ với 39,9 gam hỗn hợp X cần 380 ml dung dịch HCl 1M. Mặt khác đốt cháy 39,9 gam hỗn hợp X cần 41,776 lít O2 (đktc) thu được m gam CO2. m có giá trị là
A. 88. B. 59,84. C. 61,60. D. 66.
Câu 5: Có bao nhiêu tripeptit (mạch hở) khi thuỷ phân hoàn toàn đều thu được sản phẩm gồm alanin và glyxin?
A. 6. B. 5. C. 7. D. 4.
Câu 6: Axit cacboxylic X hai chức (có phần trăm khối lượng của oxi nhỏ hơn 70%), Y và Z là hai ancol đồng đẳng kế tiếp (MY < MZ). Đốt cháy hoàn toàn 0,2 mol hỗn hợp gồm X, Y, Z cần vừa đủ 8,96 lít khí O2 (đktc), thu được 7,84 lít khí CO2 (đktc) và 8,1 gam H2O. Phần trăm khối lượng của Y trong hỗn hợp trên là
A. 29,9%. B. 15,9%. C. 29,6%. D. 12,6%.
Câu 7: Để khử mùi tanh của cá (đặc biệt là cá mè) do hỗn hợp một số amin (nhiều nhất là trimetylamin) và một số chất khác gây nên. Người ta dùng dung dịch nào sau đây?
A. Nước vôi trong. B. Giấm. C. Muối ăn. D. Thuốc tím.
Câu 8: Dãy gồm các kim loại đều phản ứng với nước ở nhiệt độ thường tạo ra dung dịch có môi trường kiềm là
A. Na, Mg, K. B. Na, Fe, K. C. Na, Ba, Ca. D. Be, Na, Ca.
Câu 9: Cho sơ đồ chuyển hóa: ![]()
Triolein X Y Z. Tên của Z là
A. axit stearic. B. axit oleic. C. axit panmitic. D. axit linoleic.
Câu 10: Cho 11,25 gam C2H5NH2 tác dụng vừa đủ với 200 ml dung dịch HCl a(M). Sau khi phản ứng hoàn toàn thu được dung dịch (X) chỉ chứa 22,2 gam muối. Giá trị của a là
A. 1,3. B. 1,5. C. 1,36. D. 1,25.
(Còn tiếp)
Chi tiết: Đề thi thử THPT Quốc gia môn Hóa học trường THPT Đa Phúc, Hà Nội
|
TRƯỜNG THPT ĐA PHÚC (Đề thi gồm 50 câu, 04 trang) |
ĐỀ THI THỬ QUỐC GIA LẦN III NĂM 2015 Môn: HÓA HỌC Thời gian làm bài: 90 phút; không kể thời gian phát đề |
Mã đề: 289 |
|
Cho biết nguyên tử khối (theo đvC) của các nguyên tố:
H = 1; He = 4; Li = 7; Be = 9; C = 12; N = 14; O = 16; Na = 23; Mg = 24; Al = 27; S = 32; Cl = 35,5; K = 39; Ca = 40; Cr = 52; Mn = 55; Fe = 56; Cu = 64; Zn = 65; Br = 80; Rb = 85; Sr = 88; Ag = 108; Sn = 119; Cs = 133; Ba = 137; Pb = 207; I = 127.
Câu 1. Trước đây, Freon được dùng làm chất sinh hàn trong tủ lạnh và máy điều hòa nhiệt độ. Từ năm 1996, Freon đã bị cấm sử dụng, nguyên nhân chính là do khi thải vào khí quyển
A. freon phá hủy tầng ozon. B. freon gây ra hiệu ứng nhà kính.
C. freon gây ra mưa axit. D. freon gây ra hiện tượng El Nino.
Câu 2. Dãy gồm các chất trong phân tử chỉ chứa liên kết cộng hóa trị không phân cực là
A. H2O, HCl, O2 B. Cl2, NH3, CO2 C. HCl, HF, NH3 D. HF, H2O, N2
Câu 3. Chất nào sau đây là chất điện li yếu
A. NaOH B. CH3COOH C. HCl D. BaCl2
Câu 4. Chất X là chất rắn, màu vàng ở nhiệt độ thường. Người ta thường sử dụng chất X để thu gom thủy ngân khi nhiệt kế bị vỡ. X là:
A. Silic B. Cacbon C. Photpho D. Lưu huỳnh
Câu 5. Dãy gồm các kim loại đều có thể được điều chế bằng phương pháp điện phân dung dịch muối của chúng:
A. Fe, Cu, Ag B. Al, Fe, Cr C. Mg, Zn, Cu D. Na, Fe, Ni
Câu 6. Có bốn chất rắn riêng biệt: Na, Mg, Al2O3, Al. Thuốc thử dùng để phân biệt bốn chất trên là
A. NaOH B. Ba(OH)2 C. H2O D. HCl
Câu 7. Cho sơ đồ phản ứng sau: X + H2SO4 đặc nóng → Fe2(SO4)3 + SO2 + H2O
X không thể là chất nào sau đây:
A. Fe(OH)2 B. Fe3O4 C. FeO D. Fe2O3
Câu 8. Cho các chất sau: NaCl, Ba(OH)2, K2CO3, HCl, NaHSO4, Na3PO4. Số chất có thể làm mềm nước cứng tạm thời là
A. 1 B. 2 C. 3 D. 4
Câu 9. Tên của hợp chất hữu cơ có công thức CH3COOCH(CH3)2 là
A. propyl axetat B. Isopropyl axetat C. Metyl butirat D. Etyl fomat
Câu 10. Số đồng phân amin bậc 2 có công thức phân tử C4H11N là
A. 2 B. 3 C. 4 D. 5
(Còn tiếp)
Chi tiết: Đề thi thử THPT Quốc gia môn Hóa học trường THPT Lương Ngọc Quyến, Thái Nguyên
|
SỞ GD & ĐT THÁI NGUYÊN TRƯỜNG THPT LƯƠNG NGỌC QUYẾN |
ĐỀ THI THỬ THPT QUỐC GIA NĂM 2015 Môn: HOÁ HỌC Thời gian làm bài: 90 phút, không kể thời gian phát đề |
||
|
Họ và tên thí sinh:……………………………... Số báo danh: ……… |
Mã đề thi 304 |
||
ĐỀ THI GỒM 50 CÂU (TỪ CÂU 1 ĐẾN CÂU 50) DÀNH CHO TẤT CẢ THÍ SINH
(Cho biết nguyên tử khối của các nguyên tố: H=1; C=12; N=14; O=16; Na=23; Mg=24; Al=27; P=31; S=32; Cl=35,5; K=39; Ca=40; Cr=52; Mn=55; Fe=56; Cu=64; Zn=65; Br=80; Ag=108; Ba=137).
Câu 1: Trong tự nhiên, canxi sunfat tồn tại dưới dạng ngậm nước (CaSO4. 2H2O) gọi là
A. thạch cao sống. B. đá vôi. C. thạch cao nung. D. thạch cao khan.
Câu 2: Công thức chung của amin no, đơn chức, mạch hở là
A. CnH2n+1N (n ≥ 2). B. CnH2n+3N (n ≥ 1). C. CnH2n-1N (n ≥ 2). D. CnH2n-5N (n ≥ 6).
Câu 3: Cho phương trình hóa học sau: K2SO3 + K2Cr2O7 + KHSO4 → K2SO4 + Cr2(SO4)3 + H2O.
Hệ số của KHSO4 và K2SO4 lần lượt là:
A. 8;1. B. 8; 8. C. 2;3 D. 1; 8.
Câu 4: Trong tự nhiên Cl có 2 đồng vị 35Cl và 37Cl, nguyên tử khối trung bình của Cl là 35,5. Thành phần % vê khối lượng đồng vị 37Cl trong FeCl3 là:
A. 48,46% B. 17,08%. C. 16,40%. D. 65,54% .
Câu 5: Nhiệt phân hoàn toàn 34,56 gam hỗn hợp KNO3 và Cu(NO3)2, thu được hỗn hợp khí X (tỉ khối của X so với khí hiđro bằng 18,8). Khối lượng của Cu(NO3)2 trong hỗn hợp ban đầu là:
A. 11,28 gam. B. 9,40 gam. C. 8,60 gam. D. 20,50 gam.
Câu 6: Cho dãy các kim loại: Ag, Zn, Fe, Cu, Cr, Sn. Số kim loại trong dãy không phản ứng với dung dịch HCl là:
A. 1. B. 3. C. 4. D. 2.
Câu 7: Cho các cách phát biểu sau:
(1) Trong quá trình sản xuất axit H2SO4 để hấp thụ SO3 người ta dùng H2SO4 đặc.
(2) Trong công nghiệp người ta sản xuất oxi bằng cách cho MnO2 tác dụng với dung dịch axit HCl.
(3) Kim cương, than chì, fuleren và cacbon vô định hình là các dạng thù hình của cacbon.
(4) Để loại bỏ khí Cl2 trong phòng thí nghiệm dùng dung dịch NH3 loãng.
(5) SO2 là khí độc và khi tan trong nước mưa tạo thành axit gây ra sự ăn mòn kim loại và các vật liệu.
(6) Muốn pha loãng dung dịch H2SO4 đặc, cần rót từ từ dung dịch axit đặc vào nước.
(7) Để loại bỏ H2S ra khỏi hỗn hợp khí với H2 bằng cách cho hỗn hợp lội qua dung dịch NaOH hoặc Pb(NO3)2.
(8) Axit H3PO4 là axit mạnh vì nguyên tố P ở trạng thái oxi hóa cao nhất (+5).
(9) Thuốc thử để phân biệt O2 và O3 là KI có tẩm hồ tinh bột.
Trong các cách phát biểu trên, số phát biểu đúng là:
A. 4. B. 7. C. 3. D. 8.
Câu 8: Có 2 bình điện phân đặt nối tiếp nhau. Bình (1) chứa V lít dung dịch CuCl2 2x(M), bình (2) chứa 2V lít dung dịch AgNO3 xM. Thực hiện điện phân với điện cực trơ trong thời gian 50 phút, cường độ dòng điện 1,93A. Trộn 2 dung dịch còn lại trong hai bình điện phân xuất hiện kết tủa và trong dung dịch sau khi trộn có 0,08 mol ion Cl-. Nồng độ mol/l của mỗi dung dịch ban đầu lần lượt là:
A. 0,08/V; 0,02/V B. 0,02/V; 0,04/V. C.0,05/V; 0,04/V D. 0,08/V; 0,04/V
Câu 9: Cho hỗn hợp gồm 0,01 mol FeO và 0,02 mol Fe2O3 tác dụng với dung dịch chứa 0,14 mol HCl thu được dung dịch X. Cho X vào dung dịch KMnO4 và H2SO4 loãng thu được khí B. Số mol khí B thu được là:
A. 0,035 mol. B. 1,4 mol. C. 0,14 mol. D. 0,07 mol.
Câu 10: Nhúng một thanh Al nặng 45gam vào 400ml dung dịch CuSO4 0,5M. Sau một thời gian lấy thanh Al ra cân nặng 46,38 gam. Khối lượng Cu thoát ra là:
A. 0,64 gam. B. 1,28 gam. C. 2,56 gam. D. 1,92 gam.
(Còn tiếp)
Chi tiết: Đề thi thử THPT Quốc gia môn Hóa học trường THPT Chuyên Lý Tự Trọng, Cần Thơ
|
SỞ GIÁO DỤC VÀ ĐÀO TẠO CẦN THƠ TRƯỜNG THPT CHUYÊN LÝ TỰ TRỌNG |
ÐỀ THI THỬ THPT QUỐC GIA LẦN III NĂM 2015 Môn: HÓA HỌC Thời gian làm bài: 90 phút (50 câu trắc nghiệm) |
||
|
|
Mã đề thi 143 |
||
Họ, tên thí sinh:..........................................................................
Số báo danh:...............................................................................
Cho nguyên tử khối của các nguyên tố:
H = 1; C = 12; N = 14; O = 16; S = 32; Cl = 35,5; Br = 80; P = 31; Na = 23; Mg = 24; Al = 27; K = 39; Ca = 40; Cr = 52; Mn = 55; Fe = 56; Cu = 64; Zn = 65; Ag = 108; Ba = 137; Pb = 207; Ni = 59; As = 75.
Câu 1: Cho các cân bằng sau:
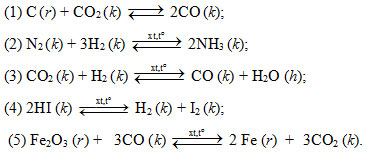
Khi thay đổi áp suất, những cân bằng hoá học bị chuyển dịch là
A. (1) và (2). B. (1), (2), (3) và (4). C. (1), (2) và (5). D. (3), (4) và (5).
Câu 2: Cho các thí nghiệm sau:
(1) Cho bột magie vào dung dịch HCl.
(2) Cho miếng kẽm vào dung dịch CuSO4.
(3) Cho đinh thép vào dung dịch muối ăn.
(4) Cho miếng gang vào dung dịch HCl.
(5) Cho miếng thiếc vào dung dịch H2SO4 loãng.
Số trường hợp xảy ra sự ăn mòn điện hoá là
A. 4. B. 2. C. 3. D. 1.
Câu 3: Trong bốn chất HF, HCl, HBr, HI, chất có tính khử mạnh nhất và chất có lực axit mạnh nhất lần lượt là
A. đều là HF. B. HF và HI. C. đều là HI. D. HI và HF.
Câu 4: Cho các chất sau: HCN, NH4CN, (CH3COO)2Ba, CH4ON2, C6H6Cl6, H3CNO2, CCl4, H2C2O4. Số chất hữu cơ là
A. 4 B. 6. C. 7 D. 5.
Câu 5: Cho m gam hỗn hợp X gồm FeO, Fe2O3 và Fe3O4 tác dụng vừa đủ với dung dịch H2SO4 loãng, dư thu được dung dịch Y. Cô cạn dung dịch Y được 27,600 gam muối khan. Nếu cho dung dịch Y tác dụng với Cl2 dư thì thu được 29,375 gam muối. Giá trị của m là
A. 19,600. B. 23,200. C. 7,600. D. 11,600.
Câu 6: Cho các phát biểu sau:
(1) Dung dịch nước của anilin không làm quì tím hóa xanh nhưng dung dịch nước của benzyl amin làm quì tím hóa xanh.
(2) Phenyl amoni clorua và phenol đều làm mất màu nước brom.
(3) Hỗn hợp gồm alanin, glixin và valin khi đun nóng tạo số tripeptit là 6.
(4) Ứng với công thức phân tử C2H7O2N có 2 chất phản ứng được với dung dịch NaOH vừa phản ứng được với dung dịch HCl?
(5) Để phân biệt 3 dung dịch: H2N − CH2 − CH2COOH, CH3COOH, C2H5−NH2, chỉ cần dùng một thuốc thử là quì tím.
Các phát biểu đúng là
A. 1, 3, 4. B. 1, 4, 5. C. 1, 3, 5. D. 3, 4, 5.
Câu 7: Cho 38,7 gam hỗn hợp A gồm một ancol đơn chức X và một axit cacboxylic đơn chức Y (cả hai đều mạch hở). Chia A thành 3 phần bằng nhau. Đem phần 1 tác dụng hết với Na, thu được 2,8 lít H2 (đktc). Đốt cháy hết phần 2 thì thu được 19,8 gam CO2. Đem phần 3 thực hiện phản ứng este hóa với hiệu suất 60%, sau phản ứng thấy có 1,08 gam nước sinh ra. Khẳng định nào sau đây sai?
A. Y tham gia phản ứng tráng gương.
B. Y không có đồng phân.
C. X không làm mất màu nước brom.
D. Từ X có thể điều chế được axit axetic bằng một phản ứng.
Câu 8: Cho phản ứng sau:
K2SO3 + KMnO4 + KHSO4 → K2SO4 + MnSO4 + H2O. Tổng hệ số nguyên, tối giản của các chất tham gia phản ứng sau khi cân bằng là
A. 13. B. 15. C. 17. D. 11.
Câu 9: Hỗn hợp A gồm 0,15 mol hai ancol đồng đẳng liên tiếp. Đốt cháy hoàn toàn A thu được 0,25 mol CO2. Mặt khác oxi hóa A thì thu được hỗn hợp B gồm các axit và andehit tương ứng (biết có x% lượng ancol biến thành andehit phần còn lại biến thành axit, hiệu suất phản ứng hai ancol là như nhau).Cho B vào lượng dư dung dịch AgNO3/NH3, đun nóng thu được 30,24 gam Ag. Giá trị của x là
A. 70,00% B. 51,43% C. 60,00% D. 50,00%
Câu 10: Công thức của tristearin là
A. (CH3[CH2]16COO)3C3H5. B. (CH3[CH2]7CH=CH[CH2]7COO)3C3H5.
C. (CH3[CH2]15COO)3C3H5. D. (CH3[CH2]14COO)3C3H5.
(Còn tiếp)